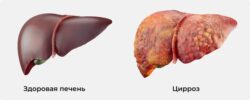
От редакции: диагноз «дисбактериоз» не включён в международную классификацию болезней (МКБ-10), его используют врачи только в России и странах СНГ. Дисбактериоз сопутствует другим патологиям, но было бы неверно однозначно утверждать, что эти патологии вызывает именно нарушение баланса микрофлоры. Изучение взаимосвязи между деятельностью микробиома и возникновением различных заболеваний — одно из перспективных направлений в медицинских исследованиях.
Что такое микрофлора кишечника и для чего она нужна
Организм человека населяют свыше триллиона бактерий. В их микробиоме в сто раз больше генов, чем в нашем собственном геноме. Они живут на коже, слизистых, в пищеварительном тракте.
Кишечное сообщество, которое мы приютили в своём организме, обладает метаболической активностью, как у целого органа. Оно помогает нам выжить, поэтому мы в корне зависим от наших колонизаторов, как и они от нас.
В норме кишечник обеспечивает среду для роста микроорганизмов, а флора поддерживает «равновесие» в организме хозяина:
- стимулирует рост энтероцитов — клеток кишечной стенки;
- помогает перерабатывать и усваивать питательные вещества;
- подавляет рост патогенных микроорганизмов;
- регулирует иммунитет и воздействует на его нарушенные звенья;
- контролирует энергетический и липидный обмен;
- участвует в развитии и функционировании мозга.
Микрофлора или микробиота — это экосистема, в которой преобладают бактерии, в основном строгие анаэробы, которым для жизни не нужен кислород. В ней есть и другие микроорганизмы: вирусы и бактериофаги, простейшие, археи (одноклеточные живые организмы) и грибы. Всего в микробиоте свыше семи тысяч штаммов.
Дисбактериоз, или дисбиоз — это синдром, при котором нарушается соотношение между представителями микрофлоры. Он не является болезнью, но лежит в основе множества заболеваний — кишечных, общевоспалительных, аутоиммунных и нейропсихических.
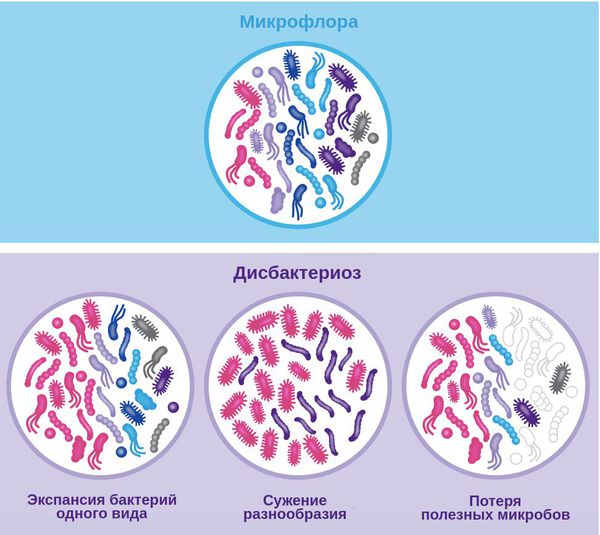
Микрофлора и типы дисбактериоза
Нарушение состава микрофлоры также может влиять на поведение человека и скорость старения: при сужении микробного разнообразия оно происходит быстрее в сравнении с темпами здорового старения.
Соотношение различных видов микроорганизмов нарушается по многим причинам:
- Диета и режим питания — пища с высоким содержанием животных жиров, сахара и крахмала, ограничением клетчатки и избытком животных белков.
- Продукты с пищевыми добавками — бисульфитом и сульфитом натрия, наночастицами металлов и антибиотиками.
- Избыточная гигиена — нарушение водно-жировой мантии кожи из-за использования бактерицидных средств для умывания (особенно с салицилатами).
- Гормональный дисбаланс. При избытке андрогена у женщин состав микробиоты нарушается, а при низком альфа- и бета-разнообразии сообществ бактерий в кишечнике повышается риск развития синдрома поликистозных яичников.
- Употребление алкоголя — уменьшается количество лактобактерий и появляются микроорганизмы, которые могут повредить слизистую. Например, Neisseria из этанола синтезирует такое ядовитое вещество, как ацетальдегид.
- Первичный и вторичный иммунодефицит. Из-за нарушения звеньев иммунитета растёт число микроорганизмов и формируется новая микрофлора, которая меняет иммунный ответ, образуя порочный круг.
- Травма и острое воспаление. В ответ на нарушение целостности тканей организма иммунитет экстренно активируется и нарушает соотношение бактерий.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы дисбактериоза
Когда защитная функция слизистой оболочки кишечника нарушается, иммунная система перестаёт адекватно реагировать на кишечную микрофлору. В связи с этим возникают разнообразные симптомы:
- При нарушении дисбактериозе кишечника могут беспокоить запоры, диарея или их сочетание, вздутие, урчание в животе, отрыжка, чувство тяжести после еды, повышенная чувствительность к определённой пище (особенно злаковой и молочной), боли и дискомфорт.
- При нарушении кожной микрофлоры появляются разнообразные сыпи, шелушение, покраснение, зуд, сухость или жирность кожи.
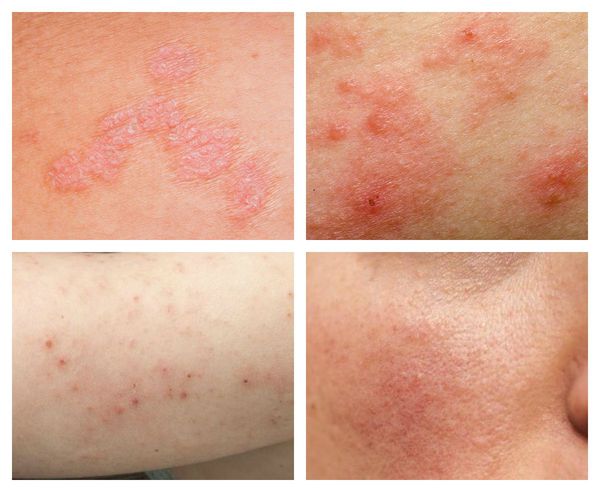
Виды поражения кожи, связанные с дисбиозом
- При генитальном дисбактериозе типичным признаком является кандидоз (молочница). Иногда могут возникать нетипичные выделения и дискомфорт вплоть до болезненности.
- При дисбактериозе полости рта развиваются стоматит, пародонтоз и кариес, появляется неприятный привкус и запах изо рта, постоянный налёт на языке.
Когда под влиянием дисбиоза начинают развиваться различные болезни, появляются другие симптомы:
- При нейропсихических заболеваниях появляется усталость, апатия, тревога, снижается настроение, ухудшается концентрации внимания, возникают навязчивые мысли, усиленная реакция на стресс, судороги.
- При инсулинорезистентности происходит набор веса, повышение сахаров и липидов в крови, возникает тяжесть в правом боку.
- При системном воспалении и аутоиммунитете до полноценного развития болезни и постановки диагноза появляются отдельные проявления в виде болей в суставах, кожных высыпаний, неадекватных сосудистых реакций, примесей слизи или крови в кале, неинфекционного подъёма температуры тела, озноба, общей слабости.
- При аллергии появляется диарея после употребления аллергенных продуктов (особенно молочных, злаковых, цитрусовых, красных фруктов и овощей, ягод, шоколада, орехов) и зудящий дерматит.
Патогенез дисбактериоза
Колонизация кишечника бактериями начинается при прохождении младенца через родовой канал. В этот момент он получает микробиоту своей матери — лактобациллы, Prevotella и другие. При кесаревом сечении микробный состав изменяется. Он напоминает кожу матери: появляются стафилоккоки, коринебактерии и пропионобактерии.
Во время грудного вскармливания увеличивается количество бифидобактерий. Они необходимы для использования олигосахаридов материнского молока. При недостаточном питании формирование этих бактерий нарушается, что приводит к стойкой незрелости микробиоты и риску развития дисбактериоза.
В зависимости от типа дисбиоза и особенностей организма могут включаться различные патологические пути.
Путь «Дисбактериоз — кишечник — мозг»
Микробиота кишечника влияет не только на физическое, но и на психологическое состояние человека. Её связь с мозгом осуществляется через блуждающий нерв (вагус) и ключевые центральные медиаторы:
- бифидобактерии infantis влияют на центральную передачу серотонина;
- лактобациллы и бифидобактерии продуцируют гамма-аминомаслянную кислоту (ГАМК);
- кишечные палочки, Bacillus и Saccharomyces spp. могут производить норадреналин;
- кандида, стрептококки, кишечные палочки и энтерококки синтезируют серотонин;
- Bacillus может продуцировать дофамин;
- лактобациллы способны производить ацетилхолин.
Ось гипоталамус-гипофиз-надпочечник регулирует реакции на стресс и может значительно влиять на ось микробиом-кишечник-мозг.
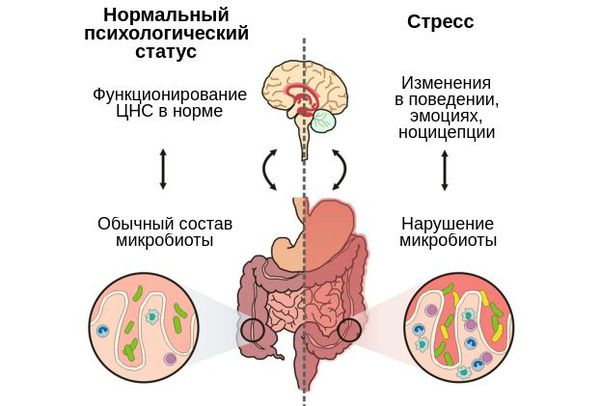
Влияние дисбиоза на нервную систему
Путь «Микробиота — воспаление — инсулинорезистентность»
Полезные бактерии вырабатывают короткоцепочечные жирные кислоты, которые усиливают связи между клетками кишечника, препятствуя попаданию токсичных соединений в кровоток. Когда численность нормальной флоры снижается, изменяется состав кишечной слизи — муцина. В связи с этим защитный барьер слабеет, развивается так называемый “синдром дырявого кишечника” — токсины из пищеварительной системы попадают в кровоток, запуская системное воспаление.
Организм разделяет флору на “свой-чужой” при помощи толл-рецепторов. Когда к рецептору присоединяется патоген, происходит передача информации об опасности внутрь клетки, где через каскад реакций запускается иммунный ответ, направленный на борьбу с возбудителем. Высвобождаются секреторный IgA, антимикробные пептиды и хемокины. Это ведёт к активации макрофагов, которые начинают выделять интерлейкин-1b и фактор некроза опухоли альфа. Эти вещества блокируют путь инсулина внутрь клетки. В результате развивается инсулинорезистентность. Без своего проводника глюкоза накапливается в крови,что приводит к диабету II типа.
Путь «Дисбактериоз — ожирение — печень»
О количестве съеденного организм узнаёт по уровню всё тех же короткоцепочечных жирных кислот, вырабатываемых флорой. При низком потреблении клетчатки — овощей и отрубей — этих жирных кислот вырабатывается мало. В ответ на это кишечник замедляет эвакуацию, чтобы запасти побольше энергии. В итоге запускается адипогенез — отложение жира.
Ещё одним веществом, которое обеспечивает передачу сигналов о чувстве сытости из кишечника в гипоталамус, является гуанилилциклаза C. При дисбиозе эта передача ослабляется, что ведёт к перееданию и набору веса.
При синдроме избыточного бактериального роста запускается процесс местного воспаления, повышается проницаемость кишечной стенки. Это ведёт к попаданию токсинов в кровь и общей воспалительной реакции, в результате которой поражается различный органы, в том числе и печень. При развитии инсулинорезистентности запускается глюкокиназный путь поступления глюкозы в клетки печени, из-за чего в органе накапливаются жировые включения. В дальнейшем развивается неалкогольная жировая болезнь печени.
Путь «Дисбактериоз — аутоиммунитет»
Изменённая композиция микробиоты воздействует на кишечную иммунную систему. Иммунитет, активированный дисбактериозом кишечника, запускает каскад воспалительных реакций, что приводит к поражению суставов, кожи, почек, кишечника и т. д. Если реакция защитных сил чрезмерна, развиваются аутоиммунные заболевания.
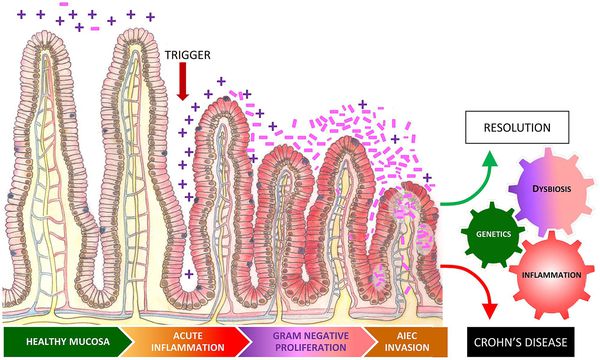
Воспаление стенки кишечника при дисбактериозе
Хронический воспалительный ответ, который вызывает дисбиоз, также может поспособствовать развитию ревматических заболеваний.
Путь «Дисбактериоз — аллергия»
Полезные бактерии поддерживают баланс иммунного ответа в организме.
Они стимулируют подавление IgE и лимфоцитов Th1 и Th2, которые сдерживают паразитарную инфекцию. Если популяция полезных микроорганизмов не развивается, это может привести к аллергическим ответам.
Полезная микрофлора формируется во младенчестве и сохраняется на всю жизнь вместе с особенностями иммунных ответов. Помешать появлению адекватного альфа-разнообразия микробиомов в этот период, помимо рождения через кесарево сечение, могут такие факторы, как:
- раннее воздействие антибиотиков;
- отсутствие домашних животных;
- постоянная обработка дома обеззараживающими средствами.
В итоге, если слишком тщательно оберегать ребёнка от столкновения с инфекциями, у него резко повышается риск развития аллергических заболеваний.
Классификация и стадии развития дисбактериоза
Из-за разнообразия агентов микрофлоры и проявлений дисбиоза, классификация нарушения микрофлоры весьма условна.
Традиционно выделяют три степени дисбиоза:
- I степень — снижение нормофлоры;
- II степень — развитие условно-патогенной флоры;
- III степень — присоединение патогенной флоры.
Кроме изменений микрофлоры важно знать, в микробиоме какого органа произошло нарушение. В связи с этим различают кишечный и внекишечный дисбактериоз. К внекишечным формам относятся:
- дисбиоз ротовой полости;
- дисбиоз кожи;
- дисбиоз половых органов;
- дисбиоз мочевыводящих путей;
- дисбиоз дыхательной системы.
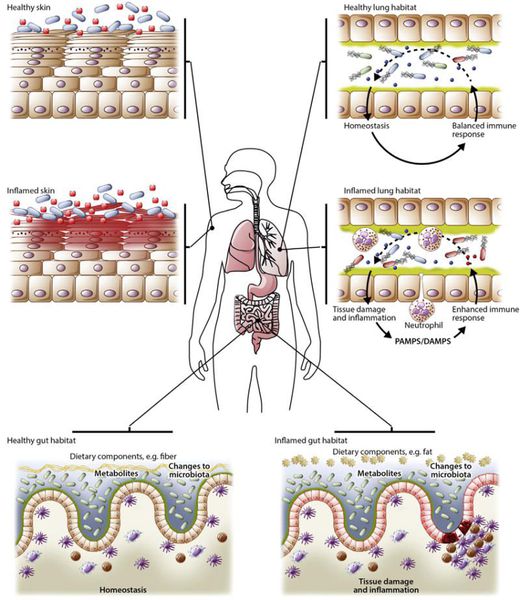
Формы дисбактериоза
По течению дисбактериоз кишечника условно подразделяют на три стадии:
- латентный дисбиоз — без проявлений, выявляется только по результатам анализов;
- дисбиоз с кишечной симптоматикой — возникает нарушение стула, боли в животе;
- стадия развития осложнений — инсулинорезистентности, нейровегетативных нарушений, хронического колита, дерматита и вагинита.
В зависимости от того, в каком отделе кишечника возникло нарушение, выделяют:
- дисбактериоз тонкого кишечника — диарея водянистая, вздутие живота появляется сразу после еды;
- дисбактериоз толстого кишечника — кал кашицеобразный, вздутие возникает к вечеру.
Осложнения дисбактериоза
Симптомы дисбактериоза кишечника с трудом можно отличить от симптомов его осложнений. Всё потому, что дисбиоз — синдром, который вносит существенный вклад в развитие многих болезней.
Осложнения можно разделить на несколько групп:
- нейропсихические болезни: депрессия, болезнь Альцгеймера, рассеянный склероз, тревожное расстройство, шизофрения, аутистические расстройства, болезнь Паркинсона;
- болезни, связанные с невосприимчивостью к инсулину: инсулинорезистентность, дислипидемия, ожирение, сахарный диабета II типа, гипертония, неалкогольная жировая болезнь печени;
- аутоиммунные патологии: сахарный диабет I типа, ревматоидный артрит, системная красная волчанка, первичный склерозирующий холагнит;
- аллергические заболевания — бронхиальная астма, атопический дерматит, пищевая аллергия;
- системные воспаления — болезнь крона, язвенный колит, синдром раздражённого кишечника, целиакия и колоректальный рак.
Нейропсихические болезни
Депрессия и тревожное расстройство коррелируют с преобладанием Firmicutes над Bacteroides.
Рассеянный склероз связан с значительным сокращением видов Clostridia XIVa и IV, увеличением содержания Methanobrevibacter и Akkermansia и уменьшением числа Butyricimonas.
На мышиной модели болезни Альцгеймера в амилоидных бляшках накапливается микробиота.
Связь шизофрении, аутистических расстройств и болезни Паркинсона с дисбиозом доказана. Но о том, являются ли эта связь основной или сопутствующей, до сих пор ведутся споры.
Аутоиммунные патологии
Сахарный диабет I типа связан с положительной корреляцией между аутоантителами и микрофлорой — островковыми клеткам, Bacteriodes и Bilophila. Также обнаружена отрицательная связь со Streptococcus и Ruminococcaceae. Кроме того, распространение Faecalibacterium приводит к снижению уровня гликированного гемоглобина.
Ревматоидный артрит усиливается из-за молекулярной мимикрии — бактерии Prevotella copri, Parabacteroides sp. и Butyricimonas воспроизводят структуру двух аутоантигенов организма. В результате антигенов в воспалённой синовиальной ткани становится намного больше. И чем больше антител GNS, тем выраженнее симптомы артрита(8). Снизить боль, отёчность и улучшить показатели крови во время различных фаз артрита можно с помощью пробиотиков.
Системная красная волчанка сопровождается снижением видового разнообразия микрофлоры. При это в пять раз увеличивается число бактерии Ruminococcus gnavus. Количество антител к этим бактериям напрямую связано с активностью заболевания.
Первичный склерозирующий холагнит связан с уменьшением разнообразия микрофлоры. После трансплантации фекальной микробиоты альфа-разнообразие увеличивается. Из-за этого щелочная фосфатаза снижается более чем в два раза, что свидетельствует о влиянии микробиоты на аутоиммунные процессы в протоках печени.
Аллергические заболевания
Бронхиальная астма связана с увеличением респираторной микрофлоры — гемофильной палочки, стрептококков, бактерий Moraxella — и снижением кишечного микробиома — бифидобактерий, бактерий Akkermansia, Faecalibacterium, Morganella, Lactobacillus. Ослабить аллергическую реакцию может вдыхание «сельскохозяйственной пыли», которая насыщена бактериями и их компонентами.
Атопический дерматит возникает при колонизации кожи золотистым стафилококком на фоне повышенной чувствительности иммунной системы и нарушения кожного барьера. Суперантигены стафилококков усиливают концентрацию IgE — антител, призванных защищать организм от паразитов. Если антитела отсутствуют, антигены атакуют собственные ткани и вызывают аллергию — активируют воспалительные лимфоциты Th2 / Th22 и способствуют появлению дендритных клеток.
Обратный эффект достигается при эпидермальном стафилококке. Он подавляет выработку CD4 — белых кровяных телец, участвующих в иммунном ответе. Мембранный белок TLR-2, связываясь с нормальной флорой кожи, стимулирует выработку антимикробных пептидов и увеличение плотных контактов, что усиливает кожный барьер.
Аллергия на еду появляется при чрезмерном разнообразии микрофлоры. Избыточное микробное обогащение кишечника у 3-месячных детей увеличивает риск развития гиперчувствительности к пище к годовалому возрасту. При обогащении кишечника микробами в 12 месяцев этого уже не происходит.
Когда количество бактерий Ruminococcaceae и Lachnospiraceae повышается, у детей развивается аллергия на молоко. Если же флора обогащена бактериями Firmicutes, включая Clostridia, то аллергия может разрешиться к школьному возрасту.
Аллергии на арахис или древесные орехи возникает при уменьшенном микробном разнообразии и увеличении числа бактерий Bacteroidetes. Выраженность симптомов аллергии и диарея могут ослабнуть при наличии или пероральном введении 17 штаммов Clostridia.
Системные воспаления
Болезнь Крона и язвенный колит возникают из-за чрезмерно агрессивного иммунного ответа на полезную кишечную флору у генетически восприимчивых людей. Разложение флорой белков, пептидов и аминокислот в дистальной части толстой кишки приводит к образованию различных биологически активных метаболитов, которые могут влиять на жизнеспособность клеток эпителия. Снижение количества видов бактерий, которые вырабатывают бутират, ведёт к чрезмерной активация толл-рецепторов, которая может нарушить иммунитет за счёт изменения в активности работы генов.
Синдром раздражённого кишечника связан с уменьшением количества лактобацилл, бифидобактерий и повышением числа аэробов по сравнению с анаэробами. Это нарушение микрофлоры модифицирует болевые и моторные реакции.
Микробиота в данном случае становится и причиной, и мишенью нарушений моторики кишечника, висцеральной гиперчувствительности и нейроиммунных сигналов. Происходит это из-за нарушения слизистого барьера, активации рецепторов, к которым крепятся бактерии, а также дисфункции оси гипоталамус-гипофиз-надпочечник (ось ГГН).
Как возникает дисфункция оси ГГН? Цитокины и избыток короткоцепочечных жирных кислот повышают уровень кортизола — гормона стресса. Он поступает в гипофиз, гипоталамус, миндалину, гиппокамп и префронтальную кору. Обратный сигнал из мозга приводит к изменению моторики и чувствительности кишечника, нарушается эпителиальный барьер и выработка нейротрансмиттеров в виде повышенной реакции на факторы окружающей среды.
Почему нарушается моторика кишечника? Микробиота модулирует моторную функцию кишечника. Её состав может измениться через толл- и нод-рецепторы. В результате повышается проницаемость кишечной стенки, и метаболиты бактерий получают доступ к подслизистой оболочке. Это изменяет экспрессию генов, которые участвуют в работе гладких мышц и нейротрансмиссии. Нормальная кишечная палочка усиливает сокращение толстой кишки, а патогенные штаммы E. coli нарушают сократимость мышечных клеток и угнетают моторику. Воздействие Lactobacillus rhamnosus значительно ухудшает ацетилхолин-стимулируемое сокращение.
Целиакия — уникальное аутоиммунное заболевание. Его причиной являются генетические факторы DQ2 / DQ8 и триггер среды — глютен, но их недостаточно для развития болезни. Пусковой механизм целиакии — нарушение микробиоты у предрасположенных детей в момент введения прикорма — высокие пропорции Firmicutes, Proteobacteria, Corynebacterium, Gemella, Clostridium, Enterobacteriaceae и Raoultella и более низкие Actinobacteria, Bifidobacterium.
Так как непереносимость глютена во взрослой жизни после многих лет употребления злаков встречается всё чаще, дополнительным фактором формирования целиакии становится воздействие окружающей среды.
Колоректальный рак — рак прямой кишки — также связан с нарушением микрофлоры. Запущенный дисбактериоз запускает хроническое воспаление. Из-за этого накапливаются продуцируемые хозяином антибактериальные пептиды, секреторные IgA, муцины, цитокины или нейромедиаторы. Также в организме скапливаются остатки повреждённых клеток и много активных форм кислорода и азота. При ошибках копирования во время деления кишечных клеток (дисплазии) эти вещества способствуют злокачественному перерождению.
Развитие рака происходит по модели «водитель — пассажир»:
- «водители» — определённые штаммы бактерий — нарушают микросреду слизистой оболочки, повреждая ДНК;
- «пассажиры» — патологическая флора — после повреждения оболочки колонизируют её, что приводит к хроническому воспалению, прямому повреждению тканей и зарождению опухоли.
Другие осложнения дисбактериоза
Повышается риск заражения венерическими заболеваниями, в том числе ВИЧ-инфекцией. У девушек этому способствует дефицит бактерий Lactobacillus, которые продуцируют молочную кислоту и пероксид водорода для защиты от патогенных микроорганизмов. У мужчин риск приобретения ВИЧ-инфекции повышается при высокой концентрации анаэробных бактерий в микробиоте под крайней плотью.
Угроза преждевременных родов. У женщин до 24 недели беременности маркером такого риска могут служить более низкие вагинальные уровни Lactobacillus crispatus и более высокие уровни BVAB1, Sneathia amnii, TM7-H1, Prevotella и девять дополнительных таксонов.
Риск развития сердечно-сосудистых заболеваний. ДНК бактерий пародонта была обнаружена в атеросклеротических бляшках у пациентов, страдающих ишемической болезнью сердца и атеросклерозом. Бактерии могут инициировать или усугублять атеросклеротические процессы. При этом активируется врождённый иммунитет, напрямую вовлекаются медиаторы, которые активируются антигенами зубного налёта.
Риск развития рака пищевода — аденокарциномы и плоскоклеточного рака. Этот риск связан с составом микробиома полости рта. Пародонтальные патогены Tannerella forsythia и Porphyromonas gingivalis коррелируют с повышенным риском аденокарциномы. Более низкий риск этой болезни наблюдался в связи с истощением полезного рода Neisseria и Streptococcus pneumoniae. Также есть взаимосвязь бактериального биосинтеза каротиноидов с защитой от развития аденокарциномы.
Диагностика дисбактериоза
Диагностика дисбактериоза проводится:
- для лабораторной оценки состояния больного в момент обращения;
- для научно-исследовательской работы, чтобы понять механизмы возникновения заболеваний и разработать методы их лечения, направленные на блокирование механизмов развития патологий.
Исследователи чаще используют генотипирование микробиоты методами ПЦР Real-time (в режиме реального времени), исследуя 16S pРНК бактерий. В клинической практике врач проводит посевы микрофлоры, реже ПЦР и микроскопию.
Молекулярная идентификация — это определение последовательностей ДНК или РНК представителей микрофлоры. Проводится не для всех видов бактерий и вирусов, но их число становится всё больше. Бывают одноцелевые (видовые) и мультиплексные (таксонные) анализы.
Для увеличения количества копий ДНК и улучшения качества идентификации используют амплификацию — многократный повтор исследования. Она позволяет обнаружить даже незначительное количество микроорганизмов.
Существует несколько вариантов амплификации:
- целевая амплификация — к ней относятся ПЦР и обратная транскриптаза-ПЦР;
- амплификация транскрипции и смещения цепи;
- аплификация сигнала — гибридный захват и анализ разветвлённой ДНК;
- ПЦР Real-time — анализ микроматрицы и кривой ликвидуса.
Чаще всего разнообразие микрофлоры изучается с помощью метода ПЦР. Ген 16S рРНК является идеальной мишенью для классификации бактерий из-за его девяти областей, которые помогают различить виды с помощью отдельных нуклеотидных полиморфизмов.
Методы биоинформатики — QIIME, Mothur и Genboree — были разработаны для обработки таксономической информации, полученной из исследований 16S. Эти инструменты упрощают процесс фильтрации качества, выбора таксономических единиц работы, удаления химерной последовательности и назначения таксономии. Они также могут выполнять базовый анализ микрофлоры, включая измерение альфа-разнообразия (в пределах сообщества) и бета-разнообразия (между сообществами). При этом необходимо учитывать вклад вирусов и грибов в микробиомные взаимодействия.
Посевы (тест-культура) — исследования, которые выявляют рост микробов на питательной твёрдой или жидкой среде для дальнейшей идентификации и определения чувствительности к антибиотикам. Они особенно важны в клинической практике, так как позволяют подобрать лечение при обнаружении инфекции на фоне дисбактериоза.
бактерии Proteus mirabilis на питательной среде
Хотя большинство образцов материала высевают на среду общего назначения (например, кровяной или шоколадный агар), некоторые болезнетворные микроорганизмы требуют определённых питательных веществ, ингибиторов или других специальных условий. Если есть подозрение на наличие особых микроорганизмов, если пациент принимал антибактериальные препараты, а также при некоторых особых случаях (например, при наличии ВИЧ-инфекци), нужно об этом сообщить в лабораторию.
Микроскопия охватывает не все микроорганизмы, зато проста и помогает в предварительном выборе антибиотиков при подозрении на инфекцию, пока ожидаются результаты окончательной идентификации.
Научные открытия в области диагностики
Благодаря комплексным исследованиям микробных сообществ MetaHit и Human Microbiome Project стал известен состав и молекулярный профиль здорового кишечного микробиома. Это знание позволило более точно анализировать последовательности ДНК хозяина, микробной ДНК (генома) и РНК (транскриптома).
Недавние достижения в технологиях молекулярной биологии — омикс-технологиях — позволили контролировать концентрации различных биологических молекул. Благодаря этому теперь можно определить их вариации микроорганизмов в различных биологических состояниях в масштабе генома.
Несколько популярных «омических» платформ включают:
- транскриптомику, которая измеряет уровни транскриптов мРНК;
- протеомику, которая количественно определяет содержание белка;
- метаболомику, которая определяет содержание мелких клеточных метаболитов;
- интерактомику, которая разрешает весь набор молекулярных взаимодействий в клетках;
- флюксомику, которая устанавливает динамические изменения молекул внутри клетки с течением времени.
Лечение дисбактериоза
Диета
Рацион питания оказывает сильнейшее влияние на микробиоту кишечника. Достичь здорового статуса микрофлоры можно при низком потреблении животных жиров и простых углеводов, включении в рацион овощей и пищи с высоким содержанием клетчатки, а также при разнообразии потребляемых продуктов.
Диета при нарушении микробиома должна быть максимально полной: чем шире рацион, тем богаче микробное разнообразие. При наличии симптомов метеоризма и неустойчивого стула следует избегать сырых овощей (лучше есть их в виде рагу) и фруктов натощак.
Если есть пищевые непереносимости, приводящие к дисбиозу, то придётся исключить:
- молочные продукты при лактазной недостаточности;
- глютен — при целиакии;
- продукты, на которые есть подтверждённая кишечная аллергия.
Кишечник и флора не любят зажаристую мясную корочку, поэтому тушение продуктов всегда лучше, чем жарка.
Пробиотики
Однозначного мнения о пользе приёма пробиотиков для лечения дисбактериоза пока нет. В исследованиях отмечалось такие положительные эффекты:
- улучшение по шкале Бека при депрессии;
- уменьшение висцеральной чувствительности и нормализация моторики кишечника при синдроме раздражения кишечника и инфекционном энтероколите;
- снижение активности аутоиммунитета при воспалительных заболеваниях кишечника, системной красной волчанки и ревматоидном артрите.
О снижении инсулинорезистентности данные неоднородны.
В западных странах терапия пробиотиками является дополнением к патогенетическому лечению — блокировки механизмов развития болезни. Решение о её назначении остаётся за врачом.
В России лакто-бифидопробиотики в дозах от 10 бактерий в капсуле рекомендованы при болезнях кишечника и как дополнительная терапия аутоиммунных и аллергических заболеваний. Тем не менее, остаётся вопрос длительности применения пробиотиков, так как изолированные заселяемые бактерии (в отличие от фекалотрансплантации) не приживаются, но помогают вытеснить патобионтов и дают возможность угнетённой нормофлоре самостоятельно восстановиться.
Важно, что для лечения различных патологий нужны различные штаммы бактерий:
- при болезни Крона и аллергии эффективен и безопасен Lactococcus lactis, экспрессирующий IL-10;
- при диабете добавление пробиотиков в течение восьми недель предотвращает повышение FPG, снижает уровень hs-CRP в сыворотке и увеличивает общий GSH в плазме;
- при диабете у беременных приём пробиотических добавок в течение 12 недель в первой половине беременности благотворно влияют на маркеры метаболизма инсулина, триглицериды, биомаркеры воспаления и окислительный стресс;
- при запоре добавки с некоторыми пробиотическими штаммами Lactobacillus или Bifidobacterium увеличивают частоту стула и снижают время транзита содержимого кишечника;
- при диарее живые пробиотики высокой концентрации (10 КОЕ/мл) замедляют сокращение мышц толстой кишки;
- при ревматоидном артрите приём добавок пробиотика в течение 8 недель снижает активность заболевания, уровень инсулина и его выделение;
- при атопическом дерматите и пищевой аллергии пробиотики улучшают их течение.
Пребиотики
Эти питательные вещества выступают в качестве «удобрений» для полезных видов бактерий кишечника. К пребиотикам относятся неперевариваемые олигосахариды, инулин, масляная кислота, многоатомные спирты, аминокислоты и пептиды, лактулоза и пищевые волокна.
Применение БАДов с пребиотическим эффектом, таких как «Максилак», «Лактофильтрум», «Закофальк», «Эубикор» и других, обоснованно и является перспективным методом лечения. Например, при выраженной тревожности у пациентов с синдромом раздражённого кишечника ежедневный приём пребиотической смеси галактоолигосахаридов в течение четырёх недель снижает чувство тревоги и положительно влияет на качество жизни.
Метабиотики (постбиотики)
Они являются структурными компонентами пробиотиков и их метаболитов. Препараты этой группы недостаточно изучены, хотя различные продукты распада бактерий содержатся в кисломолочных и квашеных продуктах питания. В аптеке можно встретить такие метабиотики, как «Хилак форте» и «Бактистатин», однако их эффективность не доказана ни в одном крупном исследовании. Поэтому лечение метабиотиками остаётся пока только на уровне концепции.
Антибиотики
При воспалительных заболеваниях кишечника и тяжёлых формах дисбактериоза лечение состоит в том, чтобы устранить микрофлору, которая активировала иммунный ответ, может приём метронидазола и ципрофлоксацина, тогда как пробиотики и пребиотики предотвращают рецидив колита.
При колоректальном раке рост Fusobacterium nucleatum (палочки Плаута) предсказывает агрессивность течения болезни, её устойчивость к химиотерапии и вероятность рецидива. В связи с этим химиотерапию рекомендуется проводить вместе с приёмом антибиотиков, направленных на борьбу с патогенными бактериями.
Улучшить течение ревматоидного артрита может подавление роста бактерией Prevotella copri, так как именно этот патобионт участвует в развитии заболевания.
При синдроме раздражённого кишечника для уменьшения симптомов, в т. ч. вздутия, показано использование местных неабсорбируемых антисептиков неомицина и рифаксимина.
Фекалотрансплантация
В отличие от приёма пробиотиков пересадка кала имеет долгосрочный устойчивый эффект. Сейчас она активно применяется только для лечения от псевдомембранозного колита, вызванного бактериями C. Difficile. Также проводятся множественные исследования об эффекте фекалотрансплантации в лечении аутоиммунных, неврологических заболеваний и инсулинорезистентости.
Бактериофаги
Бактериофаги (вирусы, избирательно поражающие бактериальные клетки) эффективны для борьбы с инфекцией — дисбактериозом 2 степени. Препарат подбирают по результатам посевов кала с чувствительностью к фагам. Однако этот метод применяется крайне редко из-за высокой стоимости препаратов и сложности их использования. Выпивать «бульон» с фагами нужно за час до еды 3 раза в день, предварительно выпивая большое количество воды, чтобы разбавить желудочную кислоту, в которой бактериофаги разрушаются. Сейчас этот метод лечения чаще используют в педиатрии, когда нет возможности дать антибиотик.
Иммуномодуляторы
Использование иммуномодуляторов для лечения дисбактериоза кишечника обсуждается, однако убедительных данных пока нет. Хорошо зарекомендовали себя только витамин Д и Омега-3, дефицит которых однозначно негативно сказывается на взаимодействии кишечной стенки с микробиомом.
Могут ли помочь народные средства
Суть народности метода в его популярности среди людей без наличия доказательной базы. Когда какой-то метод лечения проходит клинические испытания, он становится лекарством традиционной практики. Из фитотерапии положительно воздействуют на слизистую пищеварительного тракта и флору настои календулы, ромашки, шалфея и солодки.
Прогноз. Профилактика
Прогноз при дисбактериозе благоприятный. Восстановление нормальной флоры — процесс не быстрый, но достижимый.
Начинать профилактику дисбактериоза у детей необходимо с нормализации вагинальной и кишечной микрофлоры будущих мам. Роды лучше проводить естественным способом.
Следующий шаг на пути правильного формирования микрофлоры кишечного — грудное вскармливание, в ходе которого в организме появляются бифидобактерии. Слишком раннее введение глютенового прикорма поможет избежать возможного развития местного воспаления и целиакии.
Основная микробиота формируется только в первый год жизни. Воздействия на организм после года, в том числе терапевтические, влияют на бактериальные сообщества намного меньше.
В дальнейшей жизни важнейшее значение в профилактике дисбактериоза имеет образ питания, разнообразие рациона и режим приёма пищи. Диета должна быть обогащена кисломолочными продуктами, овощами, фруктами и отрубями. Преобладание растительных масел над животными жирами способствует балансу жирных кислот и противовоспалительной активности в кишечнике.
На фоне погрешности в диете, стресса и после перенесённых инфекций могут появиться первые симптомы кишечного дискомфорта — вздутие, нарушение стула, нарастание висцеральной чувствительности.
Отказ от вредных привычек (курения, злоупотребления алкоголем), минимизация консервантов, потребляемых с пищей, а также амортизация стресса помогут избежать запуска воспалительных процессов и нарушения микрофлоры, связанного с иммунным ответом.
В современном мире инфекции распространяются с огромной скоростью, поэтому отказ от антибиотиков невозможен. Важно применять их разумно, только по назначению врача и с одновременным приёмом пробиотиков.
Регулярное мытьё рук, фруктов и овощей, отказ от косметических средств с антимикробной активностью защищают от инфекций и сохраняют естественную нормофлору.
С возрастом разнообразие микробиоты естественным образом снижается. Это повышает склонность к запорам, ослабляет иммунную защиту и вызывает общую слабость. В таких ситуациях профилактикой дальнейшего развития дисбиоза будет своевременный приём курсов про- и пребиотиков или их постоянное поддерживающее применение.
Список литературы
- Dinan T.G., Cryan J.F. Gut instincts: microbiota as a key regulator of brain development, ageing and neurodegeneration // J Physiol. — 2017; 595 (2): 489-503.ссылка
- Federici E., Prete R., Lazzi C., Pellegrini N., et al. Bacterial composition, genotoxicity, and cytotoxicity of fecal samples from individuals consuming omnivorous or vegetarian diets // Front Microbiol. — 2017; 8: 300.ссылка
- Irwin S.V., Fisher P., Graham E., Malek A., Robidoux A. Sulfites inhibit the growth of four species of beneficial gut bacteria at concentrations regarded as safe for food // PLoS One. — 2017; 12 (10): e0186629.ссылка
- Mancuso C., Barisani D. Food additives can act as triggering factors in celiac disease: Current knowledge based on a critical review of the literature // World J Clin Cases. — 2019; 7 (8): 917-927.ссылка
- Torres P.G., Siakowska M., Banaszewska B., Pawelczyk L., et al. Gut microbial diversity in women with polycystic ovary syndrome correlates with hyperandrogenism // The Journal of Clinical Endocrinology & Metabolism. — 2018; 103 (4): 1502-1511.
- Howard B.M., Kornblith L.Z., Christie S.A., Conroy A.S., et al. Characterizing the gut microbiome in trauma: significant changes in microbial diversity occur early after severe injury // Trauma Surg Acute Care Open. — 2017; 2: 1-6.
- The Integrative HMP (iHMP) Research Network Consortium. The Integrative Human Microbiome Project // Nature — 2019; 641–648.
- Gianchecchi E., Fierabracci A. Recent advances on microbiota involvement in the pathogenesis of autoimmunity // Int J Mol Sci. — 2019; 20 (2): 283.ссылка
- Huang Y.J., Marsland B.J., Bunyavanich S., O’Mahony L., et al. The microbiome in allergic disease: current understanding and future opportunities—2017 PRACTALL document of the American Academy of Allergy, Asthma & Immunology and the European Academy of Allergy and Clinical Immunology // J Allergy Clin Immunol. — 2017; 139 (4): 1099-1110. ссылка
- Liu Y., Alookaran J.J., Rhoads J.M. Probiotics in autoimmune and inflammatory disorders // Nutrients. — 2018; 10 (10). ссылка
- Kennedy P.J., Cryan J.F., Dinan T.J., Clarke G. Irritable bowel syndrome: A microbiome-gut-brain axis disorder? // World J Gastroenterol. — 2014; 20 (39): 14105-14125.ссылка
- Distrutti E., Monaldi L., Ricci P., Fiorucci S. Gut microbiota role in irritable bowel syndrome: New therapeutic strategies // World J Gastroenterol. — 2016; 22 (7): 2219-2241. ссылка
- Bercik P., Denou E., Collins J., Jackson W. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice // Gastroenterology. — 2011; 141 (2): 599-609.ссылка
- Qin J., Li Y., Cai Z., Li S. A metagenome-wide association study of gut microbiota in type 2 diabetes // Nature. — 2012; 490 (7418): 55-60.ссылка
- Klimesova K., Zakostelska Z.J., Tlaskalova-Hogenova H. Oral bacterial and fungal microbiome impacts colorectal carcinogenesis // Front Microbiol. — 2018; 9: 774. ссылка
- Kostovcikova K., Coufal S., Galanova N., Fajstova A., et al. Diet rich in animal protein promotes pro-inflammatory macrophage response and exacerbates colitis in mice // Front Immunol. — 2019; 10: 919. ссылка
- Troutman T.D., Bazan J.F., Pasare C. Toll-like receptors, signaling adapters and regulation of the pro-inflammatory response by PI3K // Cell Cycle. — 2012; 11 (19): 3559-3567. ссылка
- Blomain E.S., Merlino D.J., Pattison A.M., Snook A.E., Waldman S.A. Guanylyl cyclase C hormone axis at the intersection of obesity and colorectal cancer // Mol Pharmacol. — 2016; 90 (3): 199-204. ссылка
- Houghton D., Stewart C.J., Day S.P., Trenell M. Gut microbiota and lifestyle interventions in NAFLD // Int J Mol Sci. — 2016; 17 (4): 447. ссылка
- Azzouz D., Omarbekova A., Heguy A., Schwudke D., et al. Lupus nephritis is linked to disease-activity associated expansions and immunity to a gut commensal // Ann Rheum Dis. — 2019; 78: 947-956.
- Allegretti J.R., Kassam Z., Carrellas M., Timberlake S., et al. P1425 — Fecal microbiota transplantation improves microbiome diversity and liver enzyme profile in primary sclerosing cholangitis // World Congress of Gastroenterology. — 2017.
- Shadnoush M., Nazemian V., Manaheji H., Zaringhalam J. The effect of orally administered probiotics on the behavioral, cellular, and molecular aspects of adjuvant-induced arthritis // Basic Clin Neurosci. — 2018; 9 (5): 325-336. ссылка
- Muir A.B., Benitez A.J., Dods K., Spergel J.M, Fillon S.A. Microbiome and its Impact on Gastrointestinal Atopy // Allergy. — 2016; 71 (9): 1256-1263. ссылка
- Fiocchi A., Burks W., Bahna S.L., Bielory L., et al. Clinical use of probiotics in pediatric allergy (cuppa): A World Allergy Organization Position Paper // World Allergy Organ J. — 2012; 5 (11): 148-167.ссылка
- Hijazi K., Lowe T., Meharg C., Berry S.H., et al. Mucosal microbiome in patients with recurrent aphthous stomatitis // J Dent Res. — 2015; 94 (3): 87S-94S. ссылка
- Fan x., Peters B.A., Jacobs E.J., Gapstur S.M., et al. Drinking alcohol is associated with variation in the human oral microbiome in a large study of American adults // Microbiome. — 2018; 6: 59.
- Peters B.A., Wu J., Pei Z., Yang L., et al. Oral microbiome composition reflects prospective risk for esophageal cancers // Cancer Research. — 2017; 77 (23): 6777-6787.
- Barnard E., Liu J., Yankova E., Cavalcanti S.M. Strains of the Propionibacterium acnes type III lineage are associated with the skin condition progressive macular hypomelanosis // Scientific Reports. — 2016; 6: 31968.
- Prince A.L., Chu D.M., Seferovic M.D., Antony K.M., et al. The perinatal microbiome and pregnancy: moving beyond the vaginal microbiome // Cold Spring Harb Perspect Med. — 2015; 5 (6): a023051.ссылка
- Larsen B., Monif G.R. Understanding the bacterial flora of the female genital tract // Clin Infect Dis. — 2001; 32 (4): e69-77.ссылка
- Pittman J.E., Wylie K.M., Akers K., Storch G.A., et al. Association of antibiotics, airway microbiome, and inflammation in infants with cystic fibrosis // AnnalsATS. — 2017; 14: 1548-1555.
- Olivares M., Neef A., Castillejo G., Palma G.D., et al. The HLA-DQ2 genotype selects for early intestinal microbiota composition in infants at high risk of developing coeliac disease // Gut. — 2015; 64 (3): 406-417. ссылка
- König J., Siebenhaar A., Högenauer C., Arkkila P.,et al. Consensus report: faecal microbiota transfer — clinical applications and procedures // Aliment Pharmacol Ther. — 2017; 45 (2): 222-239. ссылка
- Morgan X.C., Huttenhower C. Meta’omic analytic techniques for studying the intestinal microbiome // Gastroenterology. — 2014; 146 (6): 1437-1448. ссылка
- Asemi Z., Zare Z., Shakeri H., Sabihi S.S., Esmaillzadeh A. Effect of multispecies probiotic supplements on metabolic profiles, hs-CRP, and oxidative stress in patients with type 2 diabetes // Ann Nutr Metab. — 2013; 63 (1-2): 1-9. ссылка
- Gong J., Bai T., Zhang L., Qian W.. et al. Inhibition effect of Bifidobacterium longum, Lactobacillus acidophilus, Streptococcus thermophilus and Enterococcus faecalis and their related products on human colonic smooth muscle in vitro // PLoS One. — 2017; 12 (12): e0189257. ссылка
- Zamani B., Golkar H.R., Farshbaf S., Emadi-Baygi M., et al. Clinical and metabolic response to probiotic supplementation in patients with rheumatoid arthritis: a randomized, double-blind, placebo-controlled trial // Int J Rheum Dis. — 2016; 19 (9): 869-79. ссылка
- Bennet S.M.P., Öhman L., Simrén M. Gut microbiota as potential orchestrators of irritable bowel syndrome // Gut Liver. — 2015; 9 (3): 318-331.ссылка