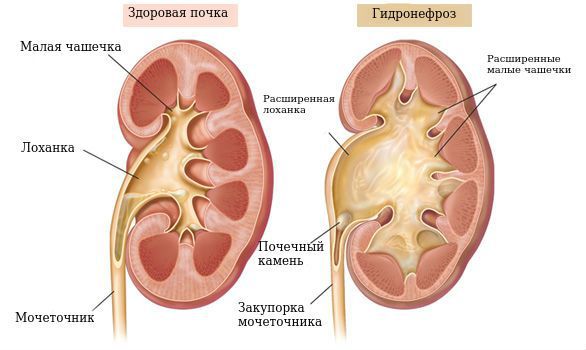
Адреногенитальный синдром (Congenital adrenal hyperplasia) — это группа наследственных заболеваний, при которых в коре надпочечников нарушается выработка стероидных гормонов .
Синонимы: врождённая дисфункция коры надпочечников (ВДКН), гиперплазия коры надпочечников (в англоязычных источниках используется именно этот термин).
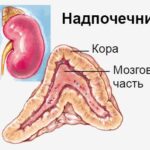
Надпочечники — это парные эндокринные железы, расположенные над почками. В каждом из них выделяют корковое и мозговое вещество. В мозговом слое синтезируется адреналин, в корковом — стероиды, которые поддерживают основные функции организма: саморегуляцию внутренней среды за счёт задержки натрия и адаптацию к стрессовым внешним факторам. Нарушение работы эндокринных желёз может проявляться снижением или увеличением выработки гормонов.
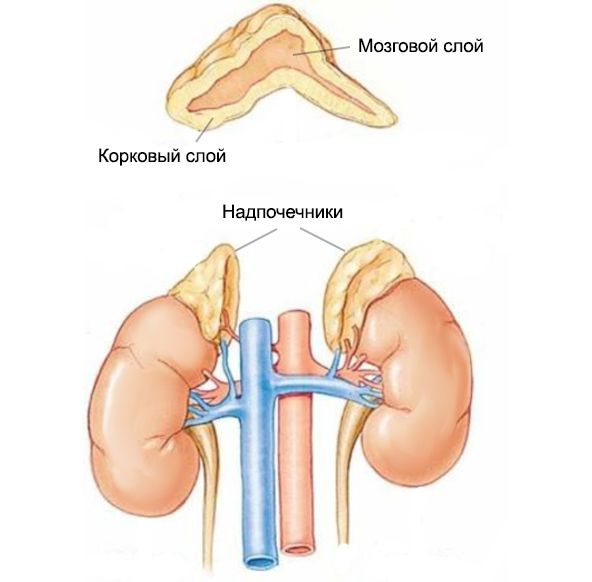
Надпочечники
Дословно адреногенитальный синдром означает «надпочечнико-половой синдром» (лат. «adrenal» — надпочечник, «genital» — половой). В начале XX века так называли опухоли надпочечников, при которых у пациента развивались одновременно мужские и женские половые органы.
Причины адреногенитального синдрома
В середине XX века с развитием биохимии и появлением количественных методов для определения стероидов в крови было установлено, что адреногенитальный синдром возникает из-за дефицита ферментов, участвующих в синтезе стероидных гормонов. Тогда же было сформулировано современное определение синдрома — врождённая дисфункция коры надпочечников (ВДКН) или гиперплазия коры надпочечников .
В 1980-е годы с наступлением эпохи молекулярной генетики была окончательно определена причина болезни — мутация в генах, которые кодируют ферменты, участвующие в образовании стероидных гормонов .
Эти мутации можно разделить на две группы:
- повреждение генов, которые отвечают за выработку фермента 21-гидроксилазы, влияющего на образование стероидов;
- дефекты генов, которые влияют на другие ферменты, связанные с образованием стероидов.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы адреногенитального синдрома
Клиническая картина зависит от вида фермента, синтез которого нарушен, и от степени нарушения его работы: полной или частичной.
Чаще всего встречается дефицит фермента 21-гидроксилазы. При полном нарушении работы фермента развиваются классические формы врождённой дисфункции коры надпочечников (ВДКН): сольтеряющая и вирильная. Для сольтеряющей формы характерен дефицит кортизола и альдостерона при значительном повышении андрогенов. При вирильной — то же самое, за исключением дефицита альдостерона .
Сольтеряющая форма
Классические формы диагностируются с рождения или в раннем детстве — до 3 лет. При сольтеряющей форме ребёнок в первые недели жизни слабый, вялый, часто срыгивает, у него плохо развит сосательный рефлекс и часто возникает жидкий стул. Из-за дефицита альдостерона и, как следствие, неспособности организма задерживать воду ребёнок худеет или плохо набирает вес.
Без лечения развивается острая надпочечниковая недостаточность, которая приводит к выраженному обезвоживанию и потере солей. Обезвоживание проявляется низким артериальным давлением, учащённым сердцебиением, сухостью кожи, уменьшением объёма или полным отсутствием мочи. При несвоевременной диагностике ребёнок может погибнуть.
У новорождённых девочек из-за повышенного уровня андрогенов изменяется строение половых органов: увеличивается клитор, сращиваются половые губы, может сформироваться микропенис при наличии матки и придатков. Не обязательные, но возможные симптомы: ноги короче и массивнее, чем у других девочек, узкий таз, широкие плечи, не растёт грудь и может появиться кадык.
У мальчиков симптомы могут быть не выраженными. Как правило, гениталии обычной формы, но может увеличиться пенис, потемнеть мошонка и раньше возникнуть эрекция. Также раньше ломается голос и начинают расти волосы на теле. Взрослых мужчин беспокоят угревая сыпь и бесплодие .
Вирильная форма
Этот тип заболевания менее опасен для жизни, так как из-за сохранённой секреции альдостерона не развивается обезвоживание. Строение половых органов нарушается так же, как и при сольтеряющей форме. Возникают признаки раннего полового созревания: появляются волосы на лобке, ребёнок растёт быстрее, чем сверстники. Часто диагноз ставят в 2–4 года. Если не начать лечение вовремя, избыток андрогенов приводит к преждевременному закрытию зон роста костей и задержке роста .
Неклассическая форма ВДКН
При частично сохранённой работе фермента развивается неклассическая форма, которая протекает без выраженных симптомов надпочечниковой недостаточности. Строение половых органов соответствует полу. Из-за стёртой клинической картины диагноз чаще ставят в подростковом возрасте или позже. Девушки обычно обращаются к врачу из-за нарушения менструального цикла (например, менструации не начались до 15 лет или цикл увеличен до 30–40 дней). Также их может беспокоить угревая сыпь, облысение, рост жёстких тёмных волос на лице, груди, спине и нижней части живота, бесплодие и невынашивание беременности. У мальчиков возможно преждевременное половое созревание, однако чаще симптомов не бывает вовсе .
Менее распространённая форма заболевания вызвана дефицитом фермента 11β-гидроксилазы. Помимо признаков нехватки кортизола и избытка андрогенов, для неё характерно повышение артериального давления —встречается у 2/3 пациентов и проявляется в раннем детстве (норма для детей 90/50—110/70 мм рт. ст.) .
Патогенез адреногенитального синдрома
Все формы ВДКН развиваются из-за генетических поломок. Мутации генов приводят к нарушению работы ферментов, которые участвуют в образовании стероидов. Более 90 % таких мутаций происходят в гене CYP21, который находится на 6-й хромосоме и кодирует фермент 21-гидроксилазу.
Вариантов поломок генов очень много:
- 75–80 % дефектов — мелкие замены одной последовательности ДНК на другую, происходящие между двумя генами во время деления клеток. Если фермент активен более чем на 5 %, развивается неклассическая форма заболевания.
- 20–25 % — крупные замены и хромосомные перестройки, при которых происходит потеря участка хромосомы. В этом случае фермент активен менее чем на 2 %, что приводит к более тяжёлым формам болезни: сольтеряющей и вирильной .
В норме образование стероидов из холестерина проходит ряд этапов, на каждом из которых работает свой фермент. Так, 21-гидроксилаза превращает прогестерон (промежуточный стероид, который образовался из холестерина) в дезоксикортикостерон (предшественник альдостерона), а 17-гидроксипрогестерон (ещё один промежуточный стероид) в дезоксикортизол (предшественник кортизола). Поэтому при дефиците 21-гидроксилазы блокируется синтез кортизола и альдостерона, которые регулируют артериальное давление, уровень глюкозы, водно-солевой баланс и защищают организм от стресса. Из-за накопления гормонов-предшественников и отсутствия нужных ферментов возникает избыток андрогенов, что приводит к гормональному сбою и нарушениям полового развития .
Работа надпочечников регулируется высшими центрами, расположенными в головном мозге: гипофизом и гипоталамусом. При снижении уровня кортизола в крови сигнал тревоги передаётся сначала в гипоталамус, а затем в гипофиз, где начинает активно вырабатываться адренокортикотропный гормон (АКТГ), который стимулирует надпочечники к образованию кортизола. В результате активной стимуляции разрастаются ткани надпочечников (гиперплазия) .
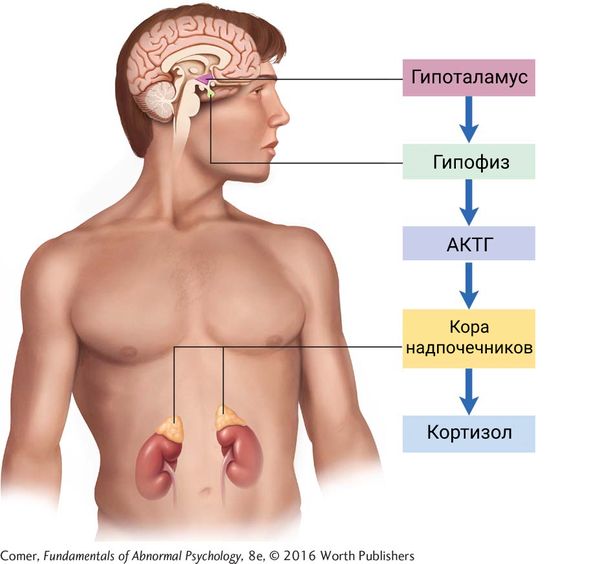
Регуляция работы надпочечников
При мутации в гене CYP11B, расположенном на 8-й хромосоме, нарушается работа фермента 11β-гидроксилазы 1-го типа. Механизм аналогичен дефициту 21-гидроксилазы, но нарушение затрагивают ещё более отдалённый этап в образовании стероидов — превращение дезоксикортикостерона в кортикостерон. Дезоксикортикостерон способен задерживать натрий и воду, поэтому при его накоплении развивается гипертоническая форма синдрома — повышается артериальное давление .
Классификация и стадии развития адреногенитального синдрома
Описано семь форм ВДКН:
- липоидная гиперплазия коры надпочечников (мутация гена, кодирующего белок StAR);
- дефицит 21-гидроксилазы;
- дефицит 11β-гидроксилазы;
- дефицит 20,22-десмолазы;
- дефицит 17α-гидроксилазы / 17,20-лиазы;
- дефицит 3β-гидроксистероиддегидрогеназы;
- дефицит оксидоредуктазы.
В 90 % случаев ВДКН связана с дефицитом 21-гидроксилазы .
В зависимости от клинических проявлений нарушение подразделяют на два вида:
- Классическая форма:
- Вирильная — связана с полным дефицитом 21-гидроксилазы, что приводит к нехватке кортизола и избытку андрогенов. При заболевании ещё с внутриутробного периода нарушается развитие половых органов.
- Сольтеряющая — также связана с полным дефицитом 21-гидроксилазы. Возникает дефицит кортизола и альдостерона, повышается уровень андрогенов. Грубое нарушение гормонального фона проявляется нарушениями полового развития и общими симптомами (например, рвотой и поносом), позже развивается обезвоживание. Если вовремя не начать лечение, ребёнок может погибнуть.
- Неклассическая (поздняя) форма — связана с неполным дефицитом 21-гидроксилазы. Эту форму ещё называют постпубертатной, так как первые признаки синдрома возникают в подростковом возрасте, ярче всего у девочек .
В мире дефицит фермента 21-гидроксилазы выявляют у одного ребёнка на 14 000 новорождённых. В РФ — у одного на 9 500 детей. На втором месте по распространённости находится дефицит 11β-гидроксилазы — 1 % всех случаев ВДКН (гипертоническая форма). В мире такой дефицит выявляют у одного ребёнка на 100 000 новорождённых. В РФ распространённость данной формы заболевания не изучена. Остальные пять форм описаны лишь в единичных клинических случаях .
Осложнения адреногенитального синдрома
Без своевременной диагностики и адекватного лечения могут развиться следующие осложнения:
- острая надпочечниковая недостаточность;
- дисфункция мочевого пузыря (стрессовое недержание мочи, энурез);
- частые инфекции мочевыводящих путей (например, пиелонефрит, уретрит, цистит, простатит);
- нарушение оттока и скопление менструальной крови в матке при закрытии её просвета (гематометра) или в вагине (гематокольпос);
- заброс мочи во влагалище (уринокольпос);
- бесплодие и невынашивание беременности;
- депрессия и расстройства личности .
Диагностика адреногенитального синдрома
В России с 2006 года всем новорождённым проводят скрининг на ВДКН — берут кровь из пятки и определяют в ней уровень17-ОН-прогестерона (17-ОHP) — предшественника стероидных гормонов. При классических формах болезни 17-ОНР значительно повышен: более 300 нмоль/л (100 нг/мл).

Неонатальный скрининг
Для диагностики неклассической формы у девушек исследуют кровь на 17-ОНР:
- если менструации есть, то в 5–7-ой день цикла;
- если менструаций нет совсем и пациентка не беременна, то в любой день.
Диагноз ВДКН подтверждают при 17-ОНР более 30 нмоль/л (10 нг/мл) и исключают при 17-ОНР ниже 6 нмоль/л (2 нг/мл). При дважды полученных пограничных значениях 17-ОНР от 6 до 30 нмоль/л (от 2 до 10 нг/мл) требуется дополнительное исследование гена CYP21A2 .
Предпочтительный метод диагностики в мировой практике — это проба с Синактеном (синтетическим аналогом АКТГ короткого действия). В РФ применяется адаптированный вариант пробы с зарегистрированным препаратом длительного действия — Синактеном-депо. Такая проба проводится только подросткам и людям постарше при значениях 17-ОНР в «серой зоне» (от 6 до 30 нмоль/л), чтобы уточнить наличие или отсутствие неклассической ВДКН.
Протокол пробы:
- Исследование базального уровня 17-ОНР в раннюю фолликулярную фазу цикла, т. е. на 3–5-й день цикла.
- Внутримышечное введение Синактена-депо сразу после забора крови.
- Исследование 17-ОНР и кортизола через 12 и/или 24 часа от момента инъекции.
В норме при стимуляции 17-ОНР не превышает 30 нмоль/л, кортизол — 500 нмоль/л. 17-ОHР более 30 нмоль/л свидетельствует о неклассической форме ВДКН .
Дефицит фермента 11β-гидроксилазы — это диагноз исключения. Если у человека ранее установлена вирильная форма ВДКН, повышено артериальное давление, а при исследовании гена CYP21A2 не выявлены типичные варианты поломок, то необходимо определить уровень 11-дезоксикортизола методом тандемной масс-спектрометрии и исследовать мутации в гене CYP11B1. Такие анализы проводят лишь в специализированных центрах . Самый известный и крупный в России — Эндокринологический научный центр в Москве.
Чтобы оценить состояние репродуктивной системы и своевременно выявить осложнения ВДКН, проводятся инструментальные исследования:
- УЗИ органов малого таза всем женщинам (по показаниям — МРТ малого таза);
- УЗИ органов мошонки всем мужчинам;
- УЗИ/КТ/МРТ надпочечников;
- рентгеноденситометрию поясничного отдела позвоночника и проксимального отдела бедренной кости всем пациентам независимо от степени компенсации адреногенитального синдрома .
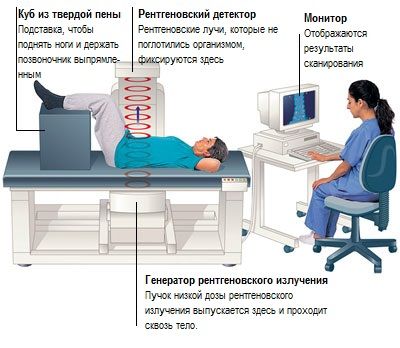
Денситометрия
При наличии показаний УЗИ/КТ/МРТ можно проводить с рождения, рентгенденситометрию назначают с 5 лет.
Если есть документы о диагностированных заболеваниях и других результатах обследований, можно показать их врачу напрямую или открыть доступ к своей электронной медкарте.
Лечение адреногенитального синдрома
Консервативное лечение
При классических формах ВДКН показана пожизненная заместительная гормональная терапия — приём синтетических глюкокортикоидов (ГК).
Препараты, полностью имитирующие собственную секрецию кортизола, пока не разработаны. Для детей предпочтительны ГК короткого действия (Гидрокортизон). У этого препарата короткий период полувыведения — 80–120 минут, что облегчает своевременную корректировку дозы.
Во взрослом возрасте можно применять как короткодействующие, так и длительно действующие препараты: Преднизолон, Дексаметазон и Метилпреднизолон. При сольтеряющей форме совместно с ГК применяют минералокортикоиды (Флудрокортизон). Их назначают для задержки натрия и для того, чтобы сбалансировать обмен веществ в организме и восстановить его саморегуляцию. Дозировку и схему приёма определяет лечащий врач.
При развитии заболеваний, сопровождающихся высокой температурой, а также при гастроэнтерите с обезвоживанием, операциях и травмах рекомендуется увеличить дозы ГК в 2–3 раза, так как при классических формах ВДКН в организме в ответ на стресс не вырабатывается достаточно кортизола. При неэффективности или невозможности приёма таблеток (если ребёнок ещё мал, чтобы принимать лекарства) Гидрокортизон вводят внутримышечно или внутривенно .
Неклассические формы ВДКН у мужчин и женщин, если нет симптомов, лечить не нужно. Исключение составляют мужчины с бесплодием, опухолями надпочечников и опухолями яичек из остаточной надпочечниковой ткани.
Тактика лечения женщин зависит от степени тяжести гиперандрогении и репродуктивных планов. Если женщина не планирует беременность и нет выраженной гиперандрогении, то применять ГК необязательно, их можно заменить на симптоматическую терапию — комбинированные оральные контрацептивы и/или антиандрогены. Они помогают бороться с акне, ростом волос в андрогензависимых зонах, нарушением менструального цикла и предменструальным синдромом.
Назначение ГК допустимо при планировании беременности, особенно при бесплодии, привычном невынашивании беременности и выраженной гиперандрогении. В этих случаях для лечения неклассических форм обычно применяются Гидрокортизон, Преднизолон, Дексаметазон (только вне беременности), Метилпреднизолон.
Гипертоническую форму ВДКН лечат так же, как и вирильную форму. Антигипертензивные препараты назначают при артериальном давлении выше возрастной нормы на 95 перцентилей: для года — выше 102/55 мм рт. ст., для 5 лет — выше 112/70 мм рт. ст., для 10 лет — выше 120/80 мм рт. ст., после 18 лет — выше 140/90 мм рт. ст. Таким пациентам назначают калийсберегающие диуретики (Спиронолактон) и дигидропиридиновые производные селективных блокаторов кальциевых каналов (Нифедипин) .
Хирургическое лечение
Первый этап феминизирующей пластики наружных половых органов (клиторопластика и рассечение урогенитального синуса) рекомендуется проводить в первые годы жизни, чтобы сформировать у девочки правильную половую самоидентификацию и сохранить психологическое здоровье.
Второй этап — интроитопластика (формирование входа во влагалище) проводят в подростковом возрасте после наступления первой менструации . Если провести интроитопластику в раннем детстве, в дальнейшем повышается риск сужения созданного входа во влагалище, что потребует повторного вмешательства (бужирования влагалища).
Другие виды лечения
При беспокойстве из-за роста волос в андрогензависимых зонах рекомендуется провести эпиляцию.
В крайне редких случаях при тяжёлой сольтеряющей форме ВДКН и гиперандрогении, которая плохо поддаётся лечению, может быть рекомендовано удаление надпочечников (адреналэктомия) с последующей постоянной гормонотерапией .
Осложнения при лечении глюкокортикоидами
Отдалённые осложнения, связанные с лечением и передозировкой глюкокортикоидами:
- избыточная масса тела и ожирение;
- дислипидемия;
- гипертония;
- нарушение углеводного обмена, сахарный диабет;
- синдром Иценко — Кушинга;
- утолщение внутренней и средней оболочек сосудистой стенки артерий — прогрессирование атеросклероза;
- повышенный риск сердечно-сосудистых заболеваний;
- нарушение костного метаболизма (уменьшение конечного роста костей, снижение минеральной плотности костной ткани).
Отдалённые осложнения, связанные с лечением и недостаточностью глюкокортикоидов:
- новообразования надпочечников;
- опухоли яичек из остаточной надпочечниковой ткани;
- снижение репродуктивной функции, бесплодие .
Чтобы избежать осложнений, следует строго придерживаться рекомендаций врача по приёму препаратов. Если состояние ухудшилось, необходимо сообщить об этом доктору, и он скорректирует схему лечения.
Прогноз. Профилактика
Прогноз для классических и гипертонической форм зависит от своевременности постановки диагноза, адекватности подобранной терапии, приверженности пациента медикаментозному лечению и результата операции на половых органах у девочек при нарушении формирования пола. Успех операции зависит от опыта хирурга и течения послеоперационного периода.
В целом ВДКН — заболевание, поддающееся лечению. При правильно подобранной терапии и качественном медицинском наблюдении пациенты ведут нормальный образ жизни .
Несвоевременная диагностика сольтеряющей формы ВДКН может привести к гибели ребёнка, но такое случается редко, так как скрининг после рождения позволяет своевременно обнаружить болезнь.
Прогноз для неклассической формы заболевания благоприятный. У 68 % женщин репродуктивная функция сохраняется и беременность наступает самостоятельно без применения ГК. Однако таким пациенткам важно планировать беременность, чтобы определить риск рождения ребёнка с адреногенитальным синдромом .
При наличии в семье детей с ВДКН и подтверждённым носительством мутации у обоих родителей риск рождения больного ребёнка составляет 25 % .
Дородовая диагностика ВДКН у плода включает следующие методы:
- измерение уровня 17-OHP в амниотической жидкости;
- HLA-типирование фетальных клеток;
- молекулярный анализ фетального гена CYP21A2 в амниоцитах или ворсинах хориона;
- неинвазивное пренатальное тестирование материнской плазмы .
Такая диагностика позволит родителям и врачам подготовиться к рождению ребёнка, вовремя подтвердить диагноз и провести лечение.
Список литературы
- Шепелькевич А. П., Лузан А. М., Градуша А. В. Современные подходы к диагностике и лечению наиболее распространённых форм врождённой дисфункции коры надпочечников // Рецепт. — 2020. — Т. 23. — № 2–3. — С. 416–429.
- Карева М. А., Орлова Е. М. Адреногенитальный синдром: прошлое, настоящее и будущее // Проблемы эндокринологии. — 2011. – Т. 57. — № 1. — С. 66–70.
- Мокрышева Н. Г., Мельниченко Г. А., Адамян Л. В. и др. Врождённая дисфункция коры надпочечников (адреногенитальный синдром): клинические рекомендации // Ожирение и метаболизм. — 2021. — Т. 18. — № 3. — С. 345–382.
- Карева М. А., Чугунов И. С. Федеральные клинические рекомендации — протоколы по ведению пациентов с врождённой дисфункцией коры надпочечников в детском возрасте // Проблемы эндокринологии. — 2014. — Т. 60. — № 2. — С. 42–50.
- Гирш Я. В., Курикова Е. А. Врождённая дисфункция коры надпочечников: случай из практики // Вестник СурГУ. Медицина. — 2020. — Т. 44. — № 2. — С. 46–53.
- Молашенко Н. В., Сазонова А. И., Трошина Е. А., Калинченко Н. Ю. Отдалённые последствия длительной глюкокортикоидной терапии у пациентов с врождённой дисфункцией коры надпочечников // Проблемы эндокринологии. — 2010. — Т. 56. — № 5. — С. 15–22.
- Аникиев А. В., Володько Е. А., Бровин Д. Н. и др. Осложнения со стороны мочеполовой системы у девочек с нарушением формирования пола и гипоспадией // Эндокринная хирургия. — 2019. — Т. 13. — № 2. — С. 89–94.
- Шифман Б. М., Дзеранова Л. К., Пигарова Е. А. и др. Поздние осложнения классической формы врождённой дисфункции коры надпочечников и её неадекватного лечения у мужчин (клинический случай с обзором литературы) // Ожирение и метаболизм. — 2019. — Т. 16. — № 4. — С. 90–102.
- Мельниченко Г. А., Трошина Е. А., Молашенко Н. В. и др. Клинические рекомендации Российской ассоциации эндокринологов по диагностике и лечебно-профилактическим мероприятиям при врождённой дисфункции коры надпочечников у пациентов во взрослом возрасте // Consilium Medicum. — 2016. — Т. 18. — № 4. — С. 8–19.
- Raff H., Sharma S. T., Nieman L. K. Physiological basis for the etiology, diagnosis, and treatment of adrenal disorders: Cushing’s syndrome, adrenal insufficiency, and congenital adrenal hyperplasia // Compr Physiol. — 2014. — № 2. — Р. 739–769. ссылка
- Aciеn P., Aciеn M. Disorders of Sex Development: Classification, Review, and Impact on Fertility // J Clin Med. — 2020. — № 11. — Р. 3555.ссылка
- White P. C., Speiser P. W. Congenital adrenal hyperplasia due to 21-hydroxylase deficiency // Endocr Rev. — 2000. — № 3. — P. 245–291.
- Grunwald T. Congenital Adrenal Hyperplasia // KidsHealth. — 2018.