Гипогонадизм (hypogonadism) — это снижение активности гонад: яичков у мужчин и яичников у женщин. При этом состоянии гонады вырабатывают недостаточно половых гормонов (тестостерона у мужчин, эстрогенов и прогестерона у женщин) или организм нечувствителен к этим гормонам .
Самые яркие проявления заболевания — отсутствие менструаций (аменорея) или нарушения менструального цикла у женщин, эректильная дисфункция у мужчин, снижение полового влечения и бесплодие как у мужчин, так и у женщин.
В зависимости от уровня поражения выделяют:
- первичный (гипергонадотропный) гипогонадизм — недостаток половых гормонов из-за первичного поражения гонад;
- вторичный (гипогонадотропный, или центральный) гипогонадизм — дефицит половых гормонов из-за недостаточной стимуляции гонад гормонами гипоталамуса и гипофиза.
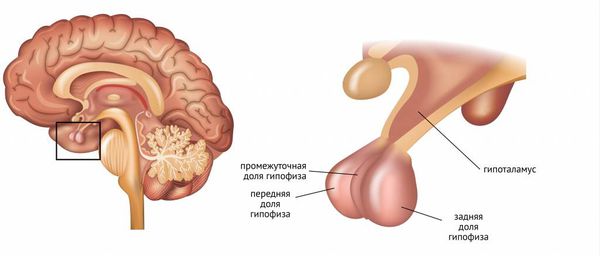
Гипофиз и гипоталамус
Распространённость гипогонадизма
Гипогонадизм одинаково часто встречается у людей всех рас. Первичный гипогонадизм чаще развивается у мужчин. Согласно исследованиям, частота синдрома Клайнфельтера (самой распространённой причины первичного гипогонадизма у мужчин) выше, чем частота синдрома Шерешевского — Тёрнера (самой распространённой причины гипогонадизма у женщин): синдром Клайнфельтера встречается у одного из 300–600 новорождённых мальчиков, а синдром Шерешевского — Тёрнера диагностируют у одной из 2000–5000 новорождённых девочек .
Заболеваемость вторичным гипогонадизмом одинаковая у мужчин и женщин .
Болезнь может возникнуть в любом возрасте, но последствия различаются в зависимости от возраста, в котором началось заболевание:
- Если гипогонадизм возникает пренатально (внутриутробно), то следствием будет нарушение формирования пола, при котором у ребёнка могут быть признаки обоих полов, например мужской кариотип (хромосомный набор клеток) и женские половые органы.
- Если гипогонадизм развивается до полового созревания (пубертата), у девочек не начинаются менструации, не появляются вторичные половые признаки (например, молочные железы), у мальчиков наблюдается крипторхизм, малый размер яичек, микропенис.
- Если болезнь проявляется после полового созревания, то характерны бесплодие и сексуальная дисфункция (снижение либидо, отсутствие эрекций у мужчин).
Что такое женский гипогонадизм
Женский гипогонадизм — это состояние, при котором яичники вырабатывают недостаточно половых гормонов (эстрогена и прогестерона) или вообще не вырабатывают их. В большинстве случаев это проявляется ановуляцией, нарушениями менструального цикла (вторичной аменореей или олигоменореей) и бесплодием. При врождённом гипогонадизме наблюдается задержка полового созревания и отсутствие менструаций (первичная аменорея).
Первичным гипогонадизмом страдает 1–2 % всех женщин мира, вторичным гипогонадизмом — 3–5 %. В структуре эндокринного бесплодия частота этих нарушений составляет 5 и 10 % соответственно, т. е. гипогонадизм — довольно редкая причина бесплодия .
Причины женского гипогонадизма
Причины гипергонадотропного (первичного) гипогонадизма:
1. Врождённых форм:
- Синдром Шерешевского — Тёрнера. Это хромосомное заболевание, при котором одна из Х-хромосом отсутствует или в ней есть дефект. Кариотип при этом синдроме — 45X, а нормальный женский кариотип — 46ХХ. Для этого синдрома характерны недоразвитые яичники.
- Мозаичный кариотип (наличие клеток с разным набором хромосом) — 45X/46XX.
- Мозаичный кариотип с обязательным присутствием Y хромосомы или её участка, чаще всего встречается кариотип 45X/46XY.
- XY-дисгенезия гонад (синдром Свайера). У человека с этим нарушением мужской кариотип, но он выглядит как женщина и имеет все женские внутренние органы, кроме яичников.
- XX-дисгенезия. У человека женский кариотип, он выглядит как женщина, но не имеет яичников.
- Синдром резистентных яичников. Это нечувствительность яичников к гормонам гипофиза: фолликулостимулирующему (ФСГ) и лютеинизирующему (ЛГ), которые в норме воздействуют на яичники и стимулируют рост фолликулов и выход яйцеклетки (овуляцию).
- Избыток галактозы — одного из основных источников энергии организма.
- Синдром нарушения гликозилирования 1-го типа. Это редкая врождённая ошибка углеводного обмена.
- Мутации гена рецептора ФСГ.
- Синдром Нунана. Это генетическая патология, которая характеризуется развитием у больных симптомов, похожих на болезнь Шерешевского — Тёрнера.
2. Приобретённых форм:
- Инфекционные поражения яичников.
- Радиация.
- Преждевременная менопауза, или синдром истощения яичников.
- Травма яичников.
- Операция на яичниках.
- Химиотерапия (алкилирующие и антинеопластические агенты).
- Аутоиммунные заболевания, например аутоиммунный оофорит, при котором собственная иммунная система атакует яичники.
- Приём токсичных веществ.
- Приём препаратов, которые подавляют синтез половых гормонов: блокаторов стероидогенеза, блокаторов ароматазы и т. д.
Причины гипогонадотропного (вторичного) гипогонадизма:
1. Врождённых форм:
- Нарушения секреции гонадотропин-рилизинг-гормона (ГнРГ) — синдром Кальмана в сочетании с аносмией (потерей обоняния) и без неё.
- Изолированное нарушение секреции ФСГ и ЛГ.
- Гипофизарная недостаточность, при которой снижена секреция большинства гормонов гипофиза.
- Мозжечковые атаксии с гипогонадизмом. Это нарушение координации, вызванное патологией мозжечка.
- Синдром Прадера — Вилли, синдром Барде — Бидля и др. При этих синдромах кроме гипогонадизма выявляются и другие нарушения.
2. Приобретённых форм:
- Инфекции и опухоли гипоталамуса, серого бугра и гипофиза, в том числе со сдавлением окружающих структур.
- Гиперпролактинемия (избыток пролактина в крови), в том числе на фоне приёма антипсихотических препаратов.
- Гиперандрогения (избыток андрогенов в крови) на фоне дефицита кортизола при врождённой дисфункции коры надпочечников.
- Лучевая и химиотерапия.
- Аутоиммунные заболевания, например лимфоцитарный гипофизит (воспаление гипофиза).
- Инфекционные заболевания, затрагивающие область гипофиза и гиполатамуса.
- Апоплексия гипофиза (резкое увеличение размера опухоли гипофиза из-за её кровоизлияния);
- Приём лекарственных препаратов: аналогов ГнРГ, половых стероидов, глюкокортикоидов, опиатов и др.
- Тяжёлые хронические заболевания: пороки сердца, заболевания желудочно-кишечного тракта, печени, почек, лёгких и др.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гипогонадизма у женщин
Общие симптомы всех форм гипогонадизма, появившегося до полового созревания:
- нет менархе (первой менструации) в возрасте 16 лет и старше;
- нет признаков полового созревания (молочных желёз, оволосения) в возрасте 14 лет и старше;
- нет первой менструации в течение трёх и более лет после развития вторичных половых признаков;
- биологический возраст не соответствует календарному;
- нет обоняния (аносмия) при синдроме Кальмана .
Проявления гипогонадизма, возникшего после начала полового созревания:
- нарушается менструальный цикл и развивается вторичная аменорея;
- замедляется развитие молочных желёз или они уменьшаются в размере;
- не наступает беременность (бесплодие);
- до 40 лет появляются симптомы климакса: приливы жара, ночная потливость, приступы удушья, озноб, ощущение усиленного сердцебиения, слабость, сонливость, беспричинное беспокойство и раздражительность .
Патогенез гипогонадизма у женщин
Ось гипоталамус-гипофиз-гонады играет решающую роль в формировании пола, половом созревании и фертильности (способности к зачатию).
Гипофиз вырабатывает ФСГ и ЛГ. У женщин ФСГ стимулирует развитие доминантного фолликула в яичнике и созревание в нём яйцеклетки . Также ФСГ помогает развиваться следующему поколению фолликулов, которые будут созревать во время остальных циклов.
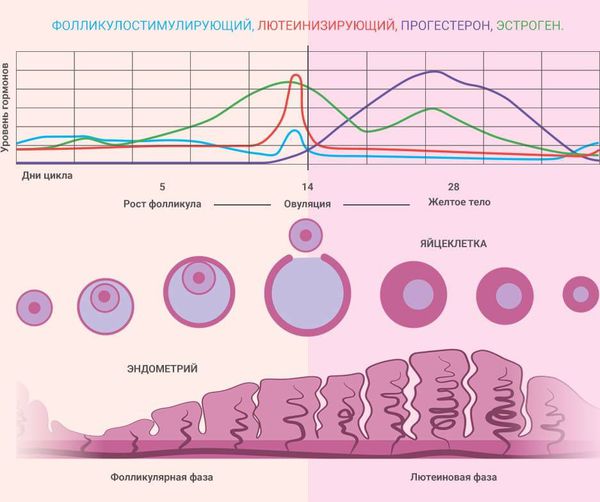
Менструальный цикл. Изменение уровня гормонов
ЛГ — это главный регулятор синтеза половых гормонов яичниками. Он стимулирует производство эстрогенов из их предшественников — андрогенов . Всплеск ЛГ в середине цикла стимулирует созревание яйцеклетки в фолликуле, разрыв доминирующего фолликула и выход яйцеклетки (овуляцию). Благодаря ЛГ стенки фолликула преобразуются в жёлтое тело, которое вырабатывает прогестерон (гормон беременности), андрогены и эстрогены .
Так ФСГ и ЛГ управляют менструальным циклом и синтезом половых стероидных гормонов. Яичники, в свою очередь, тоже регулируют уровень этих гормонов по принципу обратной связи. В лютеиновой фазе яичники вырабатывают больше половых гормонов и за счёт этого снижается выработка ФСГ и ЛГ. Если зачатия не происходит, то уровень эстрогенов и прогестерона снижается и начинается менструация, а уровень ФСГ и ЛГ, наоборот, начинает подниматься.
Гипоталамус регулирует синтез и секрецию ЛГ и ФСГ с помощью ГнРГ, обратной связи со стороны яичников, а также с помощью самого гипофиза за счёт местных факторов (активинов, ингибинов и фоллистатина) .
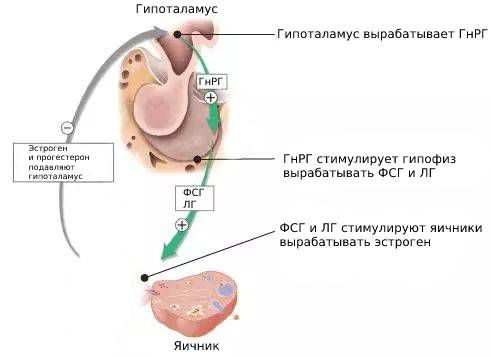
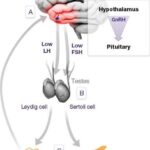
Ось гипоталамус-гипофиз-гонады
Гипергонадотропный (первичный) гипогонадизм вызван первичной недостаточностью яичников. В норме яичники вырабатывают эстрогены, которые подавляют синтез ГнРГ, ЛГ и ФСГ. Но если яичники производят недостаточно эстрогенов, уровень ГнРГ, ЛГ и ФСГ увеличивается.
Такая реакция может быть связана с генетическими причинами, при которых яичники недоразвиты, химио- или лучевой терапией, операциями на яичниках, перенесёнными инфекционными заболеваниями с вовлечением ткани яичников и др.
При гипогонадотропном (вторичном) гипогонадизме гипоталамус не вырабатывает ГнРГ или вырабатывает его недостаточно. Также это состояние возможно, если гипофиз не производит ЛГ и ФСГ или производит недостаточно. Если этих гормонов мало, снижается стимуляция яичников и они вырабатывают меньше эстрогенов.
Если такое нарушение развивается до полового созревания, причиной могут быть аномалии развития центральной нервной системы (ЦНС), нарушения чувствительности рецептора к ГнРГ или нарушения закладки гипоталамо-гипофизарных структур . Известно около 40 генов, нарушения в которых приводят к возникновению вторичного гипогонадизма .
После полового созревания эта форма гипогонадизма возникает из-за патологий гипоталамо-гипофизарной области или воздействий, которые нарушают её функцию: перенесённого энцефалита, посттравматических изменений, радиации (в том числе лучевой терапии по поводу онкозаболеваний), опухолевых процессов, туберкулёза, саркоидоза, некоторых лекарств и др.
Транзиторный (функциональный, или временный) гипогонадизм возникает при чрезмерных физических нагрузках и снижении веса из-за нарушения синтеза нейропептидов, лептина и грелина, влияющих на секрецию ГнРГ .
Временный гипогонадизм также может быть связан с синдромом гиперторможения яичников. Он развивается после длительного приёма эстроген-гестагенных препаратов (КОК), которые тормозят выделение ЛГ и ФСГ в гипофизе.
В итоге, независимо от формы гипогонадизма и его причин, развивается первичное или вторичное бесплодие.
Классификация и стадии развития гипогонадизма у женщин
Классифиакция гипогонадизма:
- Первичный (гипергонадотропный) гипогонадизм: врождённый и приобретённый.
- Вторичный (гипогонадотропный) гипогонадизм: врождённый и приобретённый (включая временный гипогонадизм).
Классификация вторичного гипогонадизма в зависимости от причины и длительности:
- Функциональный (временный) гипогонадизм:
- Конституциональная задержка роста и пубертата (синдром позднего пубертата). Наследственное нарушение, при этом у одного или обоих родителей было позднее половое созревание. Чаще встречается у мальчиков.
- Соматогенная задержка пубертата. Возникает из-за нарушений питания (гипо- или авитаминоза, дефицита белка или минеральных веществ), ожирения, хронических заболеваний (пороков сердца, заболеваний желудочно-кишечного тракта, печени, почек, лёгких и др.) или негативных социальных факторов.
- Перманентный (постоянный) гипогонадизм. В этом случае гипоталамо-гипофизарно-гонадная ось не восстанавливается и требуется пожизненная заместительная гормональная терапия (ЗГТ) .
- Реверсивный (обратимый) гипогонадизм. Через несколько лет лечения гипоталамо-гипофизарно-гонадная ось восстанавливается .
Осложнения гипогонадизма у женщин
Нарушения менструального цикла и аменорея повышают риск развития гиперплазии и рака эндометрия. Гиперплазия эндометрия может приводить к частым обильным кровотечениям и анемии на фоне хронической кровопотери .
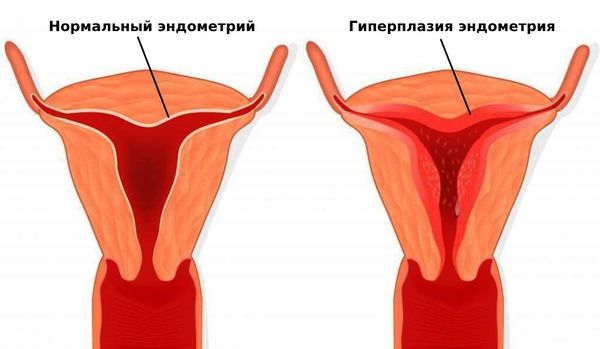
Гиперплазия эндометрия
Из-за недостатка эстрогена у женщин замедляется обмен веществ и, как следствие, возникает дефицит минералов и витаминов, из-за этого повышается риск остеопороза (повышенной хрупкости костей) и переломов. Также могут развиваться урогенитальные осложнения: сухость слизистой влагалища и боль при половом акте . Помимо этого, снижается половое влечение и сексуальная активность.
Гипогонадизм часто сопровождается избыточным весом или ожирением, а это повышает риск возникновения серьёзных патологий:
- предиабета;
- сахарного диабета 2-го типа;
- неалкогольной жировой болезни печени (жирового гепатоза);
- гипертонии;
- сердечно-сосудистых заболеваний: атеросклероза, ишемической болезни сердца, инфаркта миокарда, ишемического инсульта.
Чтобы предотвратить эти осложнения, нужно своевременно обратиться за медицинской помощью к специалисту.
Диагностика гипогонадизма у женщин
Диагностикой и лечением гипогонадизма занимается врач-эндокринолог.
Сбор анамнеза и жалоб
Чтобы изучить историю болезни пациента, врач на приёме может спросить:
- Когда наступило половое созревание у ближайших родственников и есть ли у кого-то из родных гипогонадизм или бесплодие. Позднее половое созревание у одного или обоих родителей позволяет заподозрить конституциональную задержку полового развития, а наличие в семье родственников с гипогонадизмом указывает на генетическую предрасположенность.
- Есть ли задержки психического и умственного развития, врождённые пороки развития, хронические заболевания (сахарный диабет, гипертония и др.), были ли операции в прошлом. Эти состояния характерны для некоторых форм гипогонадизма.
- Есть ли неврологическая симптоматика: сильные головные боли, нарушение зрения и терморегуляции, тошнота, рвота и др. Это может указывать на органические нарушения гипоталамо-гипофизарной области.
- При сборе анамнеза у детей врач может спросить, как изменился рост ребёнка за последние 2–3 года, когда и в какой последовательности появились вторичные половые признаки.
- У взрослых женщин при наличии вторичной аменореи специалист поинтересуется, соблюдает ли пациентка диету при избыточном весе, какие у неё физические нагрузки, принимает ли КОК и как долго.
Осмотр
Данные осмотра будут различаться в зависимости от времени появления, вида и формы гипогонадизма:
- До полового созревания у девочек нет никаких специфических проявлений гипогонадизма.
- В период полового созревания у девочек старше 13 лет не растут молочные железы, вторичные половые признаки не появляются или не соответствуют возрасту либо нет первой менструации в 16 лет и старше (первичная аменорея) .
При гинекологическом исследовании наружные и внутренние половые органы недоразвиты, слизистые оболочки вульвы и влагалища атрофированы.
Низкий вес у пациентки может указывать на функциональный гипогонадизм. При этом вторичные половые признаки будут развиты нормально. При гинекологическом исследовании наблюдается атрофия слизистых вульвы и влагалища.
При синдроме гиперторможения яичников никаких отклонений при общем осмотре не обнаруживается.
Лабораторная диагностика
Анализы крови на ФСГ, ЛГ и эстрадиол позволяют поставить диагноз «гипогонадизм» и определить его вид.
Первичный гипогонадизм устанавливают при повышении уровней ЛГ и ФСГ выше возрастных норм при сниженном значении эстрадиола. Для взрослых женщин критерием служит ФСГ > 30 Ед/л при двукратном определении . У девочек этот критерий зависит от возраста, так как есть физиологические пики секреции ФСГ .
Вторичный гипогонадизм диагностируют при снижении уровней ЛГ и ФСГ ниже возрастных норм при сниженном значении эстрадиола. Для взрослых женщин критерием служит ФСГ < 1,6 Ед/л при двукратном определении . У девочек в любом возрасте — ЛГ < 0,9 Ед/л, ФСГ < 2,5 Ед/л и неопределяемый/низкий уровень эстрадиола .
Анализы крови на тиреотропный гормон (ТТГ), пролактин, адренокортикотропный гормон (АКТГ), инсулиноподобный фактор роста (ИФР-1), кортизол и глюкозу крови помогают отличить гипогонадизм от других причин аменореи и бесплодия и выявить сопутствующие патологии.
Генетическое обследование включает:
- Определение полового хроматина (неактивной X-хромосомы) в мазках с внутренней поверхности щеки. При гипогонадизме половой хроматин не выявляется.
- Определение кариотипа. При гипогонадизме набор хромосом он будет типичен для той или иной формы болезни, например при синдроме Шерешевского — Тёрнера чаще всего пациентки имеют кариотип 45Х.
Это не обязательное исследование, так как оно дорогостоящее и не влияет на тактику лечения. Зато этот анализ позволяет проводить семейное генетическое консультирование пар, которые планируют беременность, что помогает предотвратить рождение детей с наследственными патологиями. Может выполняться у пациенток с симптомами синдрома Шерешевского — Тёрнера, а также у пациенток с нормальным уровнем гонадотропных гормонов, сформированными вторичными половыми признаками, но с первичной аменореей и отсутствием матки по данным УЗИ или МРТ.
Пробы с аналогом ГнРГ, гестагенами, эстрогенами и гестагенами. Эти пробы проводятся, чтобы отличить первичный и вторичный гипогонадизм:
- При пробах с аналогом ГнРГ сначала определяют уровень ФСГ и ЛГ, затем вводят аналог ГнРГ короткого действия, через 1 и 4 часа после введения оценивают, как изменились ФСГ и ЛГ: подъём ЛГ выше 10 мЕд/л позволяет исключить вторичный гипогонадизм.
- На фоне приёма препаратов гестагенов могут появиться кровянистые выделения, это говорит о достаточной количестве эстрогенов в организме и исключает первичный гипогонадизм.
Инструментальная диагностика
УЗИ органов малого таза позволяет оценить развитие яичников и матки, определить толщину эндометрия. Проводится во всех случаях гипогонадизма.
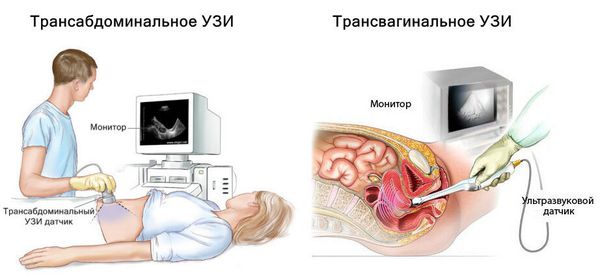
УЗИ органов малого таза
МРТ головного мозга проводится при подозрении на органические нарушения в гипоталамо-гипофизарной системе.
Оценка плотности костной ткани назначается девочкам пубертатного возраста и взрослым женщинам с гипогонадизмом при наличии отягощённого анамнеза: вторичной аменореи; функционального гипогонадотропного гипогонадизма, связанного с хроническими воспалительными заболеваниями кишечника (болезнью Крона, неспецифическим язвенным колитом); целиакии; сахарного диабета 1-го типа и др.
При подозрении на гипогонадизм дифференциальный диагноз проводится между его видами и формами.
Лечение гипогонадизма у женщин
Если в кариотипе есть мужская Y-хромосома или её фрагмент, то чаще всего яичники удаляют до 20 лет из-за высокого риска их злокачественного перерождения. После удаления яичников проводят заместительную гормональную терапию (ЗГТ) до возраста естественной менопаузы (как правило, она наступает в 46–50 лет) для профилактики осложнений, таких как остеопороз. Лечение начинают с назначения эстрогенов в форме таблеток или пластырей, далее переходят на циклическую гормональную терапию с добавлением гестагенов. Для стимуляции роста также применяют малые дозы гормона роста .
При опухолях гипофиза лечение хирургическое. ЗГТ требуется, если гипофиз перестал вырабатывать гормоны. Объём терапии зависит от результатов клинических и лабораторных исследований, как правило, ЗГТ в этом случае проводится пожизненно или до возраста физиологической менопаузы, если речь о половых гормонах.
При врождённом вторичном гипогонадизме также требуется ЗГТ . Половое созревание в этом случае стимулируется препаратами эстрогенов. При появлении на УЗИ фолликулов в яичниках, повышении уровня эстрогенов и появлении менструальноподобных выделений к терапии добавляют прогестерон, чтобы предотвратить гиперплазию эндометрия и установить регулярный менструальный цикл. Если выделений нет, значит эстрогена недостаточно и терапию нужно скорректировать.
Если пациентка хочет забеременеть, проводят стимуляцию овуляции . При успешном зачатии женщину будет наблюдать акушер-гинеколог согласно клиническим рекомендациям по нормальной беременности.
При гипогонадизме, который связан с синдромом резистентных яичников, проводят менопаузальную гормональную терапию двух- и трёхфазными эстроген-гестагенными препаратами до возраста физиологической менопаузы .
В случаях функционального гипогонадизма и синдрома гиперторможения яичников специфическую терапию не проводят. Пациентке нужно нормализовать режим сна и отдыха, питание и отменить КОК, тогда система гипоталамус-гипофиз-гонады восстановится самостоятельно в течение 3–4 месяцев .
Прогноз. Профилактика
При первичном гипогонадизме пациентка не сможет забеременеть самостоятельно, но благодаря программам вспомогательных репродуктивных технологий (ВРТ) с донорской яйцеклеткой женщина может забеременеть и родить .
У таких пациенток повышен риск развития опухолей яичников, поэтому им рекомендуется регулярно посещать гинеколога и проходить дополнительные обследования, если обнаруживаются отклонения.
При врождённом вторичном гипогонадизме рекомендовано применение ВРТ со стимуляцией овуляции . Спонтанная беременность чаще всего невозможна.
При функциональном гипогонадизме способность к зачатию восстанавливается, когда исчезают провоцирующие факторы. Если беременность не наступает в течение года у женщин до 35 лет и в течение 6 месяцев у женщин старше 35 лет, также требуется стимуляция овуляции .
Во всех вышеперечисленных случаях пациентки могут выносить ребёнка самостоятельно. Беременность наблюдает акушер-гинеколог согласно рекомендациям по нормальной беременности.
Профилактика женского гипогонадизма
Специфической профилактики не существует. Всем пациенткам с гипогонадизмом независимо от его вида и формы рекомендуется вести здоровый образ жизни, чтобы не допустить осложнений: спать не менее 8 часов в сутки, рационально питаться и быть физически активными.
Список литературы
- Vogiatzi M. G. Hypogonadism // Medscape. — 2021.
- Эндокринология: национальное руководство / под ред. И. И. Дедова, Г. А. Мельниченко. — 2-е изд., перераб. и доп. — М.: ГЭОТАР-Медиа, 2018. — 832 с.
- Paduch D. A., Bolyakov A., Cohen P., Travis A. Reproduction in men with Klinefelter syndrome: the past, the present, and the future // Semin Reprod Med. — 2009. — Vol. 27, № 2. — Р. 137–148.ссылка
- Donaldson M. D., Gault E. J., Tan K. W., Dunger D. B. Optimising management in Turner syndrome: from infancy to adult transfer // Arch Dis Child. — 2006. — Vol. 91, № 6. — Р. 513–520.ссылка
- Российское общество акушеров-гинекологов. Женское бесплодие: клинические рекомендации. — 2021. — 82 с.
- Silveira L. F., Latronico A. C. Approach to the patient with hypogonadotropic hypogonadism // J Clin Endocrinol Metab. — 2013. — Vol. 98, № 5. — Р. 1781–1788. ссылка
- Gravholt C. H., Andersen N. H., Conway G. S. et al. International Turner Syndrome Consensus Group. Clinical practice guidelines for the care of girls and women with Turner syndrome: proceedings from the 2016 Cincinnati International Turner Syndrome Meeting // Eur J Endocrinol. — 2017. — Vol. 177, № 3. — Р. G1–G70.ссылка
- Palmert M. R., Dunkel L. Clinical practice. Delayed puberty // N Engl J Med. — 2012. — Vol. 366, № 5. — Р. 443–453.ссылка
- Sidhoum V. F., Chan Y. M., Lippincott M. F. Reversal and relapse of hypogonadotropic hypogonadism: resilience and fragility of the reproductive neuroendocrine system // J Clin Endocrinol Metab. — 2014. — Vol. 99, № 3, — Р. 861–870. ссылка
- Coss D., Mellon P. L., Thackray V. G. A FoxL in the Smad house: activin regulation of FSH // Trends Endocrinol Metab. — 2010. — Vol. 21, № 9. — Р. 562–568.ссылка
- Richards J. S., Pangas S. A. The ovary: basic biology and clinical implications // J Clin Invest. — 2010. — Vol. 120, № 4. — Р. 963–972.ссылка
- Themmen A. P. N., Huhtaniemi I. T. Mutations of gonadotropins and gonadotropin receptors: elucidating the physiology and pathophysiology of pituitary-gonadal function // Endocr Rev. — 2000. — Vol. 21, № 5. — Р. 551–583.ссылка
- Российское общество акушеров-гинекологов. Аменорея и олигоменорея: клинические рекомендации. — 2021. — 57 с.
- Macklon N. S., Stouffer R. L., Giudice L. C., Fauser B. C. The science behind 25 years of ovarian stimulation for in vitro fertilization // Endocr Rev. — 2006. — Vol. 27, № 2. — Р. 170–207. ссылка
- Макрецкая Н. А., Герасимова М. В., Васильев Е. В. и др. Клиническая и молекулярно-генетическая характеристика случаев изолированного гипогонадотропного гипогонадизма, обусловленного дефектами рецептора гонадотропин-рилизинг-гормона // Проблемы эндокринологии. — 2021. — Т. 67, № 3. — C. 62–67.
- Young J., Xu C., Papadakis G. E. et al. Clinical Management of Congenital Hypogonadotropic Hypogonadism // Endocr Rev. — 2019. — Vol. 40, № 2. — Р. 669–710. ссылка
- Maione L., Dwyer A. A., Francou B. Genetics in endocrinology: genetic counseling for congenital hypogonadotropic hypogonadism and Kallmann syndrome: new challenges in the era of oligogenism and next-generation sequencing // Eur J Endocrinol. — 2018. — Vol. 178, № 3. — Р. R55–R80.ссылка
- Stamou M. I., Cox K. H., Crowley W. F. Jr. Discovering Genes Essential to the Hypothalamic Regulation of Human Reproduction Using a Human Disease Model: Adjusting to Life in the «-Omics» Era // Endocr Rev. — 2015. — Vol. 36, № 6. — Р. 603–621.ссылка
- Celik O., Celik N., Aydin S. et al. Ghrelin action on GnRH neurons and pituitary gonadotropes might be mediated by GnIH-GPR147 system // Horm Mol Biol Clin Investig. — 2016. — Vol. 25, № 2. — Р. 121–128.ссылка
- Persani L., Bonomi M., Cools M. et al. ENDO-ERN expert opinion on the differential diagnosis of pubertal delay // Endocrine. — 2021. — Vol. 71, № 3. — Р. 681–688.ссылка
- Boehm U., Bouloux P. M., Dattani M. T. et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism — pathogenesis, diagnosis and treatment // Nat Rev Endocrinol. — 2015. — Vol. 11, № 9. — Р. 547–564. ссылка
- Российская ассоциация эндокринологов. Гипогонадизм у детей и подростков: клинические рекомендации. — 2016. — 23 с.