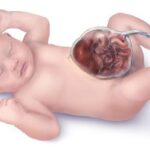
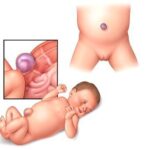
Синдром Беквита — Видемана(Beckwith-Wiedemann syndrome) — это генетическое заболевание, для которого характерна триада признаков: чрезмерный рост и вес, большой язык и омфалоцеле (выпячивание органов брюшной полости в области пупочного кольца). Болезнь ещё называют синдромом гигантизма с пуповинной грыжей (грыжей пупочного канатика).
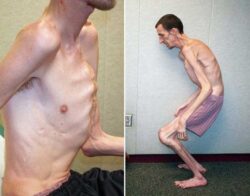
К дополнительным признакам относится гемигиперплазия (одна сторона тела растёт больше, чем другая), расхождение прямых мышц живота, пупочная грыжа, эмбриональные опухоли, увеличение коры надпочечников и размеров внутренних органов, аномалии почек, низкий уровень глюкозы в первый месяц жизни, насечки на мочке уха и характерные черты лица. Последняя особенность более узнаваема в младенчестве и становится менее очевидной в старшем возрасте .

Синдром Беквита — Видемана [17]
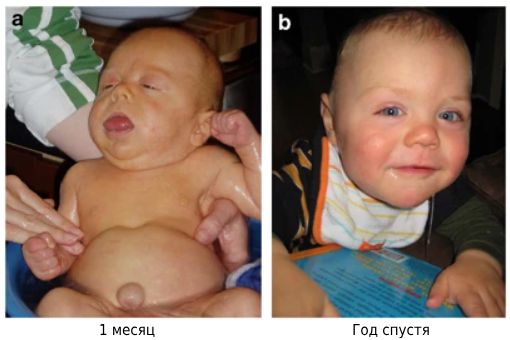
Синдром Беквита — Видемана [17]
Распространённость
Синдром Беквита — Видемана (СБВ) выявляют у 1 из 13 700 детей, мальчики и девочки болеют одинаково часто . Однако заболевание на самом деле может встречаться чаще, так как у больных с менее выраженными симптомами его могут не диагностировать. Распространённость синдрома не зависит от географических, этнических или социальных особенностей.
Гемигиперплазию выявляют у 1 из 86 000 пациентов, чаще у девочек .
Причины синдрома Беквита — Видемана
Около 85 % случаев СБВ возникают случайно и только 15 % наследуются от родителей .
К основным причинам и факторам риска этого заболевания относятся:
1. Генетические мутации. Большинство случаев СБВ — это результат генетических мутаций. Одним из ключевых генов, ответственных за нормальную регуляцию роста и развития, является CDKN1C. Мутации в этом гене считаются наиболее распространённой причиной синдрома Беквита — Видемана. Несмотря на то что 85 % случаев возникают из-за новых мутаций и ранее заболевание не встречалось в семье, иногда, в 15 % случаев, повреждённые гены передаются от одного из родителей. Ребёнок, который наследует изменённый ген, может не иметь каких-либо характерных признаков этого заболевания, чаще они присутствуют, если этот ген получен от матери . Более детально генетические причины представлены в таблице ниже.
2. Эпигенетические изменения. Эти изменения связаны не с мутациями, а с тем, как гены регулируются в организме. Как правило, у здоровых людей в геноме есть регуляторные механизмы, которые позволяют правильно контролировать экспрессию генов — процесс, при котором наследственная информация от участка ДНК преобразуется в РНК или белок. Если эти механизмы не работают должным образом, могут возникнуть изменения в метилировании ДНК или хроматиновой упаковке, что может снизить или увеличить экспрессию генов, в том числе и тех, которые ответственны за развитие СБВ. Некоторые эпигенетические изменения могут возникать во время беременности из-за аномального развития плаценты или других факторов, таких как курение, недостаток питательных веществ или стресс.
Генетические и эпигенетические причины СБВ
| Молекулярные группы | Частота | Наследственность |
|---|---|---|
| Отсутствие метилирования гена IC2 (KCNQ1OT1) на материнской хромосоме | 50 % | Впервые в семье |
| Отцовская однородительская дисомия, при которой ребёнок получает две копии хромосомы от матери и ни одной от отца | 20 % | Впервые в семье |
| Мутация гена CDKN1C | 5 % случайно 40 % от родителя | Почти исключительно от матери |
| Гиперметилирование (избыточное добавление метильных групп) IC1 (H19) на материнской хромосоме: без делеции или с делецией, т. е. с потерей участка хромосомы или без | 5 % | Впервые в семье. Если с делецией, то наследуется от матери |
| Цитогенетически видимая дупликация (удвоение) хромосомы 11p15 | < 1 % | Наследуется от отца |
| Транслокация или инверсия хромосомы. Транслокация происходит, когда часть одной хромосомы переносится и присоединяется к другой хромосоме. Инверсия — часть хромосомы переворачивается на 180 ° и встраивается обратно в ту же хромосому | < 1 % | Наследуется от матери |
3. Вспомогательные репродуктивные технологии. Применение экстракорпорального оплодотворения (ЭКО) повышает риск развития СБВ в 4 раза . Однако не все исследования подтверждают такой результат, к тому же это не означает, что ЭКО непременно приводит к СБВ. Механизм, из-за которого при ЭКО чаще возникает СБВ, до конца не изучен.
4. Возраст матери и повторная беременность — также могут повышать риск развития СБВ.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы синдрома Беквита — Видемана
Клиническая картина СБВ неоднородна и может отличаться у разных пациентов. Некоторые симптомы заболевания могут проявиться с возрастом, тогда как часть признаков присутствует сразу после рождения.
К основным симптомам синдрома Беквита — Видемана относятся:
- Макроглоссия: увеличенный размер языка, что часто заметно сразу после рождения. Язык может выходить за пределы полости рта и влиять на кормление ребёнка. Размер языка может быть настолько велик, что он может блокировать дыхательные пути, вызывая нарушение дыхания, а также задержку в развитии речи у детей старшего возраста.
- Омфалоцеле: проявляется дефектом пупочного кольца, через который органы брюшной полости выходят наружу, эту патологию можно обнаружить на скрининговом УЗИ.
- Гемигипертрофия: несимметричный рост одной стороны тела по сравнению с другой.
- Неонатальная гипогликемия: низкий уровень глюкозы в крови в первый месяц жизни, встречается примерно у половины детей с СБВ. Может проявляться тремором, сонливостью, учащённым сердцебиением, трудностями с кормлением, судорогами с потерей сознания и в самых тяжёлых случаях — комой.
- Эмбриональные опухоли: у пациентов с СБВ повышен риск развития злокачественных новообразований, таких как опухоль Вильмса (эмбриональный рак почки) и гепатобластома (опухоль печени).
- Недостаточность иммунобиологических защитных функций: у некоторых пациентов наблюдается дефицит антител классов IgA, IgG или IgM, что увеличивает риск возникновения инфекций.
- Различные дефекты почек и мочевыводящих путей: в некоторых случаях выявляют аномалии в работе почек и мочевыводящих путей, из-за чего может нарушаться мочеиспускание.
- Спланхномегалия: увеличение размеров внутренних органов брюшной полости (печени, поджелудочной железы, селезёнки и др.) .
- Передние складки мочки уха и/или задние спиральные ямки (на одном ухе или на обоих).
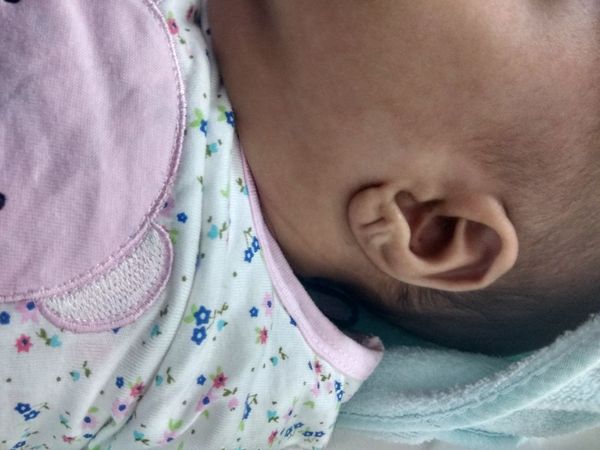
Передние складки мочки уха [17]
Патогенез синдрома Беквита — Видемана
Синдром Беквита — Видемана (СБВ) развивается из-за различных генетических и эпигенетических причин. На фоне этих изменений нарушается работа генов на участке р15 11-й хромосомы, отвечающих за рост и развитие эмбриона и плаценты . В этом кластере генов есть две области: теломерная и центромерная. Теломерная область включает гены H19 и IGF2, а центромерная — KCNQ1, KCNQ1OT1 и CDKN1C.
Так, CDKN1C кодирует белок, ограничивающий деление и рост клеток, а IGF2 — инсулиноподобный фактор роста, стимулирующий рост. При нарушениях, связанных с этими генами, могут возникать различные формы синдрома Беквита — Видемана. Например, нарушение экспрессии CDKN1C может привести к разрастанию многих тканей, что является общим проявлением СБВ. Примерно у половины пациентов с этим заболеванием выявляют адренокортикальные опухоли, а также опухоли мышц и почек .
Классификация и стадии развития синдрома Беквита — Видемана
В Международной классификации болезней (МКБ-10) синдром Беквита — Видемана относится к подгруппе Q87.3 Синдромы врождённых аномалий, проявляющихся избыточным ростом (гигантизмом) на ранних этапах развития. К Q87.3 также относятся синдромы Сотоса и Уивера .
Осложнения синдрома Беквита — Видемана
Наиболее опасные осложнения СБВ — это раковые опухоли, такие как опухоль Вильмса, гепатобластома и мезобластная нефрома. При ранней диагностике и своевременном лечении эти новообразования не приводят к гибели ребёнка. Однако у пациентов сохраняется высокая вероятность смерти из-за множественных врождённых аномалий и полиорганных нарушений, т. е. изменений в работе сразу нескольких органов. От этих осложнений погибает до 20 % детей с СБВ .
Диагностика синдрома Беквита — Видемана
СБВ можно заподозрить во время беременности с помощью УЗИ. В таких случаях роды должны проходить в специально оборудованном центре — с наличием отделения детской хирургии и интенсивной терапии новорождённых.
Сбор анамнеза и осмотр
Для диагностики синдрома Беквита — Видемана используются различные методы. В первую очередь врач осматривает ребёнка, собирает жалобы и анамнез (историю болезни) у родителей. При сборе семейного анамнеза доктор расспросит родителей об увеличенном языке при рождении и опухолях среди родственников .
У ребёнка обычно отмечается чрезмерный рост и вес, большой язык, асимметрия тела и дефекты передней брюшной стенки, такие как омфалоцеле или пупочная грыжа.
Физикальное обследование может также помочь в постановке диагноза СБВ. Для этого используется таблица диагностических критериев, которая включает большие и малые признаки. Для постановки диагноза требуется наличие трёх больших признаков или двух больших и одного малого.
Большие признаки:
- дефект передней брюшной стенки: омфалоцеле или пупочная грыжа;
- макроглоссия (увеличение языка);
- макросомия (увеличение роста и веса, рост и вес > 97-го процентиля — для расчёта можно использовать специальный калькулятор макросомии, который есть в интернете);
- передние складки мочки уха и/или задние спиральные ямки (на одном ухе или на обоих);
- увеличение печени, почек, селезёнки, поджелудочной железы и надпочечников;
- эмбриональные опухоли в детском возрасте;
- гемигиперплазия (одна сторона тела растёт больше, чем другая);
- увеличение коры надпочечников, как правило диффузное и двустороннее;
- аномалии почек, в том числе медуллярная дисплазия с последующим развитием медуллярной губчатой почки;
- случаи СБВ в семье;
- расщелина нёба.
Малые признаки:
- при беременности: многоводие, большая плацента и/или толстая пуповина;
- преждевременные роды;
- низкий уровень глюкозы в первый месяц жизни;
- пламенеющий невус;
- кардиомегалия (увеличение сердца), структурные аномалии сердца или кардиомиопатия (поражение сердечной мышцы);
- опережение костного возраста;
- расхождение прямых мышц живота;
- характерное лицо.

Характерное лицо при СБВ [17]
Например: если у ребёнка наблюдается макроглоссия и пупочная грыжа, т. е. только два больших признака, и нет малых признаков, то СБВ не выставляется и врач продолжает обследование для выявления других заболеваний.
Лабораторная и инструментальная диагностика
Проводится после физикального осмотра. Рекомендуется сдать анализ крови на уровень глюкозы, инсулина, АФП, кальция и креатинина.
Инструментальные методы диагностики СБВ включают ЭхоКГ, ЭКГ, рентгенографию, КТ, МРТ и УЗИ.
ЭхоКГ и ЭКГ могут использоваться для оценки работы сердца, так как у больных часто встречается кардиомегалия и другие структурные аномалии сердца. Эти методы могут также помочь выявить кардиомиопатию.
Рентгенография, КТ, МРТ и УЗИ могут дать дополнительную информацию об изменениях в органах и тканях. Признаками СБВ могут быть спланхномегалия (увеличение внутренних органов), что может свидетельствовать о наличии опухолей.
Генетическое исследование
Чтобы окончательно подтвердить диагноз, необходимо пройти генетическое исследование. СБВ вызвано изменениями в различных генах, поэтому лабораторная диагностика включает анализ нескольких генетических мутаций (генов KCNQ1OT1, H19 и CDKN1C).
Дополнительные методы диагностики
У детей старше одного года проводится оценка когнитивных способностей. Особенно это актуально для малышей с задержкой развития или другими расстройствами нервной системы — низкий уровень глюкозы в первые месяцы после рождения может привести к поражению головного мозга.
Дифференциальная диагностика
СБВ нужно отличать от синдромов, которые также проявляются макросомией.
| Синдром | Сходство с СБВ | Отличие от СБВ |
|---|---|---|
| Симпсона — Голаби — Бемеля | — увеличение роста, веса ребёнка; — увеличение органов; — макроглоссия; — почечные аномалии; — повышенный риск эмбриональных опухолей | — грубые черты лица: антимонголоидный разрез глаз (наружные уголки глаз расположены ниже внутренних), срединная борозда на нижней губе; — расщелина верхней губы; — структурные аномалии сердца и нарушения проводимости; — скелетные аномалии, включая полидактилию (наличие дополнительных пальцев на кистях или стопах); — отставание в умственном развитии |
| Перлмана | — макросомия; — высокий риск опухоли Вильмса
| — характерные черты лица (маленькая верхняя или нижняя челюсть, низко посаженные уши, вдавленная переносица, перевёрнутая V-образная кайма верхней губы); — высокая смертность в первый месяц жизни; — значительные интеллектуальные нарушения |
| Костелло | — симптомы проявляются только в неонатальном периоде (до 28 дня жизни) | — нарушения в работе сердца; — отставание в развитии; — огрубление черт лица |
| Сотоса | — макросомия | — характерные черты лица (длинная и узкая форма головы, лобные утолщения, антимонголоидный разрез глаз, острый подбородок); — редкие волосы в лобно-теменной области; — интеллектуальная недостаточность; — макроцефалия (увеличение размеров головы и головного мозга) |
| Мозаицизм по отцовской однородитель- ской дисомии | — большой вес для гестационного возраста; — большая плацента; — макроглоссия; — низкий уровень глюкозы на фоне избытка инсулина; — пупочная грыжа; — увеличение печени; — гемангиома; — повышенный риск опухолей почек, печени и надпочечников | — выраженная задержка развития; — признаки, характерные для импринтинга |
Лечение синдрома Беквита — Видемана
СБВ относится к генетическим заболеваниям, поэтому вылечить его полностью нельзя. Лечение прежде всего носит симптоматический характер и требует индивидуального подхода с учётом особенностей пациента. В связи с этим рекомендуется пройти комплексное обследование у эндокринолога и хирурга, после чего врачи подберут оптимальную тактику лечения.
Гипогликемия, которая возникает у 30–60 % пациентов с СБВ и связана с избытком инсулина, может быть временным или стойким состоянием и требовать медикаментозного лечения: введения глюкозы, диазоксида или соматостатина до прекращения гипогликемических состояний. В некоторых тяжёлых случаях потребуется субтотальная панкреатэктомия, при которой удаляется часть поджелудочной железы.
Макроглоссия — это ещё один распространённый симптом СБВ, который наблюдается у 90 % пациентов. Дети с лёгкой или умеренной макроглоссией, как правило, по мере роста лицевых костей учатся управлять языком, так что со временем могут полностью удерживать его в полости рта, речевые дефекты в этом случае корректирует логопед. В более тяжёлых случаях, при трудностях с дыханием, кормлением, речью и артикуляцией, может потребоваться хирургическое вмешательство — частичная резекция языка.
Дефекты брюшной стенки могут также наблюдаться у пациентов с СБВ и требуют консультации хирурга и последующего оперативного лечения.
Избыточный рост и асимметричное развитие частей тела — ещё два распространённых симптома, возникающие примерно у половины пациентов с СБВ. Лечение может включать подбор обуви или хирургическую коррекцию длины ног .
Прогноз. Профилактика
Большинство пациентов с СБВ во взрослом возрасте живут обычной жизнью, но прогноз зависит от тяжести изначальной патологии. У детей с лёгкой формой часто хороший прогноз, вырастая они не отличаются от сверстников и могут вести полноценную жизнь. Общая продолжительность жизни при этом такая же, как в среднем по популяции.
Со временем рост пациентов с СБВ замедляется, к подростковому возрасту различия между ними и сверстниками становятся менее заметными. Другие физические особенности, например увеличение языка, также становятся менее заметны во взрослом возрасте. Но даже если внешне ребёнок уже не отличается от сверстников, ему всё равно требуется постоянное диспансерное наблюдение, которое позволит на ранних стадиях выявить опасные осложнения.
У детей с тяжёлым течением синдрома и наличием множественных нарушений (включая опухоли, различные физические аномалии, гипогликемию) прогноз зависит от тяжести осложнений и эффективности лечения. Продолжительность жизни у таких пациентов напрямую связана с качеством получаемой медицинской помощи.
Профилактика осложнений СБВ
Для выявления генетических заболеваний, в том числе СБВ, во время беременности проводится УЗИ. Если у одного из родителей (особенно у матери) или у ранее рождённых детей уже выставлен диагноз СБВ, то за беременностью наблюдают особенно тщательно: на 16-й неделе нужно сдать анализ на АФП, а на 19–20-й и 32-й неделе пройти УЗИ. Если у первого больного ребёнка или родителя были обнаружены генетические отклонения, во время беременности может потребоваться диагностика с помощью биопсии хориона или амниоцентеза. При выявлении признаков СБВ роды проводятся в специально оборудованном центре.
После родов за новорождённым также пристально наблюдают, чтобы своевременно выявить и скорректировать гипогликемию — это поможет предотвратить поражение головного мозга.
Чтобы исключить онкологические заболевания, каждые 2–3 месяца до 4 лет проводится исследование АФП. При повышении его уровня рекомендуется сдавать анализ раз в месяц, а также по назначению лечащего врача проходить КТ или МРТ и посещать онколога . После 4 лет лечащий врач на основании наблюдения за ребёнком и результатов предыдущих обследований может рекомендовать продолжить контроль АПФ с интервалом в несколько месяцев или перейти к проверке раз в год, а порой даже ещё реже (раз в 2–3 года).
При гемигиперплазии показан регулярный контроль длины и обхвата поражённых частей тела, а также обследование позвоночника для выявления сколиоза. Если разница в длине ног превышает 1 см, рекомендовано посетить ортопеда и носить ортопедические стельки. Оценка костного возраста для прогнозирования роста пациента во взрослом возрасте также является важным этапом в профилактике и диспансерном наблюдении.
При задержке психического развития и нарушения поведения проводятся специальные коррекционные программы.
Для контроля за состоянием сердца и сосудов показано кардиологическое обследование: ЭКГ и ЭхоКГ. Кроме того, рекомендовано проходить УЗИ брюшной полости и почек, чтобы исключить или своевременно обнаружить увеличение размеров внутренних органов. УЗИ рекомендуется делать каждые 3 месяца до 8-летнего возраста. По достижению 8 лет обследования по решению лечащего врача могут проводиться раз в год или даже реже.
Список литературы
- Weksberg R., Shuman C., Beckwith B. Beckwith-Wiedemann syndrome and hemihyperplasia. Management of Genetic Syndromes. — 3th edition. — John Wiley & Sons, 2010. — Р. 129–148.
- Li M., Squire J. A., Weksberg R. Molecular genetics of Beckwith-Wiedemann syndrome // Curr Opin Pediutr. — 1997. — № 6. — P. 623–629.ссылка
- Li M., Squire J. A., Weksberg R. Molecular genetics of Wiedemann-Beckwith syndrome // Am J Med Genet. — 1998. — № 4. — P. 253–259.ссылка
- Thorburn M. J., Wright E. S., Miller C. G., Smith-Read E. H. Exomphalos-macroglossia-gigantism syndrome in Jamaican infants // AmJ Dis Child. — 1970. — № 4. — P. 316–321.ссылка
- Parker D. A., Skalko R. J. Congenital asymmetry: Report of 10 cases with associated developmental abnormalities // Pediatrics. — 1969. — № 4. — P. 584–589.ссылка
- Elliott М., Maher E. R. Beckwith-Wiedemann syndrome // Med Genet. — 1994. — № 7. — Р. 560–564.ссылка
- Hoyme H., Seaver L. H., Jones K. L. Isolated hemihyperplasia (hemihypertrophy): Report of a prospective multicenter study of the incidence of neoplasia and review // Am J Med Genet. — 1998. — № 4. — P. 274–278.ссылка
- Pettenati M. J., Haines J. L., Higgins R. R. et al. Wiedemann-Beckwith syndrome: Presentation of clinical and cytogenetic data on 22 new cases and review of the literature // Hum Genet. — 1986. — № 2. — P. 143–154. ссылка
- Каширина Э. А., Рубцова А. А., Югай Н. М. и др. Тактика амбулаторного наблюдения за пациентом с синдромом Беквита — Видеманна (случай из практики) // Медицинский совет. — 2017. — № 19. — С. 1.
- Brioude F., Kalish J. M., Mussa A. et al. Expert consensus document: Clinical and molecular diagnosis, screening and management of Beckwith-Wiedemann syndrome: an international consensus statement // Nat Rev Endocrinol. — 2018. — № 4. — Р. 229–249. ссылка
- Clericuzio C. L., Martin R. A. Diagnostic criteria and tumor screening for individuals with isolated hemihyperplasia // Genetics in Medicine. — 2009. — № 3. — Р. 220–222.ссылка
- Gosden R., Trasler J., Lucifero D., Faddy M. Rare congenital disorders, imprinted genes, and assisted reproductive technology // Lancet. — 2003. — № 9373. — Р. 1975–1977. ссылка
- Eggermann T. Handbook of Epigenetics. — Academic Press, 2011. — P. 96–98.
- Pettenati M. J., Haines J. L., Higgins R. R. Wiedemann-Beckwith syndrome: presentation of clinical and cytogenetic data on 22 new cases and review of the literature // Hum Genet. — 1986. — № 2. — Р. 143–154. ссылка
- Назаренко Л. П., Никонов А. М. Федеральные клинические рекомендации по диагностике и лечению синдрома Беквита — Видемана. — М, 2017. — С. 6–7.
- Международная классификация болезней 10-го пересмотра. [Электронный ресурс]. Дата обращения: 29.09.2013.
- Pandita A., Gupta S., Gupta G., Panghal A. Beckwith-Weidemann syndrome with IC2 (KvDMR1) hypomethylation defect: a novel mutation // BMJ Case Rep. — 2018.ссылка