Пузырно—мочеточниковый рефлюкс (ПМР, ПМЛР) – патологический процесс ретроградного (обратного) заброса мочи из мочевого пузыря в верхние мочевые пути (мочеточник, лоханку, чашечки). Это происходит из-за несостоятельности клапанного механизма уретеро-везикального соустья (УВС) .
Обратный ток мочи впоследствии приводит к рефлюкс-нефропатии (нефросклерозу, фиброзу). Суть патологии в том, что структурно-функциональные единицы почки (нефроны) погибают и их замещает соединительная ткань. В результате почки уплотняются, сморщиваются, уменьшаются в размерах и перестают выполнять свои функции, вплоть до развития терминальной почечной недостаточности.
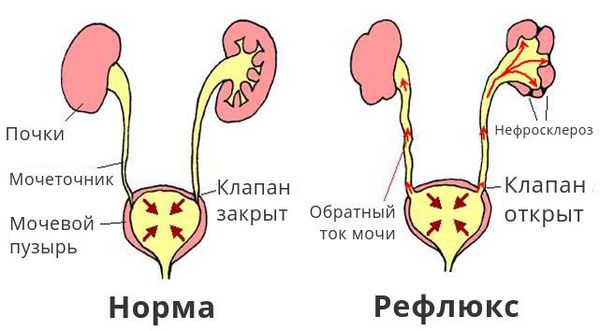
Здоровая мочевыделительная система и рефлюкс
Это наиболее часто встречающийся вид обструктивной уропатиии (нарушения нормального оттока мочи) у детей. Выявляется в 70 % случаев в возрасте до 1 года, у 25 % детей от 1 до 3 лет, у 15 % — от 4 до 12 лет. В старшем возрасте данное патологическое состояние встречается редко (в 5 % случаев), однако последствия его не менее разрушительны .
ПМР у детского населения чаще всего является результатом врождённой аномалии развития анатомических образований (мочеточников, УВС), вовлечённых в процесс физиологической динамики мочи. В этом случае рефлюкс считается первичным и иногда сочетается с другими пороками органов мочевой системы.
Напоминаем, что мышечные структуры в стенке мочеточника появляются на 15-20 неделе, а возможные дестриктуры в области пузырно-мочеточникового соустья формируются на 21-24 неделе. Это происходит в результате патологических воздействий разнообразных факторов: генетических, экзогенных (внешних), эндогенных (внутренних) или смешанных .
Наследование порока уретеро-везикального соустья связано с одиночным или несколькими генами. С вероятностью 50-70 % патология проявляется у детей, рождённых от родителей, имеющих ПМР. Данный факт свидетельствует о доминантной природе гена. Риск наследования, по сведениям разных авторов, имеют от 30 до 50 % близнецов .
Нарушение резервуарной и эвакуаторной функции мочевого пузыря (нейрогенная дисфункция мочевого пузыря — НДМП), сопровождающееся повышением внутрипузырного давления, является достаточно частой причиной появления пузырно-мочеточникового рефлюкса у детей и взрослых.
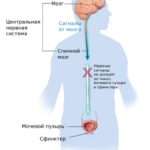
Иногда патологическая уродинамика с забросом мочи в вышележащие отделы мочевого тракта возникает вследствие аномалий развития других органов. В частности причиной могут стать дефекты развития спинного мозга, как изолированные, так и в сочетании с вариантами spina bifida aperta et occulta (неполным заращением позвоночных дужек). Например, расщепление спинного мозга или новообразования центральной нервной системы (липомы спинного мозга) .
Длительный инфекционно-воспалительный процесс в нижних мочевых путях может спровоцировать структурные нарушения клапанного аппарата уретеро-везикального соустья, что в конечном итоге приведёт к формированию ретроградного тока мочи.
Причиной ПМР могут стать врождённые аномалии развития органов мочевой системы:
- клапан задней уретры — складки слизистой оболочки, препятствующие течению мочи в мочеиспускательном канале;
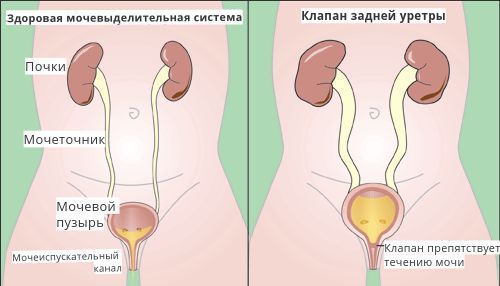
Врождённый клапан задней уретры
- удвоение почки и мочеточника;
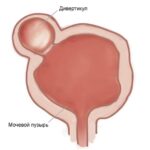
- дивертикул мочевого пузыря — мешковидное углубление в стенке мочевого пузыря;
- уретероцеле — кистозное расширение дистального отдела мочеточника .
Также пузырно-мочеточниковый рефлюкс может выступить в составе серьёзных генетических синдромов:
- болезнь Гиршпрунга — врождённый порок развития толстого кишечника, заключается в отсутствии нервных клеток в стенке кишки;
- синдром Эйлерса — Данлоса (гиперэластичность кожи) — генетическая патология соединительной ткани, вызванная дефектом в синтезе коллагена, и др. .
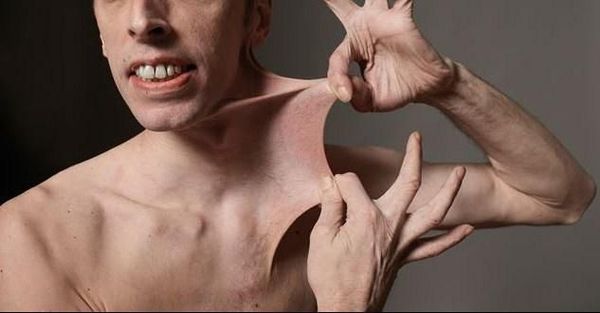
Синдром Эйлерса — Данлоса
У взрослых пациентов затруднённый поток мочи с последующим забросом её в вышележащие отделы мочевыделительного тракта является результатом множества причин:
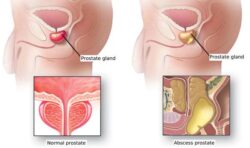
- доброкачественное образование предстательной железы у мужчин;
- сужение внутреннего или наружного просвета мочеиспускательного канала;
- склероз (рубцевание) шейки мочевого пузыря, в том числе вследствие длительного воспалительного процесса;
- детрузорно-сфинктерная диссинергия — нарушение процессов сокращения и расслабления мочевого пузыря;
- нейрогенная дисфункция мочевого пузыря;
- перенесённые оперативные и другие инвазивные диагностические или лечебные вмешательства в области мочепузырного треугольника (треугольника Льето, Trigonum vesicae);
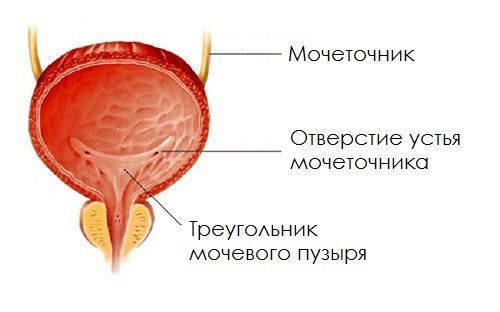
Расположение мочепузырного треугольника
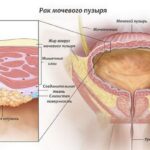
- новообразования в области малого таза, нарушающие естественный процесс опорожнения мочевого пузыря с повышением давления в его полости.
Независимо от возраста ПМР может стать последствием травмы спинного мозга, либо органов малого таза с развитием дисфункции нижних мочевыводящих путей .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы пузырно-мочеточникового рефлюкса
Наиболее вероятными признаками пузырно-мочеточникового рефлюкса являются эпизоды повышения температуры, чаще до фебрильных цифр (от 38 до 39 °С), без установленной причины. При этом объективный осмотр пациента не выявляет каких-либо признаков инфекционного процесса. Однако коварство рассматриваемого патологического состояния заключается в его способности маскироваться под другие заболевания, либо в некоторых случаях протекать бессимптомно. В таких случаях своевременная диагностика затруднена, что увеличивает вероятность и скорость развития нефросклероза.
У детей, поражённых инфекцией мочевыводящих путей, пузырно-мочеточниковый рефлюкс обнаруживается примерно в 25-40 % случаев . Атака острого пиелонефрита часто является первым клиническим проявлением рефлюкса у большинства больных. При этом отмечаются повышение температуры, боли в животе, пояснице, признаки интоксикации, изменение визуальных физических свойств мочи, расстройства стула. Чем младше ребёнок, тем выразительнее общие симптомы: у новорождённых наблюдается синдром интоксикации с поражением головного мозга, а выраженное беспокойство может выступать эквивалентом боли. В анализах мочи повышается количество лейкоцитов, белка. В гемограмме определяются лейкоцитоз (повышение числа лейкоцитов), ускорение СОЭ (скорости оседания эритроцитов).
Клиника острого цистита также является «тревожным звонком» в пользу возможного рефлюкса. При этом самыми характерными оказываются симптомы расстройства процесса мочеиспускания: поллакиурия (учащённое мочеиспускание), олигакиурия (редкие мочеиспускания), странгурия (болезненность при произвольном извержении мочи), ложные позывы к акту мочеиспускания, чувство неполного опорожнения мочевого пузыря и др. Вместе с этим происходит изменение мочевого осадка, для которого характерно повышение количества лейкоцитов и эритроцитов и особенно капля алой крови в конце акта мочеиспускания.
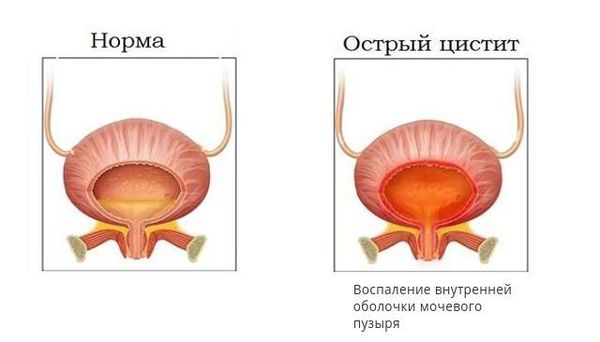
Здоровый мочевой пузырь и острый цистит
Ещё до постановки диагноза больные нередко обращают внимание на помутнение мочи, неприятный запах, изменение консистенции. В первую очередь это свидетельствует о наличии инфекции мочевыводящих путей, осложнившей пузырно-мочеточниковый рефлюкс. Среди изолированных нарушений акта мочеиспускания особенное значение придают двух-, трёхфазным мочеиспусканиям, которые являются результатом истечения мочи, скопившейся в вышележащих отделах мочевыделительной системы при активном рефлюксе. Иногда единственным признаком заболевания может выступить непроизвольное мочеиспускание в ночное время, появившиеся случаи дневного недержания, либо неудержания мочи в сочетании с мочевым синдромом (изменением объёма, состава и структуры мочи) или без него.
Повторные случаи инфекции мочевой системы неустановленной локализации, бессимптомная бактериурия (повышенное содержание бактерий в моче) также позволяют заподозрить пузырно-мочеточниковый рефлюкс. А иногда могут быть его единственным проявлением, что, несомненно, диктует необходимость наблюдения за пациентом.
Нередко допустить наличие ПМР позволяет длительный постоянный, либо повторяющийся болевой синдром. Дети старшего возраста и взрослые, как правило, жалуются на боли в поясничной области, самостоятельные и после мочеиспускания. Боль также может локализоваться в крестце, а у пациентов раннего дошкольного возраста — в животе. При этом не представляется возможным связать её возникновение с приёмом пищи или актом дефекации, что исключает болезни желудочно-кишечного тракта.
Некоторые клинические признаки: пастозность (отёчность) лица, отёки на ногах, периодическое или постоянное повышение артериального давления, астения, остеопороз и др., к сожалению, иногда являются первыми проявлениями болезни. Также они свидетельствуют о латентном хроническом пиелонефрите, разрастании соединительной ткани с образованием рубцов (фиброзировании почек/рефлюкс-нефропатии) и хронической почечной недостаточности.
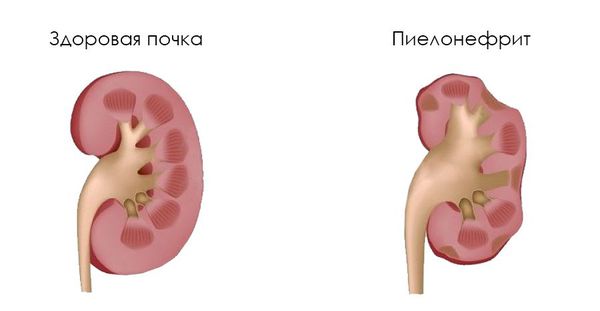
Здоровая почки и пиелонефрит
В некоторых случаях в результате длительного субклинического инфекционно-воспалительного процесса в мочевыделительной системе с развитием рефлюкс-нефропатии и почечной недостаточности выявляется задержка физического развития. Это может стать отправным критерием для дальнейшей диагностики и выявления дополнительных симптомов пузырно-мочеточникового рефлюкса. Клинико-лабораторные признаки анемии без обнаружения её причин и стойкости к стандартной терапии также могут указывать на длительно-существующий ретроградный ток мочи с развитием воспаления и выраженного нарушения почечных функций.
Патогенез пузырно-мочеточникового рефлюкса
Формирование физиологически полноценного пузырно-мочеточникового соустья с достаточным количеством мышечных и элластических структур начинается с эмбрионального периода развития и заканчивается в школьном возрасте. К 9-14 годам снаружи от циркулярного слоя начинает формироваться третий слой из продольных пучков гладкомышечных волокон.
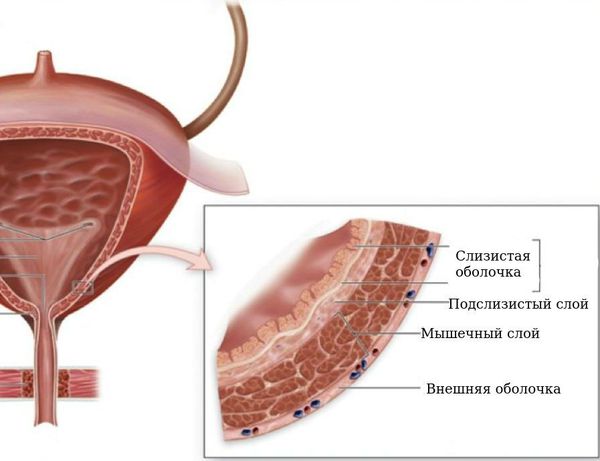
Строение мочевого пузыря (слои)
Этот слой завершает процесс формирования физиологических сфинктеров, или гидравлических жомов, что препятствует обратному забросу мочи из мочевого пузыря в вышерасположенные отделы мочевыделительной системы. В этом случае внутрипузырная часть мочеточника, заключаясь между слизистым и мышечным слоями мочевого пузыря, становится сомкнутой при наполнении последнего мочой. При правильном формировании замыкательных механизмов эластичность и мышечный тонус помогают неизменённому мочеточнику адаптироваться к меняющемуся объёму мочевого пузыря и давлению в нём.
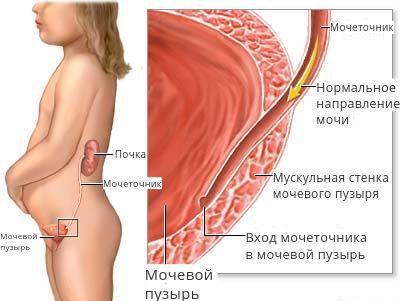
Внутрипузырная часть мочеточника
Если подслизистый отдел мочеточника уменьшен или практически отсутствует, если в мочепузырном треугольнике недостаточно гладкомышечных и соединительнотканных клеток, если давление в мочевом пузыре повышается по ряду ранее перечисленных причин, то формируется уретеротригональный дефект и происходит обратный заброс мочи, что способствует инфицированию вышерасположенных отделов мочевого тракта.
При этом микроорганизмы (чаще кишечная палочка, протей, клебсиелла и др.) благодаря наличию жгутиков и ворсинок более легко, чем в случае нормальной нисходящей уродинамики, адгезируются (прилипают) на уроэпителии, подавляя его местную иммунную защиту (макрофаги, лимфоциты, иммуноглобулин А, цитокины, белок Тамма — Хорсфалла и др.). Далее бактерии размножаются и выделяют продукты своей жизнедеятельности, вызывая общеинтоксикационные симптомы, а также расстройства мочеиспускания, болевые ощущения и т. п. Запускается каскад защитных реакций организма:
- перекисное окисление липидов;
- накопление свободных радикалов;
- местная гиперкоагуляция (повышение активности свёртывающей системы крови);
- выброс медиаторов воспаления, способствующих расширению сосудов, нарушению кровоснабжения органа. И многие другие патофизиологические механизмы .
«Гидродинамический удар» (скачок давления) в чашечно-лоханочную систему, рецидивирующий с различной степенью частоты и активности, постепенно приводит к формированию участков склерозирования почечной ткани, прежде всего канальцев, а затем и паренхимы. Под действием постоянно повышенного давления синтезируются факторы активации воспаления и фиброза: тромбоксан А2, фактор роста фибробластов, трансформирующий фактор роста, ангиотензин-2. В дальнейшем данные факторы увеличивают продукцию мезангиального матрикса (межклеточного вещества) и снижают его деградацию, провоцируют размножение фибробластов, что в конце концов приводит к развитию нефросклероза (рефлюкс-нефропатии) и почечной недостаточности .
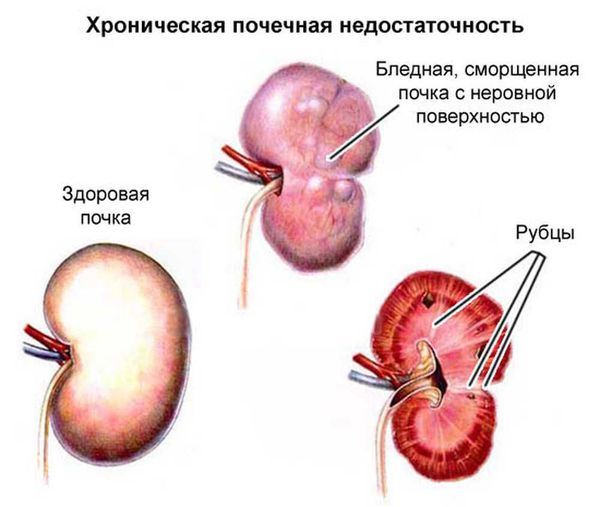
Хроническая почечная недостаточность
Высокая эпизодическая лихорадка в случае ПМР является отражением синтеза первичных и вторичных пирогенов — факторов, вызывающих подъём температуры тела (IL-1, IL-6, FNО – фактора некроза опухоли и др.). Они активизируются в результате растяжения лоханки и давления на почечную ткань или вследствие течения инфекционного процесса в мочевых путях.
Болевой синдром при течении рефлюкса может появиться по разным причинам:
- растяжение стенки почечной лоханки;
- спазм почечной лоханки в ответ на накопление в ней мочи и реакцию воспаления;
- растяжение почечной капсулы при отёке вследствие нарушения функционального состояния почек.
Классификация и стадии развития пузырно-мочеточникового рефлюкса
В зависимости от причины выделяют два типа пузырно-мочеточникового рефлюкса:
- первичный — нарушение (недоразвитие) мышечного аппарата слоев треугольника Льето, которое рассматривается как врождённый анатомический дефект;
- вторичный — является следствием инфравезикальной обструкции (заболеваний, вызывающих нарушение оттока мочи из мочевого пузыря), воспалительного процесса, эктопии устьев мочеточников, удвоения мочеточников, нейрогенной дисфункции мочевого пузыря, ятрогенных последствий и других выше названных причин.
По частоте возникновения пузырно-мочеточниковый рефлюкс бывает двух видов:
- постоянным;
- транзиторным (периодическим) — чаще появляется на фоне обострений или усугублений патологии других органов.
По тяжести протекания, согласно данным рентгеноурологического исследования (микционной цистографии), различают следующие формы рефлюкса:
- активный — возникает в момент мочеиспускания;
- пассивный — возникает в фазу наполнения;
- активно-пассивный или смешанный — обратная уродинамика осуществляется в обе фазы.
По физиологической выраженности различают пять степеней рефлюкса, выявляемые при микционной цистоуретерографии:
I степень — забрасывание рентгеноконтрастного вещества в дистальный отдел мочеточника без изменения его диаметра.
II степень — заполнение рентгеноконтрастным веществом мочеточника и чашечно-лоханочной системы без их расширения.
III степень — полостная система заполнена, мочеточник и лоханка расширены, но контуры чашечек не деформированы.
IV степень — расширенный мочеточник несколько извит, чашечки значительно уплощены, происходит умеренное истончение паренхимы почек.
V степень — вся полостная система значительно расширена без видимых сосочковых вдавлений, определяется значительное искривление мочеточника и резкое истончение паренхимы почек .
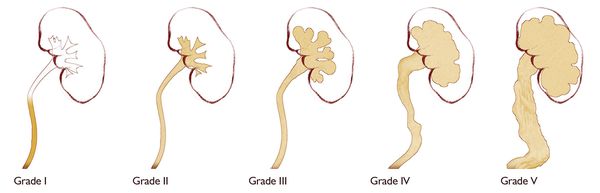
Степени развития пузырно-мочеточникового рефлюкса
Следует отметить, что помимо указанных критериев классификации при постановке диагноза необходимо учитывать осложнение рефлюкса, факт наличия рефлюкс-нефропатии, степень нарушения почечных функций.
Осложнения пузырно-мочеточникового рефлюкса
Часто на фоне рефлюкса, а также уже после его излечения, прогрессирует рефлюкс-нефропатия. Заболевание приводит к поражению всех структурных компонентов нефрона с развитием рубцевания почечной паренхимы, артериальной гипертензии и хронической почечной недостаточности. Такой больной в конце концов нуждается в постоянной заместительной терапии (гемодиализ, перитонеальный диализ), либо в трансплантации почки, что помимо ранней инвалидизации значительно снижает качество жизни больного .
Чем больше степень рефлюкса, тем выше вероятность и скорость развития осложнений. Однако иногда нефросклероз не подчиняется общеизвестным законам и склеротические процессы развиваются независимо от выраженности уродинамических нарушений. Доказано, что присутствие некоторых генов цитокинов (субстанций, ответственных за многие иммунные процессы в организме) предрасполагают к развитию нефросклероза при обструктивном пиелонефрите на фоне ПМР у детей. Также выявлены полиморфизмы (формы гена), влияющие на формирование врождённого рефлюкса непосредственно (полиморфный маркер rs2430561 гена INF-γ и др.) .
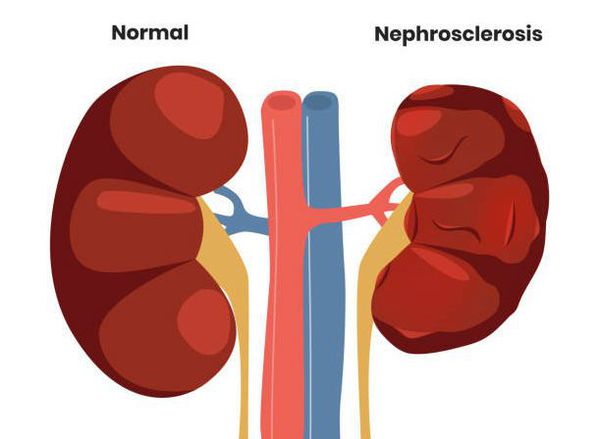
Нефросклероз
Диагностика пузырно-мочеточникового рефлюкса
Своевременное выявление пузырно-мочеточникового рефлюкса, качественное лечение и мониторинг позволяют предотвратить серьёзные осложнения с разрушительными последствиями для органа и организма в целом.
Тщательно собранный анамнез (включая семейный) составляет основу диагностики. Необходимо выяснить:
- характер мочеиспускания (у детей — беспокойство, натуживание, учащение, урежение, болезненность, двухкомпонентный мочевой акт, недержание, неудержание мочи и т. п.);
- факты немотивированных эпизодов повышения температуры, атак инфекций мочевыводящих путей;
- наличие необъяснимых болей в животе, пояснице, крестце;
- наследственность в плане заболеваний органов мочевой системы у близких и дальних родственников;
- течение беременности.
Физикальное обследование имеет не последнее значение в постановке диагноза. При этом обращают внимание на физическое развитие ребёнка, цвет кожи и слизистых, эластичность и влажность. Их патологические изменения могут быть признаком скрытого воспалительного процесса в мочевой системе, в том числе хронической почечной недостаточности. Наличие отёков различной локализации предоставляет возможность заподозрить снижение водовыделительной функции почек, сопутствующей ПМР. Необходимы осмотр и пальпация живота и поясничной области с оценкой болезненности в рёберно-позвоночных, рёберно-поясничных, мочеточниковых точках. Обязательным при любом виде объективного обследования является измерение артериального давления, частоты дыхательных движений, сердечных сокращений. Больному или его законному представителю необходимо в течение 2-3 суток регистрировать ритм спонтанных мочеиспусканий. Это поможет выявить картину функционального состояния мочевого пузыря.
Общий анализ крови косвенно указывает на какое-либо почечное страдание (анемию, лейкоцитоз, ускоренное СОЭ). Биохимичекий анализ крови с изменением нормальных показателей креатинина, мочевины, мочевой кислоты, электролитов свидетельствует о нарушенных канальцевых и клубочковых функциях. Проба Реберга, либо расчёт показателя скорости клубочковой фильтрации (очищения крови от продуктов обмена), рассчитанной по формуле Шварца, уточняет степень нарушения в почках.
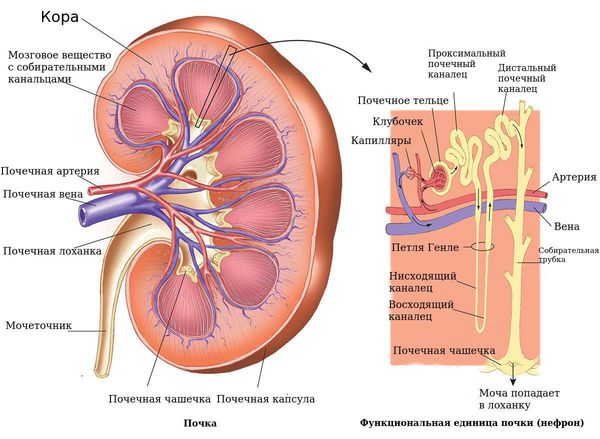
Процесс клубочковой фильтрации
Общий анализ мочи помимо воспалительных изменений, характерных для ПМР, может показать стойкую изолированную протеинурию (увеличение количества белка в моче), которая отражает присутствие рубцового процесса в почках при рефлюкс-нефропатии. Факт нарушения процессов концентрирования мочи при получении результатов диагностических проб (пробы Зимницкого) свидетельствует о снижении канальцевых функций. Регулярный посев мочи при установленном рефлюксе (не менее одного раза в шесть месяцев) помогает уточнить этиологию и стадию течения воспалительного процесса.
Из инструментальных методов исследования самым доступным является УЗИ органов мочевой системы, при котором обнаруживают косвенные признаки рефлюкса:
- расширение чашечно-лоханочной системы;
- изменение структуры слизистой лоханки, мочевого пузыря при сопутствующем воспалении;
- подозрение на другие пороки развития органов мочеобразования и мочевыделения, так как рефлюкс часто сочетается с таковыми.
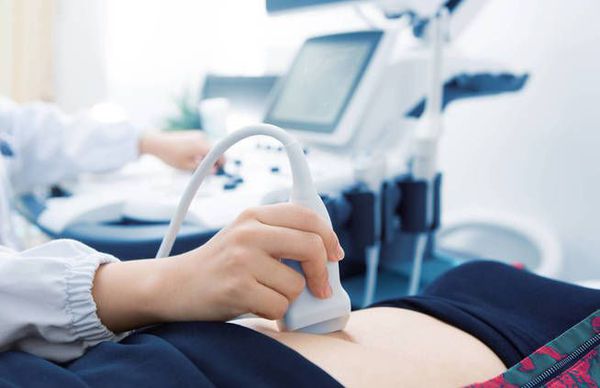
УЗИ органов мочевой системы
Доплерография (дуплексное сканирование почечного кровотока) позволяет определить состояние интраренальной гемодинамики, что ранее других методик визуализирует начало рефлюкс-нефропатии.
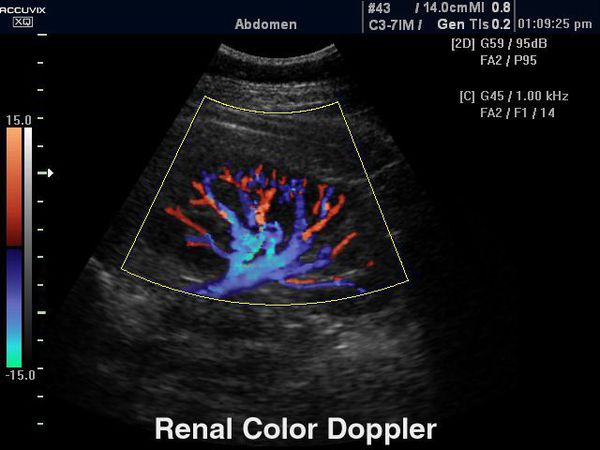
Доплерография (дуплексное сканирование почечного кровотока)
Первостепенным рентгеноконтрастным методом диагностики является микционная цистоуретрография (МЦУГ), позволяющая подтвердить, либо исключить заподозренный пузырно-мочеточниковый рефлюкс, а также установить его степень.
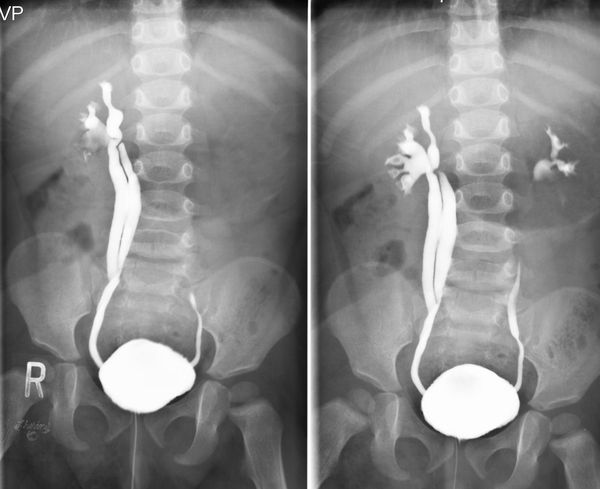
Микционная цистоуретрография
При радиоизотопной цистографии (РЦ) воздействие радиации значительно меньше, чем при МЦУГ, однако анатомические детали отражаются несколько слабее.
В клиническом отношении особое место занимает интермиттирующий пузырно-мочеточниковый рефлюкс, не доказанный повторными рентгенологическими методами, но имеющий характерную клиническую картину: рецидивирующий пиелонефрит, периодическую лейкоцитурию (повышенное количество лейкоцитов в моче), косвенные ультразвуковые и рентгенологические признаки. В таком случае ведение пациента осуществляется консервативным методом, либо решается вопрос об оперативном вмешательстве после визуализации зияющих устьев мочеточников при цистоскопии .
Всем больным с установленным ПМР ΙIΙ-IV степени показано проведение экскреторной урографии. Исследование осуществляется путём внутривенного введения рентгеноконтрастного препарата с последующим выполнением рентгенологических снимков. Данный метод позволяет визуализировать верхние мочевые пути и оценить их функциональность.
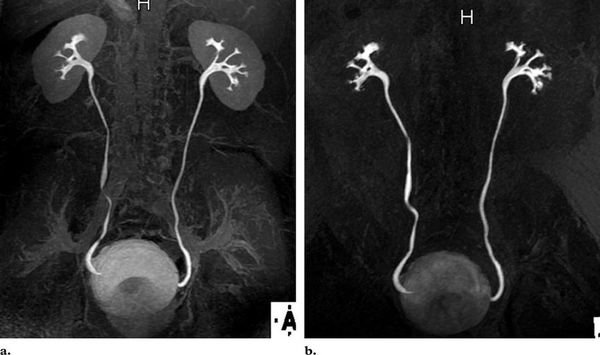
Экскреторная урография
Иногда выполняется уродинамическое исследование:
- для оценки функционально-обструктивных или функционально-необструктивных нейрогенных нарушений мочевого пузыря и сфинктеров;
- для определения функциональных нарушений нижних мочевых путей (урофлоуметрия, профилометрия пузырно-мочеточникового соустья и др.) .
Такое тестирование особенно важно для пациентов, у которых подозревается вторичный рефлюкс (при спинномозговой грыже или у мальчиков с клапанами задней уретры). Но в большинстве случаев у пациентов с нейрогенными дисфункциями мочеиспускания диагностика и оценка состояния в отдалённом периоде должна ограничиться неинвазивными методами (УЗИ мочевого пузыря, ритм спонтанных мочеиспусканий).
Статическая и динамическая нефросцинтиграфия (введение и регистрация выведения радиоизотопа) с последующей оценкой на сцинтиграмме послойной структуры, размеров почек при уже установленном ПМР проводиться регулярно. Радиоизотопная ренография оценивает работу почек и скорость выведения мочи из организма справа и слева в отдельности, частота исследований определяется индивидуально. Магнитно-резонансная томография, позволяющая подробно оценить паренхиму, наличие рубцов и аномалий, является нечастой альтернативой экскреторной урографии.
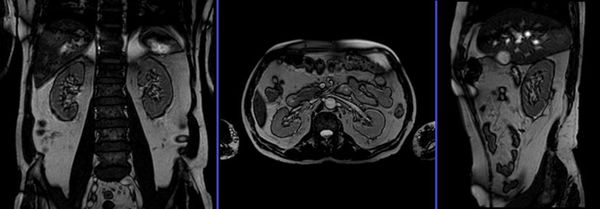
Магнитно-резонансная томография почек
Не менее важной является пренатальная (дородовая) диагностика рефлюкса. Наличие одно- двустороннего расширения лоханок у плода, иногда в сочетании с расширением мочеточника, нестабильные размеры и вариабельность их в пределах микционного цикла, нарушения мочеиспускания плода являются предвестниками формирования ПМР в постнатальном (внеутробном) периоде .
Обязательным является наблюдение специалистов: терапевта/педиатра, нефролога, уролога, стоматолога, оториноларинголога, по показаниям — невролога, офтальмолога, ортопеда. Целью наблюдения должна быть профилактика инфекций и перманентного повреждения почечной паренхимы, а также его поздних осложнений. Для этого назначается антибиотикопрофилактика, ренопротективная терапия и/или хирургическая коррекция рефлюкса.
Лечение пузырно-мочеточникового рефлюкса
В настоящее время не существует чётких представлений о выборе и эффективности способов и методов лечения в каждой конкретной клинической ситуации. Лечебные варианты представлены консервативной терапией и оперативными вмешательствами (эндоскопические, лапароскопические и открытые операции), изолированно или в комбинации.
Индивидуальный выбор и успех лечения пузырно-мочеточникого рефлюкса зависит от идентификации его степени, возраста больного, стадии течения воспалительного процесса, наличия почечных рубцов, функционального состояния поражённой почки, ёмкости и функции мочевого пузыря, наличия сочетанных аномалий мочевого тракта, сопутствующей патологии, длительности течения болезни и возраста пациента.
Консервативная терапия подразумевает комплекс мероприятий, целью которых является:
- профилактика обострений хронической мочевой инфекции и борьба с инфекцией;
- лечение рефлюкс-нефропатии;
- коррекция артериального давления;
- коррекция водно-электролитных нарушений;
- лечение дисфункции мочевого пузыря с постоянным мониторингом анатомического и функционального состояния верхнего мочевого тракта .
В состав консервативной терапии входят соблюдение достаточного питьевого режима, диеты с ограничением поваренной соли, жирной, жареной пищи, копчёностей, маринадов, консервантов, пряностей. В рацион стоит включить пищу, богатую витаминами, обладающую оптимальной калорийностью. Рекомендован достаточный уровень физической активности, ежедневное опорожнение кишечника. Обязателен режим принудительных мочеиспусканий (один раз в 1,5-2,0 часа), при этом иногда прибегают к временной, либо постоянной катетеризации мочевого пузыря.
Антибиотикотерапия проводится с учётом выявленной, либо природной чувствительности препарата к инфекционному агенту, рост которого определён при бактериальном посеве мочи. В качестве лечения выбирают «защищённые» пенициллины, цефалоспорины IΙ-IΙI поколения, фторхинолоны в возрастных дозировках. При снижении функции почек проводится коррекция дозы, либо кратности применения в зависимости от степени нарушения. Для лечения артериальной гипертензии и профилактики нефросклероза используют ингибиторы АПФ, ангиотензина ΙI, кальциевых каналов, бета-блокаторы. При этом выбор препарата осуществляется с учётом ведущих патогенетических механизмов, степени выраженности, сопутствующей патологии, возраста больного.
Коррекция дискоординации мочевого пузыря проводится в зависимости от источника нарушения (уровня регуляции нормального акта мочеиспускания), формы (гиперрефлекторной, гипорефлекторной, арефлекторной, норморефлекторной). Используются лекартсвенные препараты: М-холиноблокаторы, антагонисты мускариновых рецепторов, ингибиторы ацетилхолинэстеразы, ноотропы, седативные средства, витамины группы В.
Физиолечение представлено лекарственным электрофорезом, диадинамометрией, амплипульс-, лазеротерапией. Разработан комплекс лечебной физкультуры, направленный на укрепление мышц промежности. Противорецидивные курсы продолжаются в течение долгих месяцев с использованием уроантисептиков нитрофуранового ряда в дозах 1/5-1/15 от нормальных.
Электрофорез
Показаниями к оперативному лечению являются:
- неэффективность вышеуказанных методов;
- IΙI-V степени рефлюкса;
- низкая вероятность самостоятельного разрешения;
- нефросклероз;
- снижение функции почек более чем на 30 %;
- рецидивирующий пиелонефрит, цистит;
- сохраняющиеся фебрильные «температурные свечи» (нерегулярные подъёмы температуры до 39 °C и выше).
Относительным показанием к хирургической коррекции может явиться предпочтение родителей/законных представителей. Цель оперативного лечения — восстановление нарушенного антирефлюксного механизма. Открытая антирефлюксная операция (традиционная пересадка мочеточника с формированием нового устья) показана в основном для лечения высоких степеней рефлюкса с нарушением анатомии уретеро-везикального соустья.
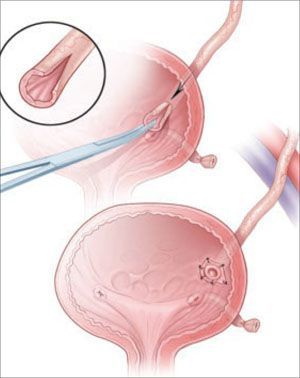
Пересадка мочеточника
Лапароскопическое вмешательство является альтернативой открытой операции, отличается меньшими инвазивностью и временем, затраченным на коррекцию. При лапароскопии вероятность и выраженность послеоперационных осложнений сведена к минимуму, восстановление проходит гораздо быстрее.
Эндоскопическое лечение подразумевает трансуретральное внедрение в подслизистый слой биоимплантов на основе тифлона, коллагена, силикона, геля для формирования состоятельности (замкнутости) пузырно-мочеточникового сегмента. При неэффективности вмешательства могут повторяться с вариациями вида операции.
При лечении вторичного ПМР на начальных этапах предлагается устранение причины, вызвавшей заболевание. Например, лечение нейрогенной дисфункции мочевого пузыря или хирургическое разрушение клапана задней уретры, ликвидация стенотического (суженного) участка мочеиспускательного канала у мальчиков, меатотомия (рассечение наружного отверстия уретры при её сужении) у девочек.
При потере функции почкой или выраженном её нарушении, проводится нефруретерэктомия (удаление почки с мочеточником).
Прогноз. Профилактика
Профилактика пузырно-мочеточникового рефлюкса заключается в планировании, правильном ведении беременности, внимательном физикальном осмотре пациента вне зависимости от возраста и клинической ситуации, своевременном опорожнении мочевого пузыря и кишечника. Широко распространено медико-генетическое консультирование. Рекомендуется не пренебрегать регулярной диспансеризацией, лечением на ранних стадиях любой патологии мочеполового тракта.
Для профилактики возможных тяжёлых и опасных для жизни осложнений пузырно-мочеточникого рефлюкса большое значение имеет выбор оптимальных методов оперативного лечения, консервативной терапии, в первую очередь антибактериальной. Мультидисциплинарный подход, грамотное ведение документации, внимательное наблюдение за пациентом позволяют предупредить возникновение и развитие серьёзных последствий.
Прогноз заболевания во многом зависит от своевременной диагностики и адекватности терапии, а также от степени рефлюкса и скорости развития рефлюкс-нефропатии.
Возможно спонтанное разрешение рефлюкса, чаще всего за счёт созревания корковых и спинальных механизмов регуляции произвольных микций и пузырно-мочеточникового сегмента. Вероятность самоизлечения тем выше, чем меньше степень рефлюкса и возраст ребёнка.
Ранняя постановка диагноза, особенно при ПМР невысокой степени, правильный выбор способа лечения в большинстве случаев позволяет избавиться от рефлюкса без тяжёлых последствий. В противном случае формируются грозные осложнения — вторичное сморщивание почки (почек) с последующей утратой их функций. Последнее приводит к почечной недостаточности, которая со временем может грозить трансплантацией органа, что значительно снизит качество жизни больного, а также может привести к гибели от различных осложнений.
Список литературы
- Батаева Е.П., Зеленева А.Ю., Калинина Л.Р. Клинический случай нейрогенной дисфункции мочевого пузыря на фоне липомы спинного мозга // Дальневосточный медицинский журнал. — 2016. — № 4. — С. 101-103.
- Бехало В.А., Сысолятина Е.В., Нагурская Е.В. Регуляция врождённого иммунного ответа в очаге хронического воспаления // Иммунология. — 2009. — №3. — С. 184-189.
- Дерюгина Л.А. Пузырно-мочеточниковый рефлюкс и его пренатальное прогнозирование // Педиатрия. Журнал им. Г.Н. Сперанского. — 2018. — Т. 97, № 5. — с 14-19.
- Клиническая нефрология детского возраста. Руководство для врачей. — СПб: Левша. — 2008. — 600 с.
- Лопаткин Н.А., Пугачев А.Г., Москалева Н.Г. Интермиттирующий пузырно-мочеточниковый рефлюкс у детей. — М.: Медицина, 2004. —136 с.
- Лубенников А.Е., Трушкин Р.Н., Подкорытова О.Л. Пузырно-мочеточниковый рефлюкс после трансплантации почки // Московский хирургический журнал. — 2014. — № 3 (37). — С. 64-68.
- Основные принципы диагностики и лечения расстройств мочеиспускания у детей и подростков : Методические рекомендации №10 / А.А. Камалов и др. — М., 2013. — 38 с.
- Писклаков А.В., Шевляков А.С., Павленко Н.И., Лысов Н.И. Показатели профилометрии уретеровезикального соустья при пузырно-мочеточниковом рефлюксе у детей с нейрогенной дисфункцией мочевого пузыря // Педиатрия. Журнал имени Г.Н. Сперанского. — 2016. – Т. 95, № 5. – С. 21-25.
- Хворостов И.Н., Смирнов И.Е., Зоркин С.Н. Обструктивные уропатии у детей // Российский медицинский журнал. — 2007. — №1. — С. 50.
- Шахновский Д.С., Зоркин С.Н., Савостьянов К.В., Пушков А.А., Бурденный А.М. Исследование полиморфизма генов TNF-α INFγ TGFβ c риском развития пузырно-мочеточникого рефлюкса у детей в российской популяции // Педиатрия. Журнал имени Г.Н. Сперанского. — 2018. — Т. 97, №5. — С. 79-84.
- Drozdz D,. Kwinta P., Sztefko K., Kordon Z., Drożdż T., Łątka M,. Miklaszewska M., Zachwieja K., Rudziński A., Pietrzyk J.A. Oxidative stress biomarkers and left ventricular hypertrophy in children with chronic kidney disease // Oxidative medicine and cellular longevity. — 2016.ссылка
- Copelovitch L., Warady B.A., Furth S.L. Insights from the Chronic kidney disease in children (CKiD) study // Clin. J. Am. Soc. Nephrol. — 2011; 6: 2047-2053. ссылка
- Lim R. Vesiculouretereal reflux and urinary tract infection: evolving practices and current controversies in pediatric imaging // AJR Am J Roentgenol. — 2009; 192 (5): 1197-208.ссылка
- Litwin M., Feber J., Niemirska A., Michalkiewicz J. Primary hypertension is a disease of premature vascular aging associated with neuro-immuno-metabolic abnormalities // Pediatr. Nephrol. — 2016; 31: 185-194.ссылка