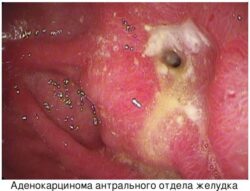
Рак мочевого пузыря (РМП) — заболевание, при котором в тканях мочевого пузыря образуются злокачественные клетки.
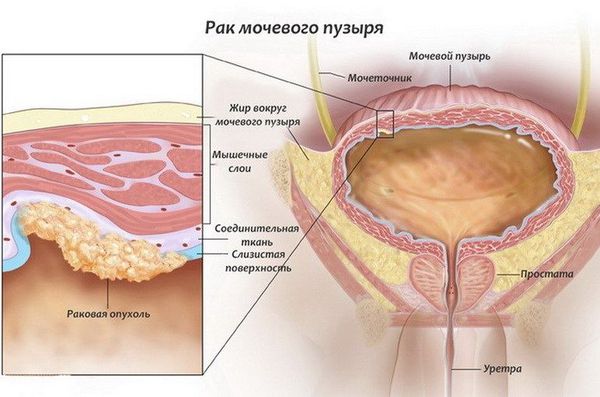
Злокачественная опухоль в мочевом пузыре
Анатомия и физиология мочевого пузыря
Мочевой пузырь — это непарный полый орган выделительной системы. Он расположен в нижней части живота и выполняет резервуарную функцию. В него по мочеточникам из почек поступает моча. Изнутри полость этого органа выстилает особый тип эпителия — уротелий.
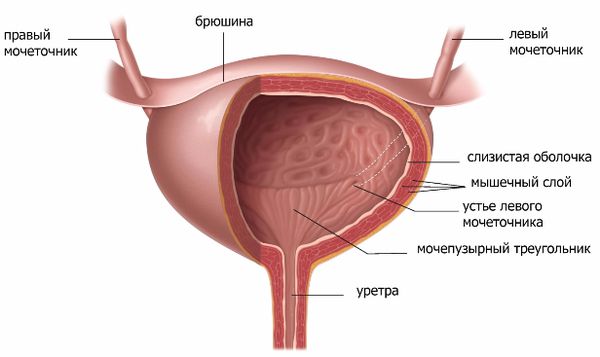
Анатомия мочевого пузыря
Распространённость рака мочевого пузыря
Согласно мировой статистике, каждый год появляется более 430 тысяч новых случаев заболевания (около 330 тысяч мужчин и примерно 99 тысяч женщин), и эта цифра продолжает расти . В России рак мочевого пузыря занимает третье место среди других онкоурологических заболеваний после рака предстательной железы у мужчин и рака почки у женщин (26,2 % случаев от всех злокачественных новообразований мочеполовой системы) . В 2016 году в нашей стране было впервые зарегистрировано максимальное количество случаев заболевания — более 16 тысяч, из них 12 тысяч у мужчин и 3 тысячи у женщин . В структуре онкологической заболеваемости на долю рака мочевого пузыря в 2016 году приходилось 4,6 % .
В США, где за год выявляется от 57 до 60 тысяч новых случаев РМП и ежегодно умирают 12,5 тысяч больных, эта патология занимает пятое место среди всех злокачественных новообразований, четвёртую позицию по частоте опухолей среди мужчин и девятую среди женского населения . Американское онкологическое общество (ACS) в 2018 году в США прогнозирует регистрацию новых случаев рака мочевого пузыря более чем у 81 тысячи человек, из них 62 тысячи мужчин и 18 тысяч женщин .
Это заболевание также является серьёзной проблемой для стран Европейского союза. Так, в 2012 году там было выявлено 124 тысячи новых случаев, более 50 тысяч человек умерло. Стандартизованный показатель заболеваемости составил 19,1 у мужчин и 4,0 у женщин, а общие затраты на лечение составили 4,9 млрд евро . Самые высокие показатели заболеваемости среди стран ЕС были зарегистрированы в Бельгии (31 у мужчин и 6,2 у женщин), а самые низкие в Финляндии (18,1 у мужчин и 4,3 у женщин). По прогнозам к 2030 году количество заболевших РМП может увеличиться до 219 тысяч.
Факторы риска рака мочевого пузыря
К предрасполагающим факторам относятся :
- Табакокурение. Это самый важный известный фактор риска рака мочевого пузыря. У курильщиков злокачественные опухоли мочевого пузыря развиваются в 4-7 раз чаще, в отличие от некурящих .
- Возраст. Шансы диагностировать рак мочевого пузыря увеличиваются с возрастом. 90 % людей с этим заболеванием старше 55 лет, а средний возраст людей с этим диагнозом — 73 года.
- Пол. У мужчин в 3-4 раза чаще развивается РМП, чем у женщин, но для женщин заболевание чаще становится смертельным .
- Раса. Показатели заболеваемости у белых мужчин в два раза выше, чем у чернокожих, и в восемь раз выше, чем у индейцев. Чернокожие вдвое чаще погибают от этого заболевания .
- Химические вещества. Некоторые промышленные и природные химические вещества, а также употребление хлорированной воды и содержащегося в воде мышьяка могут увеличить риск развития рака мочевого пузыря.
- Лекарственные препараты. Фенацетинсодержащие анальгетики повышают риск заболевания РМП в 2,0-6,5 раза при их постоянном применении .
- Хронические заболевания мочевого пузыря. Камни, инфекции мочевого пузыря, а также использование катетеров у парализованных людей могут увеличить риск развития рака мочевого пузыря.
- Водный режим. Исследования показывают противоречивые результаты: потребление большого количества жидкости, по-видимому, является фактором риска рака мочевого пузыря у мужчин и жителей Америки в Европе, но снижает вероятность развития этой патологии у жителей Азии .
- Циклофосфамид (Cytoxan, Clafen, Neosar). Люди, перенёсшие химиотерапию циклофосфамидом, имеют более высокий риск развития рака мочевого пузыря .
- Шистосомоз. Люди с некоторыми формами этой паразитарной болезни, которая встречается в некоторых частях Африки, Южной Америки, Юго-Восточной Азии и на Ближнем Востоке, с большей вероятностью имеют риск развития плоскоклеточного рака мочевого пузыря .
- Синдром Линча. Люди с синдромом Линча (ранее называемым наследственным неполипозным колоректальным раком, или HNPCC), могут иметь повышенный риск развития рака мочевого пузыря.
- Высококалорийное питание .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака мочевого пузыря
Злокачественные опухоли мочевого пузыря, как правило, сопровождаются отчётливой клинической симптоматикой. Однако иногда у людей с раком мочевого пузыря нет каких-либо изменений (бессимптомное течение) или причиной симптома может быть другое заболевание, которое не является раком .
Симптомы рака мочевого пузыря:
- кровь в моче (гематурия);
- частое и болезненное мочеиспускание;
- никтурия (частые ночные мочеиспускания);
- односторонние боли в пояснице;
- необъяснимая потеря аппетита и веса.
Односторонние боли в пояснице при раке мочевого пузыря
Симптомы рака мочевого пузыря у мужчин и женщин схожи. Как правило, первым признаком, позволяющим заподозрить заболевание, становится кровь в моче (встречается у 92 % больных с опухолями мочевого пузыря). Иногда в моче содержится небольшое незаметное количество крови (микроскопическая гематурия), которое можно определить только с помощью анализа мочи. Со временем емкость мочевого пузыря уменьшается, мочеиспускание становится более частым и болезненным, а гематурия — интенсивнее и продолжительнее. Появляется анемия.
Общий анализ мочи не используют для специфического диагноза рака мочевого пузыря, поскольку содержание крови в моче может быть признаком других, нераковых заболеваний, например инфекции или мочекаменной болезни.
В некоторых случаях появление первых симптомов рака мочевого пузыря становится признаком того, что раковые клетки уже распространились на другой орган. Тогда по симптоматике можно определить, куда именно распространилась опухоль: если на лёгкие, признаком может быть кашель или одышка, если в печень — боли в животе или желтуха, в кости — боли в костях или переломы.
Ведущими симптомами рака мочевого пузыря являются макрогематурия (кровь в моче, видимая невооружённым глазом) и дизурические расстройства (нарушение мочеиспускания: рези, боли и др.). Выраженность клинических проявлений определяется стадией заболевания.
Патогенез рака мочевого пузыря
Рак мочевого пузыря — генетически детерминированное заболевание. Превращение нормальной клетки в злокачественную — многостадийный и последовательный процесс. Он осуществляется при накоплении в геноме клетки достаточного количества повреждений в генах, которые контролируют клеточную пролиферацию (размножение), дифференцировку (обретение клеткой отличительных черт для исполнения в многоклеточном организме предназначенных ей функции), морфогенетические реакции и апоптоз (запрограммированную гибель клеток). При этом повреждаются не только отдельные составляющие регуляторных сетей, но и ключевые перекрёстные звенья нескольких сигнальных путей.
В результате накопления мутаций происходит нарушение нормального синтеза белков — белковый спектр опухоли значительно отличается от белкового спектра нормальной ткани. Злокачественный фенотип опухоли в конечном счёте определяется качественным и количественным изменением профиля белковых молекул, вовлечённых в канцерогенез .
Классификация и стадии развития рака мочевого пузыря
В Международной классификации болезней (МКБ-10) рак мочевого пузыря кодируется как C67 Злокачественное новообразование пузыря.
Тип рака мочевого пузыря зависит от того, какое он имеет клеточное строение и как выглядит под микроскопом. Различают 3 типа рака мочевого пузыря по типу клеток .
- Уротелиальная карцинома (in situ). Уротелиальная карцинома составляет около 90 % всех случаев РМП. Она возникает в уротелиальных клетках слизистой оболочки мочевого пузыря. Уротелиальная карцинома — это обобщающий термин, ранее использовалось другое название — переходно-клеточный рак.
- Плоскоклеточная карцинома (эпителиальное новообразование мочевого пузыря). Плоские клетки слизистого эпителия мочевого пузыря начинают усиленно делиться и активно развиваться в ответ на раздражение или воспаление. Со временем эти клетки могут стать раковыми. Плоскоклеточная карцинома составляет около 4 % от всех случаев рака мочевого пузыря.
- Аденокарцинома. Этот тип составляет около 2 % всех случаев рака мочевого пузыря и возникает из железистых клеток.
Существуют и другие менее распространённые типы рака мочевого пузыря, в том числе саркома, мелкоклеточная карцинома и др. Саркома начинается в жировых или мышечных слоях мочевого пузыря. Мелкоклеточная карцинома возникает из нейроэндокринных клеток.
Рак мочевого пузыря по наличию инвазии (проникновения):
- Неинвазивный рак мочевого пузыря, как правило, прорастает только в собственную пластинку слизистой оболочки.
- Мышечно-неинвазивный рак также можно назвать поверхностным раком, он не прорастает в более глубокие слои стенки мочевого пузыря, можно предположить, что этот тип рака не является серьёзным.
- Мышечно-инвазивный рак мочевого пузыря проникает в мышцы стенки мочевого пузыря, а иногда и в жировые слои или окружающие ткани за пределами мочевого пузыря.
Все варианты уротелиальных опухолей, описанных для мочевого пузыря, также могут встречаться в верхних мочевыводящих путях .
Классификация TNM
Одним из инструментов, которые используют врачи для описания рака, является система TNM. Используя различные диагностические тесты, врачи отвечают на ряд вопросов:
- T (tumor — опухоль). Насколько велика первичная опухоль, где она находится?
- N (nodus — узел). Опухоль распространяется на лимфатические узлы? Если да, то где и сколько?
- М (metastasis — метастазы). Рак метастазирует в другие части тела? Если да, то где и сколько?
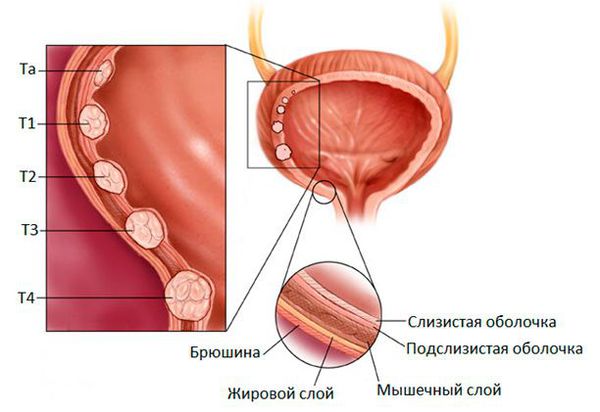
Стадирование рака мочевого пузыря
Полученные результаты объединяются для того, чтобы определить стадию рака индивидуально для каждого человека. В таблице представлена TNM классификация (Union Internationale Contre le Cancer, 2009), широко используемая врачами-урологами .

Классификация TNM
Группировка рака мочевого пузыря по стадиям:
| Стадия | Т | N | М |
|---|---|---|---|
| Стадия 0а | Та | N0 | М0 |
| Стадия 0is | 0is | N0 | М0 |
| Стадия I | Т1 | N0 | М0 |
| Стадия II | Т2а | N0 | М0 |
| Т2b | N0 | М0 | |
| Стадия III | Т3а | N0 | М0 |
| ТЗЬ | N0 | М0 | |
| Т4а | N0 | М0 | |
| Стадия IV | Т4b | N0 | М0 |
| Любая Т | N1,2,3 | М0 | |
| Любая Т | Любая N | Ml |
Согласно TNM классификации, в качестве регионарных лимфоузлов рассматриваются лимфоузлы ворот почки, парааортальные, паракавальные и внутритазовые лимфоузлы (для мочеточника). Сторона поражения не влияет на N-классификацию.
Для уротелиального рака согласно действующей системе Всемирной организации здравоохранения (ВОЗ, англ WHO) и Международного общества уропатоморфологов (ISUP) рекомендуется следующее разделение по степеням дифференцировки :
- LG — low-grade (высокая степень дифференцировки).
- HG — high-grade (низкая степень дифференцировки).
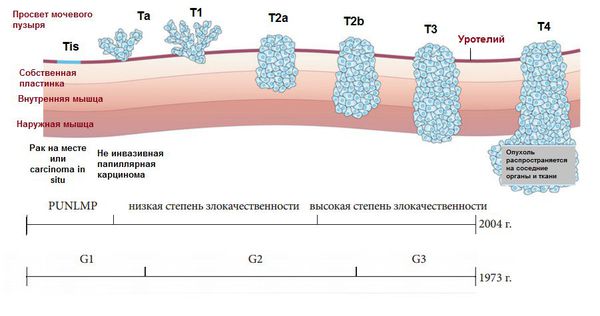
Стадирование и степень дифференцировки РМП
Согласно классификации ВОЗ/ISUP 2004 года, среди уротелиальных опухолей выделяют :
- папиллярную опухоль уротелия с низким злокачественным потенциалом (PUNLMP);
- папиллярный уротелиальный рак низкой степени злокачественности;
- папиллярный уротелиальный рак высокой степени злокачественности.
PUNLMP определяется как образование, которое не имеет цитологических признаков злокачественности, но нормальные клетки уротелия объединяются в папиллярные структуры.
Если опухоль мочевого пузыря распространилась на окружающие органы, такие как матка и влагалище у женщин, простата у мужчин и/или близлежащие мышцы, это называется местно-распространённым заболеванием. Рак мочевого пузыря также часто распространяется на лимфатические узлы в области таза. Если он распространился в печень, кости, лёгкие, лимфатические узлы вне таза или другие части тела, рак называется метастатическим заболеванием.
Европейская организация по исследованию и лечению рака (EORTC) предложила систему распределения больных раком мочевого пузыря на 3 группы риска и прогрессии: низкого, высокого и промежуточного.
При первичном обращении у 74,2 % больных выявляются опухоли в I-II стадии, и только у 25,8 % больных диагностируется инвазивный рак в III-IV стадии опухолевого процесса.
Осложнения рака мочевого пузыря
Локализация опухоли мочевого пузыря в области устья мочеточника может вызвать нарушение оттока мочи, что может сопровождаться приступами почечной колики либо тупой постоянной болью в области поясницы. Сдавление устья мочеточника — наиболее трагический признак заболевания, сопровождающийся функциональными изменениями почек.
Инвазивный рак мочевого пузыря в большинстве случаев осложняется пиелонефритом (воспалением ткани почек) и почечной недостаточностью. Инфицирование мочи проявляется клиникой вторичного цистита (в 51 % случаев). По мере нарастания стадии процесса частота цистита увеличивается.
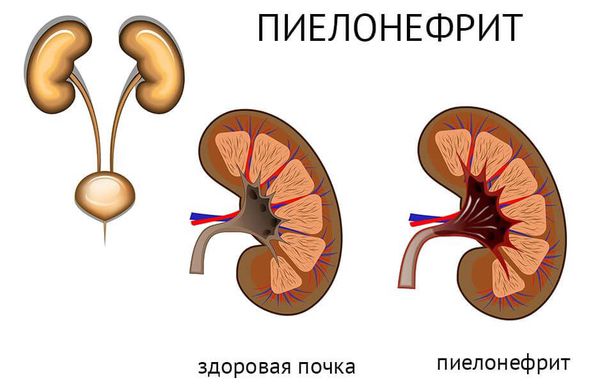
Пиелонефрит
Метастазы рака мочевого пузыря обнаруживаются в головном мозге, костной системе и лёгких. Гематурия может быть терминальной. Терминальной, или конечно, называют макрогематурию, которая при проведении трёхстаканной пробы видна только в последнем стакане, то есть после 150 миллилитров мочи, которые находятся в первых двух стаканах.
Наиболее часто встречающиеся осложнения рака мочевого пузыря:
- анемия;
- уретерогидронефроз;
- почечная недостаточность;
- инфекции;
- хроническая задержка мочеиспускания .
Диагностика рака мочевого пузыря
Предварительная клиническая стадия устанавливается по данным уретроцистоскопии (эндоскопического исследования мочевого пузыря и мочеиспускательного канала) или трансуретральной резекции (оперативного малоинвазивного вмешательства) с последующим гистопатологическим исследованием биопсийного материала.
Карциному in situ диагностируют по сочетанию цистоскопии, цитологического анализа мочи и гистологического исследования материала нескольких биопсий слизистой оболочки мочевого пузыря.
Компьютерная томография с урографией на сегодняшний день является методом выбора при обследовании пациентов с подозрением на рак мочевого пузыря. КТ заменила ультразвуковое исследование . Установлено, что чувствительность этого метода (способность давать правильный результат) в отношении мышечно-неинвазивного РМП находится в пределах от 67 до 100 %, а специфичность (способность не давать при отсутствии заболевания ложноположительных результатов) — в пределах от 93 до 99 % в зависимости от используемой методики и оборудования .
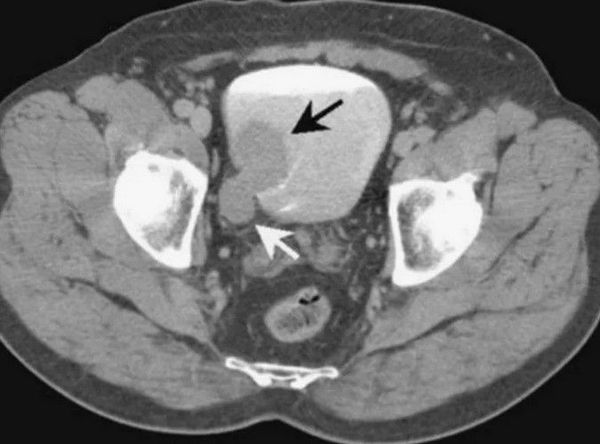
Рак мочевого пузыря на КТ
МСКТ-урография может выявить утолщение стенки почечной лоханки или мочеточников, являющееся признаком уротелиального рака верхних мочевыводящих путей, даже при отсутствии роста в просвет органа. Плоские опухоли таким образом выявить невозможно .
Цитологическое исследование осадка мочи наиболее информативный метод неинвазивной диагностики РМП с чувствительностью 80-90 % и специфичностью 98-100 %. Его проводят в дополнение к цистоскопии при выявлении злокачественных опухолей мочевого пузыря высокого риска рецидивирования (High grade) и прогрессирования .
В последнее время предложены и применяются различные методы лабораторной диагностики РМП:
- UroVysion;
- анализ на микросателлиты, иммуноциты/uCyt+ и цитокератины;
- определение ВТА (bladder tumor antigen), NMP 22 (nuclear matrix protein), антигена UBC (urinary bladder cancer), теломеразы мочи и др.
При специфичности 55-98 % чувствительность NMP 22 составила 47-100 %, BTA stat — 29-83 %, UBC — 64 %, проточной цитометрии — 61 %, UroVysion — 30-86 %, анализа на микросателлиты — 58-92 %, иммуноциты/uCyt+ — 50-100 %, цитокератинов — 12-88 %.
Трансабдоминальное УЗИ почек и мочевого пузыря может использоваться в ходе первичного обследования пациентов с гематурией, согласно рекомендациям Европейской ассоциации урологов (EAU) 2013 и 2016 года . Однако следует помнить, что оно не может заменить компьютерную томографию с урографией для диагностики уротелиальной карциномы верхних отделов мочевых путей из-за низкой чувствительности метода . Чувствительность ультразвукового исследования при определении стадии опухолевого процесса составляет 80,6 % при Т1 стадии, 91,2 % при Т2 стадии и 93,3 % при Т3-4.
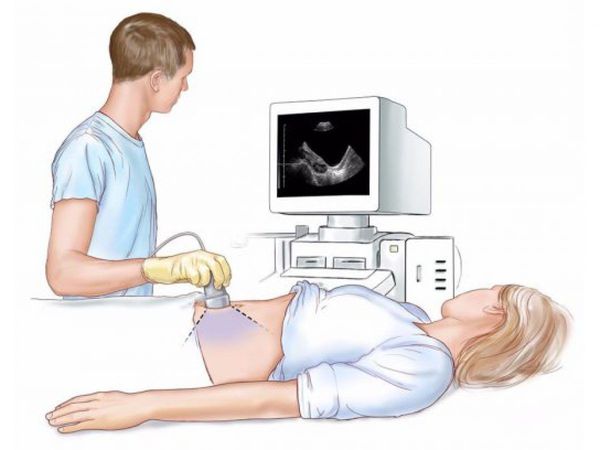
Трансабдоминальное УЗИ мочевого пузыря
Цветное допплеровское ультразвуковое исследование обладает хорошей чувствительностью, но плохой специфичностью для диагностики низкодифференцированных опухолей мочевого пузыря .
Уретероцистоскопия/трансуретральная резекция опухолей мочевого пузыря в «белом свете» в настоящее время по-прежнему являются наиболее широко используемыми и доминирующими инвазивными методами обнаружения опухолей мочевого пузыря и остаются достаточно надёжными для определения стадии и степени дифференцировки опухоли: позволяют установить размеры, количество, локализацию опухоли мочевого пузыря .
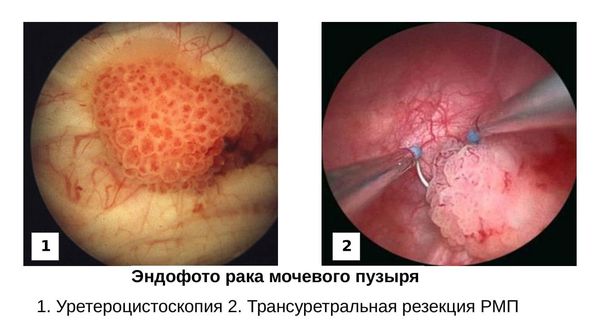
Эндофото рака мочевого пузыря
Более ценным методом в отношении диагностики РМП в рутинной клинической практике, чем традиционная уретероцистоскопия в «белом свете» является узкоспектровая (узкополостная) цистоскопия, её специфичность составляет 67,4 %, а чувствительность приближается к 93,3 % . Узкоспектровое (NBI — narrow band imaging) изображение является новой медицинской технологией.
Современные технологии визуализации РМП классифицируются на основе макроскопического, микроскопического и молекулярного полей зрения . Макроскопические техники, такие как фотодинамическая цистоскопия и узкополосная визуализация, схожи с цистоскопией в «белом свете», однако способны визуализировать даже самые незначительные поражения слизистой оболочки мочевого пузыря благодаря использованию повышенной контрастности.
Микроскопические техники, такие как оптическая когерентная томография и конфокальная лазерная эндомикроскопия, позволяют получать в высоком разрешении изображения везикулярных тканей в разрезе, которые очень схожи с изображениями, получаемыми при гистопатологических исследованиях . Поэтому подобные исследования часто называют «оптической биопсией». Совмещая все эти методы, урологи могут получать в реальном времени высокоспецифичные изображения раковых клеток и дифференцировать их от здоровых.
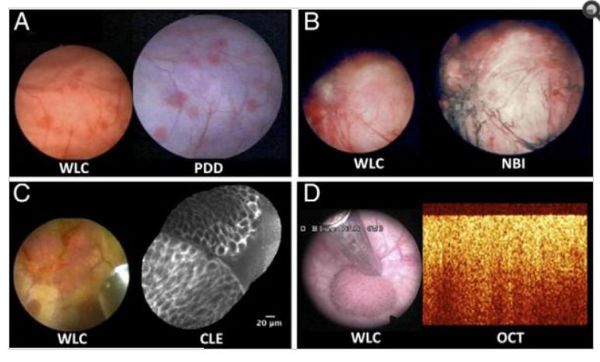
Современные технологии оптической визуализации РМП
На фото представлены современные технологии оптической визуализации рака мочевого пузыря .
- А — WLC-цистоскопия в «белом свете» и PDD — фотодинамическая диагностика;
- B — WLC-цистоскопия в «белом свете» и NBI — флуоресцентная цистоскопия;
- C — WLC-цистоскопия в «белом свете» и CLE — конфокальная лазерная эндомикроскопия;
- D — WLC-цистоскопия в «белом свете» и OCT — оптическая когерентная томография.
Из этих четырёх технологий цистоскопии в «белом свете» конфокальная лазерная эндомикроскопия имеет наивысшее разрешение (от 2 до 5 мкм) и может обеспечить оптическую биопсию, выявив микроархитектуру и клеточную морфологию предполагаемых поражений .
Лечение рака мочевого пузыря
Главным методом лечения большинства больных злокачественными новообразованиями мочевого пузыря остаётся оперативное вмешательство. Хирургический метод признан основным в лечении больных раком мочевого пузыря во всём мире.
С клинической точки зрения в выборе лечения играет значимую роль подразделение рака мочевого пузыря на неинвазивный, или мышечно-неинвазивный, и мышечно-инвазивный. Развитие мышечно-неинвазивного РМП (Tis, Ta, T1) трудно предугадать. Два основных фактора определяют судьбу пациента с этим типом рака: рецидивирование и прогрессирование заболевания. Мышечно-неинвазивный рак мочевого пузыря имеет непредсказуемое течение и обладает опасностью быстрого рецидивирования. В 40-80 % случаев после трансуретральной резекции (ТУР) в течение 6-12 месяцев развивается рецидив, а у 10-25 % больных — инвазивный рак. С каждым новым рецидивом вероятность сохранить мочевой пузырь уменьшается.
Лечение мышечно-неинвазивного рака мочевого пузыря
Принципиальная стратегия лечения мышечно-неинвазивного рака мочевого пузыря основывается на радикальном удалении опухоли, предотвращении рецидивирования, метастазирования и перерождения в инвазивные формы рака.
Существуют различные виды органосохраняющего хирургического лечения РМП:
- трансвезикальная резекция мочевого пузыря (резекция опухоли через разрез в стенке пузыря);
- ТУР — трансуретральная резекция;
- ТУР-вапоризация — разновидность электрохирургического лечения, объединяющая в себе преимущества резекции и «выпаривания» ткани.
С появлением современных эндоскопических методик для хирургического лечения мышечно-неинвазивных опухолей мочевого пузыря метод трансвезикальной резекции стал редким вмешательством.
Согласно современным рекомендациям Европейской ассоциации урологов (2017), признанным стандартом хирургического органосохранного лечения пациентов с мышечно-неинвазивным РМП считается проведение первичной лечебно-диагностической трансуретральной резекции мочевого пузыря (ТУР МП) . Целями вмешательства являются: верификация диагноза и стадирование опухоли (определение категории Т и степени дифференцировки опухоли), определение возможных рисков рецидивирования и прогрессии на основании полученных морфологических данных (количество опухолевых очагов, их диаметр, наличие сопутствующей карциномы in situ) и удаление видимых новообразований.
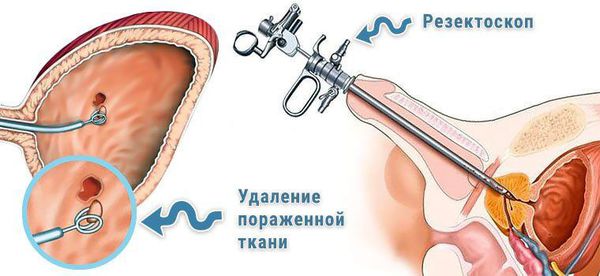
Трансуретральная резекция мочевого пузыря
Химиотерапия при раке мочевого пузыря. После выполнения ТУР МП всем больным проводится однократная ранняя (в течение 6 часов) инстилляция (капельное введение) химиопрепарата в мочевой пузырь (препарат выбирает врач). Было доказано, что это уменьшает частоту рецидивов. Основная цель внутрипузырной лекарственной терапии опухолей мочевого пузыря состоит в максимальном воздействии лекарственного препарата на остатки опухоли (раковые клетки).
Дальнейшее лечение после ТУР МП и однократной инстилляции химиопрепарата зависит от результатов гистологического исследования и группы риска, к которой относится пациент.
Лечение после ТУР МП и ранней однократной инстилляции химиопрепарата:
- В группе низкого риска: дальнейшее лечение может не проводиться, поскольку вероятность рецидива и прогрессии незначительна.
- В группе высокого риска: адъювантная (вспомогательная) внутрипузырная иммунотерапия вакциной против туберкулёза — БЦЖ (в полной дозе) с поддерживающей терапией в течение 1-3 лет. При высочайшем риске прогрессии опухоли или неэффективности БЦЖ-терапии показана цистэктомия (удаление мочевого пузыря или его части).
- В группе промежуточного риска: адъювантная внутрипузырная химиотерапия (препарат выбирается врачом) продолжительностью не более 1 года или адъювантная внутрипузырная иммунотерапия вакциной БЦЖ (в полной дозе) с поддерживающей терапией 1 год.
Внутрипузырная пострезекционная лекарственная химио- или иммунотерапия является вторым после ТУР методом лечения мышечно-неинвазивного РМП. Внутрипузырную лекарственную терапию подразделяют на профилактическую, проводимую для предотвращения возникновения рецидивов после удаления всех видимых опухолей, и лечебную, проводимую с целью уничтожения остаточных, частично резецированных и неудалённых опухолей
По виду используемого агента внутрипузырную терапию делят на химиотерапию (ХТ) и иммунотерапию (ИТ). Они отличаются по механизму действия используемых препаратов, показаниям, продолжительности лечения и эффективности. 35 различных лекарственных веществ, включая цитостатики, иммуномодуляторы и витамины, были использованы с адъювантной целью при Та, Т1 стадии рака мочевого пузыря, и лишь некоторые из них оказались эффективными.
По рекомендуемым для внутрипузырной терапии химиотерапевтическим агентам (включая митомицин C, доксорубицин, эпирубицин, гемцитабин, вальрубицин, пирарубицин и тиотепа) в настоящее время нет единого мнения относительно того, какой препарат способствует лучшим онкологическим результатам .
Лечение мышечно-инвазивного рака мочевого пузыря
Мышечно-инвазивный РМП — потенциально смертельное заболевание, так как без лечения больные погибают в течение 24 месяцев. Основным единственно радикальным методом лечения мышечно-инвазивного РМП (Т2-Т4а, N0, М0) является радикальная цистэктомия — удаление вместе с мочевым пузырем у мужчин предстательной железы с семенными пузырьками и покрывающей брюшиной, а у женщин — матки, придатков, фаллопиевых труб, уретры, передней стенки влагалища. Следует отметить, что цистэктомия является органоуносящим методом хирургического лечения, при котором качество жизни пациента заметно ухудшается. Неотъемлемой частью цистэктомии является удаление лимфатических узлов.
Радикальная цистэктомия показана также при невозможности проведения органосохранного лечения мышечно-неинвазивного РМП, неблагоприятного прогноза и его рецидивов . Согласно рекомендациям Национальной сети по борьбе с раком (NCCN) от 2017 года и Европейской ассоциации урологов (EAU) от 2017 года, такой объём вмешательства при мышечно-неинвазивном РМП показан лишь в следующих ситуациях: при отсутствии ответа на иммунотерапию вакциной БЦЖ после проведённой ТУР, при рецидиве опухоли (при цитологически подтверждённом диагнозе) .
В настоящее время широко используются лапароскопические методики и появилась возможность выполнения цистэктомии с помощью робот-ассистированной техники. Для сохранения сексуальной функции у мужчин выполняют нервосберегающую цистэктомию с сохранением кавернозных сосудисто-нервных пучков .
Неотъемлемой частью радикальной цистэктомии является восстановление резервуарной функции мочевого пузыря.
Радикальная цистэктомия обеспечивает 5-летнюю выживаемость только у 50 % больных. В связи с этим, начиная с 1980-х годов, для улучшения подобных неудовлетворительных результатов используют дооперационную химиотерапию. Применение неоадъювантной цисплатинсодержащей комбинированной ХТ способствует улучшению общей 5-летней выживаемости на 5-8 % .
Цистэктомия спасения показана больным, у которых неэффективна консервативная терапия, при рецидивах после лечения с сохранением мочевого пузыря, при наличии непереходно-клеточных опухолей и только с паллиативной целью .
Выполнение только ТУР при мышечно-инвазивном РМП не относится к радикальному лечению .
Дистанционная лучевая терапия может служить альтернативным методом лечения для пациентов с противопоказаниями к выполнению радикальной операции .
Прогноз. Профилактика
Чем позже пациент обращается за медицинской помощью, тем ниже показатель выживаемости и больше вероятность рецидивирования.
Всем пациентам с опухолями стадии Та, Т1 и с карциномой in situ следует обязательно провести первую цистоскопию 3 месяца спустя после ТУР. Из-за риска рецидива и прогрессирования больные с опухолями на этих стадиях должны проходить регулярное обследование согласно протоколу. Регулярные (ежегодные) визуализации верхних мочевыводящих путей (КТ-внутривенная урография или внутривенная урография) рекомендуются в случае опухолей высокого риска.
Профилактика:
- Отказ от активного и пассивного курения.
- Соблюдение водно-питьевой режим. Согласно исследованию, рекомендуется ограничение употребления жидкости до 3000 мл в день для людей, живущих в Америке, и до 2000 мл в день для мужчин из Европы .
- Устранение профессиональных вредностей (контакта с химикатами). Рабочие должны быть проинформированы о возможном канцерогенном эффекте различных веществ, длительности воздействия и латентном периоде развития РМП.
- Своевременное лечение воспалительных заболеваний мочевого пузыря.
Список литературы
- Каприн А. Д. Злокачественные новообразования в России в 2016 году (заболеваемость и смертность) [Текст] / А. Д. Каприн, В. В. Старинский, Г. В. Петрова. — М.: ФГБУ «МНИОИ им. П.А. Герцена» Минздрава России, 2018. — 250 с.
- Рак мочевого пузыря (классика и новации) [Текст]: монография / Алексеев Б. Я. и др.; под редакцией М. И. Коган. — М.: Медфорум, 2017. — 262 с.
- Трушин, А. А. Возможности оптической диагностики мышечно-неинвазивного рака мочевого пузыря [Текст] / А. А. Трушин, Е. В. Филоненко, И. Г. Русаков // Медицинский совет — 2017. — № 6. — С. 110-116.
- Babjuk M. EAU Guidelines on Non–Muscle-invasive Urothelial Carcinoma of the Bladder: Update 2016 [Text] / M. Babjuk // Eur. Urol. — 2017; 71: 447-461.ссылка
- Liu J-J. New optical imaging technologies for bladder cancer: considerations and perspectives [Text] / J-J Liu [et al.] // The Journal of urology. — 2012; 188 (2): 361-368.ссылка
- Sylvester R. J. Systematic review and individual patient data meta-analysis of randomized trials comparing a single immediate instillation of chemotherapy after transurethral resection with transurethral resection alone in patients with stage pTa–pT1 urothelial carcinoma of the bladder: which patients benefit from the instillation? (2016) [Text] / R. J. Sylvester [et al.] // European Urology. — 2016; 69(2): 231-244.ссылка
- Tan W. S. Management of non-muscle invasive bladder cancer: A comprehensive analysis of guidelines from the United States / W. S. Tan [et al.] // Europe and Asia Cancer Treatment Reviews. — 2016; 47: 22–31.ссылка
- Witjes A. J. Updated 2016 EAU Guidelines on Muscle-invasive and Metastatic Bladder Cancer [Text] / Witjes A. J. // European Urology. — 2017; 71 (3): 462-475.ссылка
- Smoking and Bladder Cancer // National Institutes of Health. — 2011.
- The impact of gender on oncologic outcomes of bladder cancer / Dong-Ho Mun, Shoji Kimura, Shahrokh F Shariat, Mohammad Abufaraj // Curr Opin Urol. — 2019; 29(3): 279-285.ссылка
- Racial and Socioeconomic Disparities in Bladder Cancer Survival: Analysis of the California Cancer Registry / John M Sung, Jeremy W Martin, Francis A Jefferson, Daniel A Sidhom // Clin Genitourin Cancer. — 2019; 17(5): e995-e1002. ссылка
- Analgesic and anti-inflammatory drug use and risk of bladder cancer: a population based case control study / Joan Fortuny, Manolis Kogevinas, Michael S Zens, Alan Schned // BMC Urol. — 2007; 7: 13.ссылка
- Total fluid consumption and risk of bladder cancer: a meta-analysis with updated data / Qinyu Liu, Banghua Liao, Ye Tian, Yuntian Chen, Deyi Luo // Oncotarget. — 2017; 8(33): 55467-55477.ссылка
- Cyclophosphamide associated bladder cancer—a highly aggressive disease: analysis of 12 cases / E. T. Fernandes, J. C. Manivel, P. K. Reddy, C. J. Ercole // J Urol. — 1996; 156(6): 1931-1933.ссылка
- Understanding Urogenital Schistosomiasis-Related Bladder Cancer: An Update / Kenji Ishida, Michael H. Hsieh // Front Med (Lausanne). — 2018; 5: 223.ссылка
- Overview. Bladder cancer // NHS. — 2018.
- Лыжко Н.А. Молекулярно-генетические механизмы инициации, промоции и прогрессии опухолей // Российский биотерапевтический журнал. — 2017. — Т. 16, № 16. — С. 7-17.