Миастения — это прогрессирующее аутоиммунное заболевание, при котором наблюдаются кратковременные эпизоды слабости и утомляемости в различных мышцах. Оно также известно под названием «миастения гравис» и «болезнь Эрба — Гольдфлама» (в честь учёных, внёсших большой вклад в изучение патологии) . Чаще всего начало заболевания проявляется двоением в глазах, затруднением при жевании и глотании, к вечеру больному становится трудно держать глаза открытыми.
Считается, что эта болезнь впервые была описана британским учёным-медиком Томасом Уиллисом в 1672 году, а первое доказательство её аутоиммунной природы появилось спустя более 200 лет.
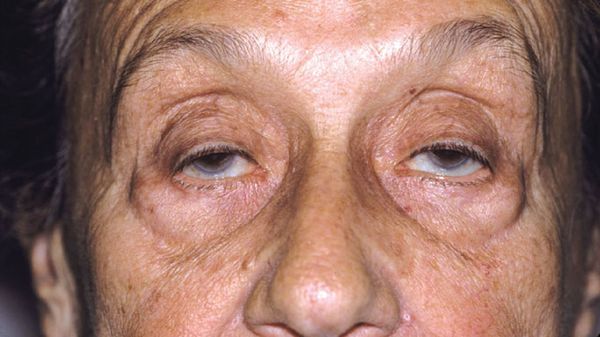
Проявление миастении
Миастения — это хроническое аутоиммунное заболевание с прогрессирующим течением. Оно связано с разрушением рецепторов, которые участвуют в передаче нервных импульсов. При миастении эти рецепторы атакуются антителами, в результате чего нервно-мышечная передача нарушается.
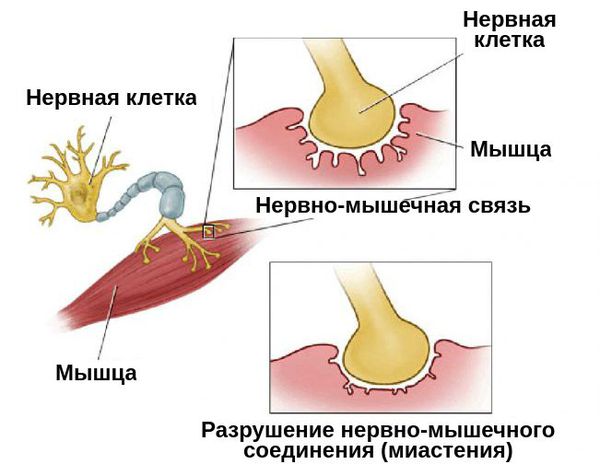
Разрушение нервно-мышечной связи
Причина образования антител не известна. Ею могут стать как стресс, перенесённые вирусные заболевания или проблемы с эндокринной системой, так и совокупность других факторов. Миастению связывают с аутоиммунными нарушениями: ревматоидным артритом, В12-дефицитной анемией и системной красной волчанкой .
Также причиной миастении может стать патология тимуса (вилочковой железы) — главного органа иммунной системы. В частности её развитие может быть связано с тимомой — группой опухолей вилочковой железы. В 30 % случаях они являются злокачественными.
Распространённость миастении составляет 10 случаев болезни на 100 тысяч человек. Чаще всего ею страдают мужчины и женщины 20-40 лет. Однако другие возрастные группы также не защищены от этого заболевания: оно может развиться как в раннем детстве, так и в глубокой старости. В целом среди заболевших количество женщин в три раза больше, чем мужчин (причина этого до конца не выяснена). Среди беременных миастения встречается в одном из 20 тысяч случаев .
Провоцирующими факторами развития миастении являются:
- вирусные заболевания;
- беременность и роды;
- стресс;
- чрезмерные физические нагрузки;
- травмы;
- аллергические реакции (конъюнктивит, атопический дерматит);
- приём некоторых лекарств (например, антибиотиков), особенно при заболеваниях почек .
Благодаря непрерывному изучению заболевания, современным методам диагностики и лечения около 80 % пациентов достигают полной или неполной ремиссии, а летальность составляет менее 1 % . Но несмотря на это миастения остаётся серьёзным заболеванием, требующим пристального наблюдения и соблюдения всех предписаний врача.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы миастении
В клинической картине миастении преобладают: двоение в глазах, опущение век, утомление мышц челюстно-лицевой мускулатуры при длительном пережёвывании пищи. Также может возникнуть слабость в руках и ногах, кашель после глотания и охриплость голоса. Все эти признаки болезни появляются после нагрузки на соответствующие мышцы, чаще во второй половине дня, и становятся менее выраженными после отдыха или охлаждения задействованных мышц .
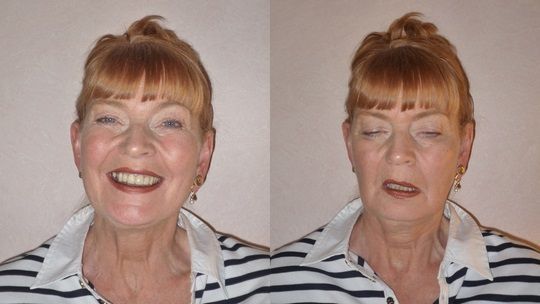
Пациент с миастенией: состояние мимической мускулатуры в начале дня (слева) и вечером (справа)
В целом симптомы миастении яркие и многообразные. Они зависят от формы патологии:
- Доброкачественная миастения характеризуется попёрхиванием во время еды и офтальмоплегией — полной неподвижностью глазных яблок.
- При семейной детской миастении попёрхивание во время еды усиливается и становится резко выраженным, из-за чего пациенту трудно глотать. В связи со слабостью дыхательных мышц затрудняется дыхание.
- Юношеская миастения проявляется опущением век, обездвиженностью глазных яблок, попёрхиванием при приёме пищи и, затем, нарушением глотания. У больных развивается слабость всех мышц, у 40 % — дыхательные нарушения.
- Генерализованная (распространённая) миастения проявляется расстройствами глотания, слабостью туловищной мускулатуры и дыхательными нарушениями.
- Глазная миастения отличается поражением только мышц глаз и век.
- Бульбарная миастения возникает при синдроме поражения определённых черепных нервов. Она проявляется гнусавостью голоса, попёрхиванием во время еды и невнятностью речи.
- Краниальная миастения сопровождается поражением некоторых черепно-мозговых нервов, в том числе глазодвигательных. Также в результате вовлечения мимических мышц и жевательной мускулатуры развивается нарушение речи.
Патогенез миастении
Патогенез миастении до конца не выяснен. Но известно, что в развитии патологической утомляемости мышц главную роль играют аутоантитела. Они блокируют постсинаптические холинергические рецепторы нервно-мышечных соединений. В результате этой блокады развиваются структурные изменения и часть рецепторов гибнет.
Вероятно, это связано с патологической активностью фермента ацетилхолинэстеразы. Он ускоряет разложение ацетилхолина, который участвует в передаче нервного импульса и мышечном сокращении. В результате данный нейромедиатор быстро разрушается, что приводит к патологической мышечной утомляемости .
Также на развитие миастении влияет вилочковая железа. При нарушении её функции в организме начинают синтезироваться антитела к холинергическим рецепторам, что в дальнейшем ведёт к развитию миастении.
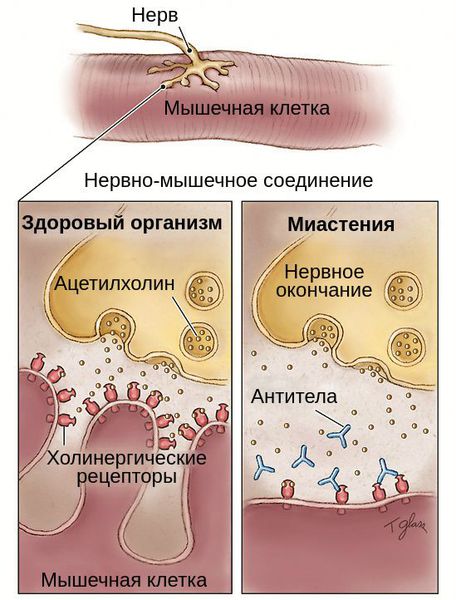
Нарушение нервно-мышечной связи
Имеются данные о возможной роли персистирующей (постоянной хронической) инфекции вилочковой железы. Например, при миастении выявлено повышение титра комплемент-связывающих антител к цитомегаловирусу. У больных, которым проводилось лечение стероидами или тимэктомия (операция по удалению вилочковой железы), этот признак отсутствовал.
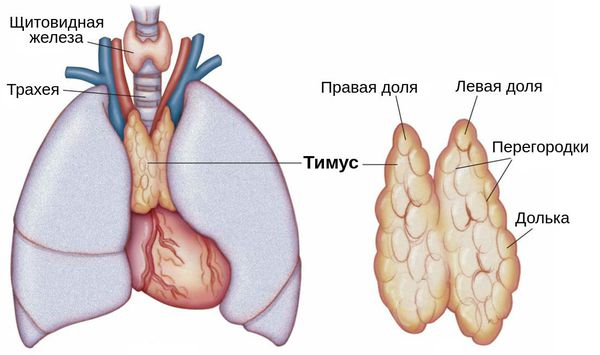
Вилочковая железа (тимус)
Ко всему прочему, при миастении может идти речь о генетически детерминированном или приобретённом дефекте иммунологического ответа .
Классификация и стадии развития миастении
Миастения делится на генерализованные и локальные формы.
К локальным формам относятся:
- Глазная форма — сопровождается двоением в глазах, косоглазием, плохой фокусировкой взгляда, опущением верхних век с двух сторон. Не опасна для жизни, приводит к умеренной инвалидизации. Без лечения в течение года может перерасти в генерализованную миастению .
- Бульбарная форма — проявляется гнусавостью голоса и невнятностью речи, попёрхиванием твёрдой пищей и попаданием жидкости в нос .
- Краниальная форма — проявляется невнятностью речи, вялостью мимики и жевательными нарушениями
К генерализованным формам относятся:
- Миастения новорождённых (или неонатальная миастения) — временная форма заболевания, возникает у некоторых детей, рождённых от матерей с миастенией. Как правило, симптомы проходят спустя несколько недель или месяцев после рождения .
- Врождённая миастения — крайне редкая форма болезни. Обычно симптомы возникают сразу после рождения и сохраняются на всю жизнь . Выделяют два типа такой формы болезни:
- доброкачественную с частичным или полным ограничением подвижности глазных яблок (офтальмопарезом или офтальмоплегией);
- семейную детскую — сопровождается опущением век, нарушением глотания и дыхания, которые сохраняются годами, глазодвигательные функции в норме .
- Юношеская миастения (или ювенильная миастения) — в большинстве случаев (75 %) проявляется после 10 лет, редко — после первого года жизни ребёнка . В отличие от других форм болезни, птозу век может сопутствовать косоглазие, офтальмоплегия и подёргивание век . У детей 2-10 лет данная форма может развиваться остро и молниеносно. Без своевременной диагностики и тщательного лечения прогноз неблагоприятный: при поражении дыхательных мышц может возникнуть удушье и аспирация, требуется поддержка дыхания .
- Генерализованная миастения взрослых.
Последнюю форму генерализованной миастении можно разделить по стадиям:
- лёгкая;
- умеренная;
- тяжёлая;
- острая молниеносная;
- поздняя тяжёлая;
- с ранним развитием мышечных атрофий.
Также миастению можно разделить по характеру течения. Выделяют:
- миастенические эпизоды — характерно быстрое регрессирование, промежуток между эпизодами может составлять от нескольких месяцев до 10 лет;
- миастеничекое состояние — проявляется развитием симптоматики в течение нескольких месяцев с последующей длительной стабилизацией процесса;
- прогрессирующая миастения — несмотря на своё название, развивается и прогрессирует достаточно медленно, через какое-то время возможна стабилизация состояния;
- злокачественная форма миастении — является наиболее тяжёлой, характеризуется быстрым вовлечением всё новых и новых мышц, что приводит к утяжелению состояния .
Осложнения миастении
Как было описано выше, важную роль в развитии миастении играет нейромедиатор ацетилхолин. Его недостаток приводит к нарушению работы дыхательных мышц. В результате может резко нарушиться дыхание, вплоть до его остановки.
К наиболее значимым осложнениям миастении относятся холинергический и миастенический криз.
Холинергический криз вызывает передозировка антихолинэстеразными препаратами или внезапное повышение чувствительности к ним (например, при операции или рентген-облучении). В клинической картине наряду с нарушениями глотания, речи и дыхания, поражением мимических и жевательных мышц, а также мышц плечевого пояса наблюдается повышенное слюноотделение, потливость, боли в животе, жидкий стул, рвота и учащённое мочеиспускание. При осмотре отмечается сужение зрачков, редкий пульс и пониженное давление .
Миастенический криз проявляется развитием тетрапареза (т. е. выраженной слабостью в руках и ногах, невозможностью долго держать их на весу) или слабостью дыхательных мышц, которая угрожает жизни. Такое осложнение развивается примерно у 15-20 % пациентов с генерализованной миастенией .
Чаще всего причинами возникновения миастенического криза становятся:
- патология органов дыхания, в том числе ОРВИ с поражением верхних отделов респираторного тракта;
- аспирационная пневмония;
- сепсис;
- оперативные вмешательства, которые выполняются под общей анестезией (особенно тимэктомия).
Отдельно стоит сказать о тимоме, при которой риск миастенического криза увеличивается в два раза.
Также существует ряд лекарственных препаратов, провоцирующих развитие осложнений миастении. К ним относятся:
- бензодиазепины;
- антидепрессанты;
- препараты, нормализующие мышечный тонус;
- антибиотики (аминогликозиды, макролиды, тетрациклины);
- препараты, содержащие йод и магний;
- нарушение схемы приёма кортикостероидов и антихолинэстеразных препаратов.
Особенное внимание при подозрении на миастению следует уделять жалобам ребёнка, так как он не всегда может правильно сформулировать их. Это приводит к поздней диагностике заболевания и нарушению дыхания.
Диагностика миастении
Диагностика миастении начинается со сбора жалоб. Больные жалуются на опущение век и двоение в глазах, в дальнейшем появляется слабость в мышцах ног и рук, возможна гнусавость голоса, проблемы с глотанием, попёрхивание во время еды, слабость жевательных мышц. В тяжёлых случаях наблюдаются дыхательные расстройства.
При сборе анамнеза (истории болезни) следует обращать внимание:
- было ли у родственников такое же заболевание;
- возникали ли у пациента ощущения быстро преходящей слабости и утомляемости, которая частично или полностью проходила самостоятельно или на фоне приёма неспецифических препаратов — противосудорожных, нейролептиков, некоторых гормонов (в т. ч. оральных контрацептивов), антибиотиков «мицинового» ряда, миорелаксантов и др.
- сопровождалась ли преходящая слабость и утомляемость двоением в глазах, опущением век, попёрхиванием во время еды или слабостью мышц туловища.
При физикальном обследовании необходимо обращать внимание на птоз век, бульбарные расстройства (проблемы, связанные с глотанием пищи) и быструю мышечную утомляемость во время и после физической нагрузки.
Так как в большинстве случаев патогенез миастении связан с выработкой антител к холинергическим рецепторам, для подтверждения клинического диагноза достаточно выполнить иммунологический тест — анализ крови на наличие антител. В случае отрицательного результата могут потребоваться дополнительные методы диагностики.
Для исключения других заболеваний возможно проведение КТ и МРТ переднего средостения . В более редких случаях применяется исследование биоптата мышц.
Наиболее современным и решающим методом диагностики при подозрении на миастению является электронейромиография (ЭНМГ) с проведением декремент-теста (исследования нервно-мышечной передачи). Для выполнения теста на области поражённых мышц фиксируются специальные электроды, через которые к мышцам ритмично поступают электрические импульсы. Получаемые мышечные ответы отображаются на нейромиографе в виде графика амплитуд.
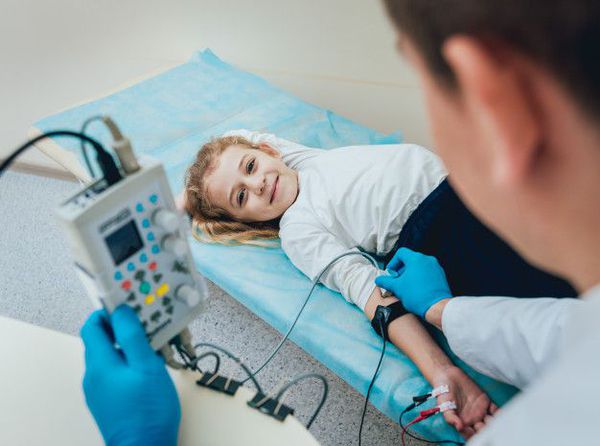
Электронейромиография
Заподозрить миастению позволяет постепенное снижение амплитуд мышечной реакции более чем на 10 % от изначального мышечного ответа. Чтобы убедиться в диагнозе, после текста пациенту подкожно вводят прозерин 0,05 % и снова выполняют тестирование. В случае миастении данный препарат временно устранит нарушение нервно-мышечной передачи, тем самым увеличит амплитуду мышечных ответов.
Дифференциальная диагностика
Миастению необходимо отличать от следующих заболеваний:
- гиперплазия (увеличение) вилочковой железы;
- тимома;
- заболевания щитовидной железы;
- системные заболевания соединительной ткани;
- болезни крови;
- кожные заболевания (витилиго или пузырчатка);
- рассеянный склероз;
- саркоидоз;
- язвенный колит .
Клиническая картина тимомы варьирует от бессимптомного течения до миастении с выраженными симптомами. Помимо слабости и утомляемости мышц для неё характерен кашель, боль в области груди и одышка . Чтобы исключить её, необходимо провести КТ или МРТ переднего средостения.
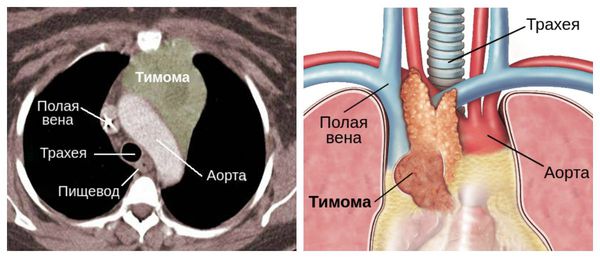
Тимома
Миастенические синдромы также возникают при:
- паранеопластических процессах (миастеническом синдроме Ламберта — Итона);
- ботулизме;
- поли- и дерматомиозите;
- семейном прогрессирующем бульбарном параличе;
- гипотиреоидной миопатии;
- боковом амиотрофическом склерозе .
Особое внимание следует уделять дифференциальной диагностике между холинергическим и миастеническим кризом. Первый тип криза встречается всего лишь у 3 % больных и начинается медленнее, чем миастенический криз. Он всегда связан с передозировкой антихолинэстеразными препаратами. В течение суток или более у пациента нарастает слабость и утомляемость, он не выдерживает прежнего интервала между приёмами данных средств, мышечная сила в ответ на стандартную или увеличенную дозу препарата снижается даже без предшествующей физической нагрузки.
Важное диагностическое значение при определении типа криза имеет прозериновая проба: пациенту подкожно вводят 2 мл 0,05 % прозерина. В течение 30 минут после введения препарата при холинергическом кризе отмечается уменьшение мышечной слабости, тогда как при миастеническом кризе мышечная сила увеличивается.
Лечение миастении
Методы лечения миастении делятся на две группы:
- консервативные — медикаментозное лечение, плазмаферез, радиотерапия и энтеросорбция;
- оперативные — удаление вилочковой железы (тимэктомия).
К средствам медикаментозного лечения относятся: антихолинэстеразные препараты, анаболические стероиды, АКТГ (адренокортикотропный гормон) и кортикостероиды. Как правило, применяется только один препарат, так как использование нескольких средств чревато холинергическим кризом.
Антихолинэстеразные препараты способствуют накоплению ацетилхолина в синапсах (так как препятствуют разрушению нейромедиатора), в результате нарастает мышечная сила . Их вводят внутримышечно, а также принимают в форме таблеток. Доза препарата подбирается индивидуально.
Анаболические стероиды вводят внутримышечно. Они снижают риск генерализации заболевания, показаны при непереносимости других способов консервативной терапии, а также при наличии противопоказаний к тимэктомии . Препаратом выбора является Ретаболил.
АКТГ стимулируют выработку кортикостероидов надпочечниками, которые обладают противовоспалительным и иммуномодулирующим действием . Их применяют внутривенно или внутримышечно. Более эффективными для лечения миастении считаются глюкокортикоиды (например, Преднизолон). Их использование требует значительного уменьшения дозировки антихолинэстеразных препаратов во избежании холинергического криза.
Длительный приём стероидов повышает риск развития остеопороза. В связи с этим рекомендуется рентгенографию грудной клетки .
Иммунодепрессанты искусственно подавляют иммунитет для снижения выработки антител . Они являются препаратом выбора у пожилых людей с острой формой миастении, а также при лечении больных с неоперабельными тимомами, противопоказаниях к хирургическому лечению, неэффективности ацетилхолинэстеразных препаратов и кортикостероидов .
При лечении больных с тяжёлой генерализованной миастенией проводится плазмаферез — забор и очистка крови с возвращением её или какой то её части обратно в кровоток. Такая процедура позволяет уменьшить количество антител к холинергическим рецепторам в кровяном русле. Её рекомендуют проводить перед тимэктомией .
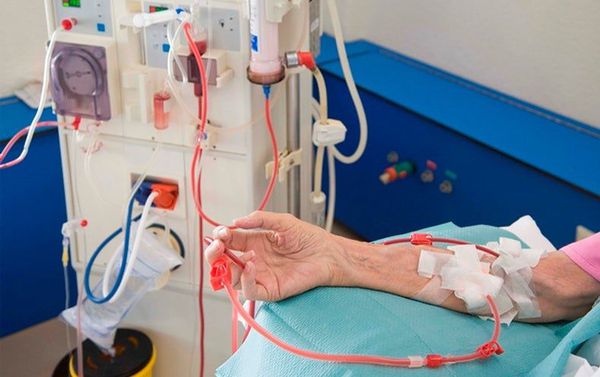
Плазмаферез
Для лечения миастении также применяется внутривенное ведение иммуноглобулинов G 5 % и 10 %. Они быстро, но временно улучшают течение заболевания. Так как использование высоких доз человеческих иммуноглобулинов способно подавлять иммунные процессы, иммуноглобулины G позволяют снижать выработку антител к холинергическим рецепторам.
При выявлении у пациента цитомегаловируса или вируса Эпштейна — Барр рекомендовано применение специфических иммуноглобулинов к герпетическим вирусам .
Также эффективным методом лечения миастении может быть энтеросорбция. Она предполагает приём лекарственных средств, например волокнистого угольного сорбента, для удаления аутоантител. Наиболее эффективна при комплексном лечении миастении средней степени тяжести .
Тимэктомия выполняется у пациентов с тимомой при отсутствии противопоказаний: миастеническом кризе и наличии множественных метастазов. Удаление вилочковой железы при отсутствии эффекта от консервативной терапии неоправдано, так как миастения не всегда связана с патологией вилочковой железы .
Улучшения после удаления вилочковой железы могут наступают не сразу, а через несколько месяцев или лет. Поэтому операцию рекомендуется выполнять тогда, когда состояние пациента стабильно .
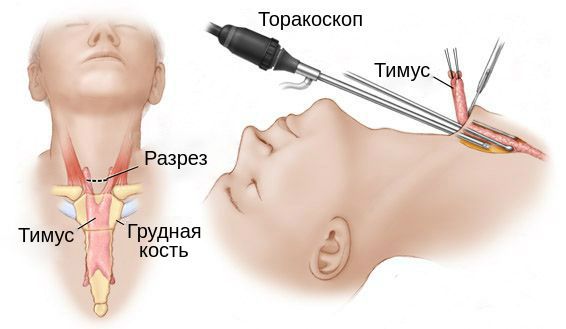
Тимэктомия
К радиологическим методам лечения относится гамма-облучение вилочковой железы. Оно может проводиться при наличии противопоказаний к тимэктомии или после удаления тимомы. К осложнениям гамма-облучения относится лучевой дерматит и пневмонит .
Прогноз. Профилактика
Миастения является достаточно тяжёлым заболеванием. Если пациент вовремя не обратится к врачу и диагноз не будет установлен, то возможен быстрый переход болезни в генерализованую форму и миастенический криз с летальным исходом.
При своевременной постановке диагноза и правильно подобранном лечении возможно наступление ремиссии. При нарушении режима приёма препаратов, после перенесённых инфекций, черепно-мозговых травм и стрессов возможно развитие миастенических кризов с острой дыхательной недостаточностью, нередко приводящих к гибели.
Пациентам с миастенией необходимо ограничить приём препаратов магния, миорелаксантов, петлевых диуретиков, D пеницилламина, нейролептиков, транквилизаторов, хинина, аминогликозидов, фторхинолонов, Стрептомицина, Арбидола и Дексаметазона. Данные средства способствуют развитию миастенических симптомов и усиливают слабость скелетных мышц, т. е. ведут к прогрессированию заболевания.
Больным миастенией следует избегать стрессов, интенсивных физических нагрузок, длительного нахождения на солнце, т. к. это может привести к усугублению дисфункции иммунитета и ухудшению состояния. Особое внимание следует уделять возрастной группе до 18 и старше 60 лет, которые длительно принимают антихолинэстеразные препараты.
К специфическим методам профилактики относится соблюдение режима и дозировки приёма препаратов, контроль своего состояния и необходимость систематических визитов к врачу. При своевременной диагностике, соблюдении рекомендаций врача и регулярном обследовании пациенты живут до самой старости .
Список литературы
- Миастения. Диагностика и лечение / Под ред. С. В. Лобзина. — СПб: СпецЛит, 2015. — 160 с.
- Санадзе А. Г. Миастения и миастенические синдромы. — М.: ЛитТерра, 2012. — 256 с.
- Кумар В., Аббас А. К., Фаусто Н., Астер Дж. К. Основы патологии заболеваний по Роббинсу и Котрану / Пер. с англ. Е. А. Коган, Р. А. Серова и др. — Том 3. — М.: Логосфера, 2016. — С. 1436-1437.
- Мурзалиев А. М., Мусабекова Т. О., Усенова Н. Ш. Миастения (обзор литературы) // Вестник КРСУ. — 2015. — Т. 15, № 11. — С. 109-112.
- Кузин М. И., Гехт Б. М. Миастения. — М.: Медицина, 1996. — 224 с.
- Всероссийское общество неврологов. Миастения. Клинические рекомендации. — М.: 2016.
- Карлов В. А. Неврология / Руководство для врачей. — М.: Медицинское информационное агентство, 1999. — 624 с.
- Дифференциальная диагностика нервных болезней / Под ред. Г. А. Акимова. — СПб.: Гиппократ, 1997. — 608с.
- Карлов В. А. Терапия нервных болезней. — М.: Шаг, 1996. — 653 с.
- Пономарева Е. Н., Казьменок О. И., Синкевич П. А. Миастения гравис: эпидемиология, клинические формы, современный взгляд на патогенез // Мед. новости. — 1998. — № 9. — С. 3-7.
- Харченко В. П., Саркисов Д. С., Ветшев П. С., Галил-Оглы Г. А., Зайратьянц О. В. Болезни вилочковой железы. — М.: Триада–Х, 1998. — 232 с.
- Suresh A. B., Asuncion R. M. D. Myasthenia Gravis // StatPearls Publishing/ — 2020.ссылка
- Bardhan M., Dogra H., Samanta D. Neonatal Myasthenia Gravis // StatPearls Publishing. — 2020.ссылка
- Finnis M. F., Jayawant S. Juvenile Myasthenia Gravis: A Paediatric Perspective // Autoimmune Dis. — 2011: 404101.ссылка
- Sharma S., Lal V., Prabhakar S., Agarwal R. Clinical profile and outcome of myasthenic crisis in a tertiary care hospital: A prospective study // Ann Indian Acad Neurol. — 2013; 16 (2): 203-207.ссылка
- Скворцов М. Б., Шинкарев Н. В. Тимэктомия — обоснование и её роль в лечении миастении // Сибирский медицинский журнал. — 2009. — Т. 86, № 3. — С. 15-23.
- Валикова Т. А., Алифирова В. М., Пугаченко Н. В., Баженова О. А. Клинические проявления и лечение больных миастенией // Бюллетень сибирской медицины. — 2008. — № 5. — С. 72-77.
- Пономарва Е. Н. Ятрогении как фактор риска дебюта и рецидива миастении // Медицинские новости. — 2005. — № 2. — С. 19-21.
- Yeh J. H., Kuo H. T., Chen H. J., Chen Y. K. Higher Risk of Myasthenia Gravis in Patients With Thyroid and Allergic Diseases // Medicine (Baltimore). — 2015; 94 (21): e835.ссылка
- Бардаков С. Н., Живолупов С. А., Рашидов Н. А. Иммунологическая и клиническая гетерогенность миастении // Вестник Российской военно-медицинской академии. — 2016. — № 1. — С. 154-164.
- Чухловина М. Л., Шабалов Н. П., Цинзерлинг Н. В. Особенности патогенеза, клиники и диагностики миастении в детском возрасте // Педиатрия. — 2006. — № 3. — С. 90-94.
- Jowkar A. Myasthenia Gravis Medication / Medscape. — 2018
- Климова Е. М., Дроздова Л. А., Лавинская Е. В., Быченко Е. А. Интегральная методология И. И. Мечникова и современная адресная иммунокоррекция при миастении // Annals of Mechnikov Institute. — 2015. — № 2. — С. 30-37.
- Косачев В. Д., Жулев Н. М., Мартынов А. К. Энтеросорбция в комплексном лечении миастении // Эффективная терапия. — 2006. — № 3. — С. 45-48.
- Даллакян Д. Н., Разумовский А. Ю. Торакоскопическая тимэктомия при генерализованной миастении у детей: обзор литературы // Нейрохирургия и неврология детского возраста. — 2012. — № 4. — С. 106-115.