Системный кандидоз (systemic candidiasis) — это инфекционное грибковое поражение внутренних органов и систем, вызванное неконтролируемым ростом грибков рода Candida. Заболевание обычно развивается у людей со слабым иммунитетом, не способным контролировать грибковый рост.
Синонимы: висцеральный, глубокий, инвазивный кандидоз, висцеральная молочница.
Наиболее распространённой формой системного кандидоза является кандидозная инфекция кровотока, или кандидемия. Она развивается, если грибок попадает в кровоток. При этом инфекция может распространиться по всему организму и затронуть практически все органы: сердце, мозг, лёгкие, печень, почки, селезёнку, кровеносные сосуды и др. Для инфекции кровотока характерно тяжёлое течение и высокая смертность .
Распространённость системного кандидоза
Исследования показывают, что Candida входит в десятку самых распространённых патогенов кровотока. В последние 5–10 лет заболеваемость этой инфекцией выросла .
В прошлом системные инфекции, вызванные грибами Candida и Aspergillus, обычно встречались у пациентов с иммунодефицитом из-за серьёзных заболеваний, таких как лейкемия, нейтропения (аномально низкая концентрация нейтрофилов), СПИД и т. д. Сейчас эти инфекции всё чаще наблюдаются у больных, которые находятся в отделениях интенсивной терапии. Это связано с прогрессом медицины: постоянно растущим числом инвазивных процедур, всё более агрессивными методами лечения, которые подавляют иммунитет, и частым использованием антибиотиков широкого спектра действия.
Эта тенденция подтверждается недавним крупным международным исследованием. В нём оценивали распространённость системных инфекций в отделениях интенсивной терапии и выявили, что Candida стала причиной инфекции у 17 % пациентов, Aspergillus — у 1,4 % .
Инфекция является основной причиной заболеваемости и смертности в отделениях интенсивной терапии во всём мире. Системный кандидоз является наиболее распространённой грибковой инфекцией среди госпитализированных людей в странах с высоким уровнем дохода, включая США .
Причины системного кандидоза
Основным возбудителем системного кандидоза являются грибы рода Candida. Это одноклеточные аэробные микроорганизмы округлой или овальной формы размером от полутора до десяти микрометров. Грибы могут образовывать псевдомицелии (нити из удлинённых клеток) и иногда бластоспоры (бесполые споры грибов, которые образуются путём почкования). Грибы хорошо растут и размножаются в слабокислой среде при температуре 20–37 °С .
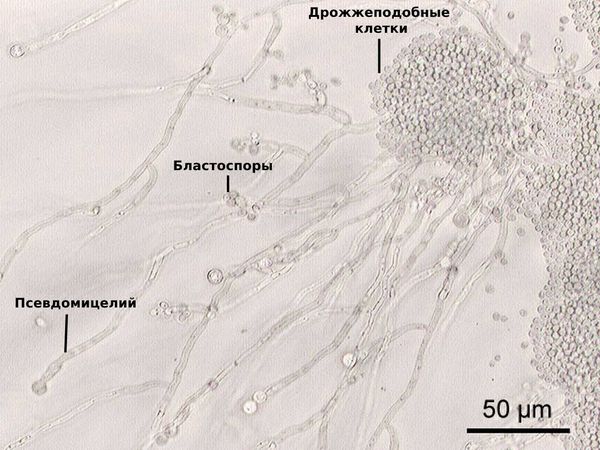
Грибы рода Candida
Грибы Candida относятся к условно-патогенной микрофлоре. Они живут на слизистых оболочках и на коже большинства людей и в умеренном количестве не вызывают симптомов, потому что иммунитет сдерживает их рост.
Ребёнку эти грибки могут передаваться от матери при прохождении через родовые пути и кормлении грудью. Взрослый может заразиться при беспорядочных половых контактах (урогенитальный кандидоз).
Факторы риска системного кандидоза
За последние десятилетия было выявлено множество факторов риска, связанных с развитием системного кандидоза .
В литературе есть мнение, что одним из факторов риска является дисбактериоз — нарушение микрофлоры кишечника. Огромное значение в развитии дисбактериоза имеют антибиотики широкого спектра действия (Стрептомицин, Пенициллин, Синтомицин) и их комбинации. Если долго принимать антибактериальные препараты (около трёх месяцев), полезных бактерий, сдерживающих развитие грибов, становится меньше. В результате защитные силы организма снижаются и возникают благоприятные условия для развития кандидозного поражения. Считается, что комбинированное применение антибиотиков напрямую стимулирует рост дрожжевых грибов.
Немаловажную роль в развитии системного кандидозе учёные и врачи разных стран отводят глюкокортикостероидам и цитостатическим препаратам, хотя ещё недостаточно изучено, как именно они влияют на развитие грибковых поражений.
Также к основным факторам риска относят:
- Приём пероральных контрацептивов.
- Заболевания эндокринной системы: сахарный диабет, ожирение, гипергликемию.
- Онкологические заболевания.
- Иммунодефицитные состояния, например СПИД.
- Цирроз печени.
- Полное парентеральное (внутривенное) питание.
- Оперативные вмешательства на органах брюшной полости.
- Беременность.
Высокая вероятность возникновения кандидоза у беременных связана со снижением иммунитета из-за гормональных сдвигов: высокой концентрации прогестерона и кортикостероидов.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы системного кандидоза
На начальном этапе системного кандидоза появляются симптомы интоксикации: слабость и боль в мышцах, повышенная температура тела, тошнота, рвота и др. Это связано с тем, что накапливаются продукты жизнедеятельности грибов, которые отравляют организм. При этом сами внутренние органы ещё не повреждены .
Кандидоз полости рта сопровождается появлением белого налёта, жжением, дискомфортом и неприятным запахом изо рта . Если грибы попадают изо рта в органы дыхания, больные жалуются на одышку, кашель с выделением слизи, в которой можно заметить «белые нити», и зуд в горле .
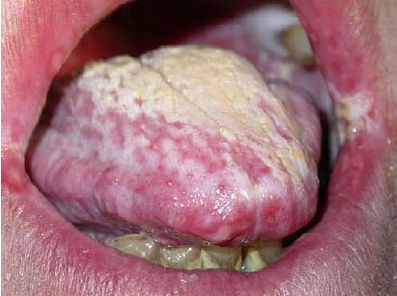
Кандидоз полости рта [53]
При поражении ЖКТ человеку становится трудно глотать, появляется боль в животе и в кишечнике, частая отрыжка, чувство тяжести в области живота, изжога, диарея или запор, метеоризм и др. Зачастую это приводит к тому, что у человека снижается аппетит и он теряет вес.
При поражении мочеполовой системы возникает зуд и жжение в области промежности, учащённое болезненное мочеиспускание, боль в гениталиях и малом тазу при половом акте. Женщины жалуются на творожистые выделения и неприятный запах из влагалища.
При системной кандидозе часто развивается онихомикоз — поражение ногтей. При этом ногти крошатся, слоятся и становятся серыми.
Кандидозное поражение нередко захватывает область вокруг заднего прохода и внутреннюю поверхность бедра. Появляются жалобы на зуд, при этом наблюдается покраснение кожи, её влажность и размягчение .
Патогенез системного кандидоза
В развитии системного кандидоза важную роль играет состояние иммунитета. Если иммунитет сильный, грибы Candida присутствуют на коже и слизистых оболочках, не вызывая развития болезни . Специальные рецепторы (толл-подобные рецепторы и дектин-1) распознают вещества клеточной стенки грибов, при этом вырабатываются провоспалительные цитокины, которые защищают организм . Также было доказано, что клетки иммунитета CD4 и Т-клетки вызывают выработку антикандидозных иммуноглобулинов, которые играют решающую роль в защите организма от инфекций Candida .
Под воздействием разных факторов количество CD4 и Т-клеток снижается, и иммунная защита ослабевает. Если при этом на коже или слизистых есть повреждения, то грибы могут проникнуть в организм, проходя последовательно три стадии:
- Адгезия — прикрепление грибов к клеткам слизистой оболочки. Адгезия грибов Candida связана с их способностью расщеплять секреторный иммуноглобулин А и α-антитрипсин (они защищают слизистые оболочки) и прикрепляться к эпителию.
- Колонизация — процесс размножения в месте адгезии.
- Инвазия — проникновение грибков через слизистую в подлежащие ткани.
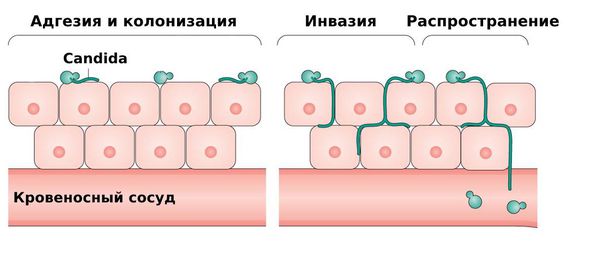
Проникновение грибов в организм
Классификация и стадии развития системного кандидоза
А. Ю. Сергеев и Ю. В. Сергеев выделяют поверхностный и глубокий (висцеральный, или системный) кандидоз.
Классификация поверхностного кандидоза:
- Локализованные формы:
- кандидоз слизистых оболочек (полости рта и вагинальный кандидоз);
- кандидоз кожи и её придатков.
- Генерализованные формы:
- врождённый кандидоз кожи.
В классификации глубокого кандидоза выделено три больших группы:
- Поражения внутренних органов в пределах одной системы (например, кандидоз пищеварительного тракта, органов мочевыделения и др.).
- Диссеминированный кандидоз (кандидозный сепсис).
- Кандидоз ран, травматических и случайных травм во время лечения (медицинского вмешательства).
В каждой группе выделяют множество разновидностей кандидоза .
Осложнения системного кандидоза
Системный кандидоз может приводить к тяжёлым осложнениям тех органов и систем, которые он поражает. В зависимости от локализации патологического процесса осложнения могут быть разными.
При поражении мочеполовой системы может возникнуть пиелонефрит, при поражении дыхательной системы — пневмония. Среди сердечно-сосудистых осложнений выделяют миокардит и эндокардит. При кандидозе пищевода — это стриктура (сужение), кровотечение, перфорация и свищи. Характерно также поражение глаз (эндофтальмит) и суставов (остеомиелит, артрит, хондрит) .
Хроническое течение может наблюдаться, если количество CD4 клеток находится в пределах 200–500 мкл, что говорит об ослаблении иммунитета.
У недоношенных новорождённых тяжёлым осложнением системного кандидоза может стать кандидозный менингит или эндокардит .
Если лечение не проводится, грибы проникают в кровь и распространяются по всему организму человека, при этом может развиться одно из самых опасных проявлений системного кандидоза — кандидозный сепсис, при котором нарушается работа сразу нескольких органов или систем, что может стать причиной смерти.
Диагностика системного кандидоза
При подозрении на кандидоз следует обратиться к врачу:
- при вагинальном кандидозе — к гинекологу или урологу;
- при кандидозе полости рта — к терапевту, стоматологу или гастроэнтерологу;
- при общем недомогании — к терапевту.
Быстрая и точная диагностика системного кандидоза позволяет как можно раньше начать противогрибковое лечение и тем самым улучшить прогноз.
Диагноз «системный кандидоз» ставится на основании лабораторных исследований, но сначала врач спрашивает пациента о его жалобах и осматривает.
Сбор анамнеза и жалоб
На приёме врач изучает историю болезни пациента и спрашивает про жалобы. Среди жалоб может быть белый налёт на слизистых, чувство жжения и дискомфорта, неприятный запах изо рта или влагалища, общее ухудшение состояния, боли в животе, в горле и т. д.
Осмотр
В зависимости от жалоб специалист осматривает слизистые оболочки влагалища или полости рта. Если есть признаки поражения дыхательной системы, врач может провести аускультацию (выслушивание), при подозрении на поражение органов брюшной полости — перкуссию (простукивание) и пальпацию (прощупывание) и т. п.
Лабораторная диагностика
Лабораторные исследования позволяют выявить грибы в исследуемых материалах, а также помогают определить вид гриба-возбудителя и его чувствительность к антимикотикам. Но лабораторная диагностика не всегда проста.
Так как симптомы болезни многообразны, приходится исследовать разный патологический материал: образцы кожи, собранные при соскобе; мокроту; кровь; мочу; ликвор (спинномозговую жидкость); фекалии; желчь; ткани, полученные при пункции полостей (например, желудка); вагинальные выделения; отделяемое свищей; биопсийный материал (кусочки слизистой желудка).
Микроскопическое исследование (исследование биоматериала под микроскопом) выполняется быстро и может быть полезно, но отрицательный результат не исключает заражения .
Посевы крови положительны только в 50–70 % случаев кандидозной инфекции кровотока. Это связано с тем, что в крови может содержаться небольшое количество грибов, которое не распознаётся методом посева . К тому же, чтобы определить вид Candida и его чувствительность к противогрибковым препаратам, требуется несколько дней.
Более того, посевы крови редко бывают положительными у пациентов с глубоко укоренившимся кандидозом. Это связано с низкой чувствительностью культур крови (50 %). Культуры материала, собранные из глубоких участков инфекции, также чувствительны только на 50 %, вероятно, это связано с небольшими объёмами образцов, неравномерным распределением и низкой нагрузкой клеток Candida . Кроме того, сбор образцов с внутренних органов требует травматичных процедур, которые могут быть противопоказаны пациентам с риском заражения Сandida .
В последнее время были разработаны некультурные диагностические тесты, которые позволяют обнаружить в крови компоненты грибковой клеточной стенки, такие как маннаны и β-d-глюканы (БДГ), с помощью иммуноанализа; ДНК с помощью ПЦР; антитела с помощью серологии. Анализ БДГ доказал свою эффективность . Однако это исследование не способно выявить конкретный вид грибка: чтобы его определить, нужны дальнейшие тесты.
Выявление в крови маннанов и антител к ним с высокой вероятностью указывает на наличие в крови грибов Candida . Однако, чтобы подтвердить системный кандидоз, одного положительного теста мало, требуется провести серийные измерения.
Чтобы точно поставить диагноз, современная технология предлагает объединить несколько способов диагностики: ПЦР и гибридизацию (объединение генетического материала разных клеток в одной). Такой метод позволяет менее чем за 3 часа с высокой точностью определить наличие грибов в крови, за счёт этого уменьшить приём противогрибковых средств и снизить смертность . Однако это дорогостоящий метод, который не везде доступен, поэтому необходимы дальнейшие исследования, чтобы подтвердить целесообразность его использования и оценить соотношение затрат и выгод.
Дифференциальную диагностику проводят с трихомониазом, гонореей, гарднереллёзом, лейкоплакией, аллергическим стоматитом, хейлитом и сифилисом.
Лечение системного кандидоза
Лечение системного кандидоза должно быть комплексным и проводиться под контролем врача. Только адекватная терапия поможет не допустить дальнейшего распространения грибковой инфекции в организме. При системном кандидозе недопустимо заниматься самолечением, так как это заболевание может стать причиной смерти.
Трудность терапии заключается в том, что чаще всего у пациентов истощены защитные силы организма. Кроме этого, сам грибок может формировать особые микробные сообщества — биоплёнки, которые защищают его от лекарственных препаратов .
Противогрибковое лечение может быть:
- профилактическим — оно проводится пациентам без симптомов грибковой инфекции, но с высоким риском её развития;
- эмпирическим — проводится до подтверждения диагноза при наличии факторов риска и симптомов грибковой инфекции, например длительной лихорадки;
- упреждающим — проводится при наличии микробиологических или биомаркерных признаков грибка, но без симптомов инфекции;
- окончательным — проводится после положительного микробиологического результата и определения чувствительности грибка.
В большинстве случаев назначается эмпирическое лечение . Упреждающая терапия может быть полезной, но нужны дополнительные исследования, чтобы определить, каким пациентам она подходит и может ли более широкое использование противогрибковых средств негативно повлиять на грибковую экологию .
Есть три основных группы противогрибковых препаратов: азолы, полиены и эхинокандины. Выбор схемы лечения зависит от нескольких факторов:
- эпидемиологических данных: сведений о контактах пациента с инфекционными больными, поездках в регионы, где распространены определённые болезни;
- характеристик пациента, например наличие аллергии к определённым препаратам;
- больничных условий;
- грибкового штамма;
- места инфекции.
Хотя разные противогрибковые препараты могут быть одинаково эффективны, всё же между ними есть различия, например в побочных эффектах, поэтому были разработаны специальные рекомендации, которые помогают врачам правильно выбрать препарат .
При кандидозе чаще всего назначают Флуконазол. Однако в руководстве Европейского общества клинической микробиологии и инфекционных заболеваний (ESCMID) он больше не считается препаратом выбора для системного кандидоза. В качестве эмпирического лечения первой линии рекомендуется использовать эхинокандины . По сравнению с Флуконазолом эхинокандины более эффективны против грибов и у них меньше побочных эффектов при приёме с другими препаратами.
Недавние рекомендации Общества инфекционных заболеваний Америки (IDSA) также рекомендуют эхинокандины для начальной терапии . Все три доступных эхинокандина (Каспофунгин, Микафунгин и Анидулафунгин) хорошо проникают в биоплёнку, препятствуя образованию клеточной стенки гриба.
Тем не менее, Флуконазол остаётся хорошо известным и хорошо переносимым противогрибковым препаратом с более низкой стоимостью по сравнению с эхинокандинами. Его назначают стабильным пациентам без нейтропении, ВИЧ-инфицирования и выраженного угнетения иммунитета после пересадки органов .
Амфотерицин В более токсичен, поэтому его применяют только при низком иммунитете и нейтропении. Длительность терапии будет зависеть от общего состояния пациента, формы системного кандидоза, ответа на лечение и результата посева крови в начале терапии. Обычно лечение продолжается от 72 до 96 часов, после этого делают повторный посев крови. Если посев не выявил грибов в крови, то лечение нужно продолжать ещё 14 дней. Если терапия была начата эмпирически (без положительного посева крови), длительность терапии составляет 14 дней при условии, что состояние пациента улучшается. Повторный посев крови докажет, устранена ли грибковая инфекция .
При кандидозе полости рта назначают спрей Клотримазол и пастилки Нистатин.
При кандидозном эзофагите применяют суспензию Кетоконазола или Флуконазола внутрь.
При кандидозе ЖКТ лечение обычно начинают с введения Амфотерицина В, затем переходят на терапию Флуконазолом или другими азольными антимикотиками в виде таблеток (Кетоконазолом, Итраконазолом). Эти препараты активно всасываются из кишечника и оказывают действие на весь организм.
Некоторые авторы считают, что назначение эубиотиков (препаратов живых бактерий) на начальном этапе терапии кандидоза нецелесообразно, так как антибиотики всё ещё будут действовать. Их применение должно быть обоснованным и индивидуальным . Чаще эубиотики назначают после уничтожения грибов для восстановления микрофлоры после применения антибактериальных препаратов.
Рецидивы возможны, если сохраняются факторы риска. Частота их возникновения зависит от иммунной системы.
Прогноз. Профилактика
Несмотря на усилия по совершенствованию методов лечения, системный кандидоз остаётся опасным заболеванием с высоким риском смерти. Общая смертность находятся в диапазоне 30–60 %, приписываемая смертность оценивается в 25–40 % .
Факторы неблагоприятного прогноза:
- злокачественное новообразование;
- применение мочевого и артериального катетера;
- мужской пол;
- применение глюкокортикостероидов.
Согласно исследованиям, снизить риск смерти помогает раннее начало противогрибкового лечения .
Профилактика системного кандидоза
Чтобы предотвратить развитие системного кандидоза, необходимо:
- Вести здоровый образ жизни:
- отказаться от курения и алкоголя;
- быть физически активным;
- питаться сбалансировано, употреблять больше клетчатки и витаминов и меньше острой, солёной и жареной пищи;
- соблюдать режим труда и отдыха;
- больше времени проводить на свежем воздухе.
- Исключить случайные половые контакты, использовать барьерную контрацепцию.
- Соблюдать личную гигиену полости рта и половых органов: чистить зубы два раза в день, подмываться.
- При вагинальном и других формах поверхностного кандидоза определять чувствительность грибов к антибиотикам, чтобы подобрать грамотную терапию и не допустить распространения инфекции у ослабленных пациентов.
- Медицинские работники должны следовать правилам инфекционной безопасности.
У людей с высоким риском развития системного кандидоза может проводиться профилактика противогрибковыми препаратами.
Обычно она рекомендуется для следующих групп:
- пациентам с трансплантацией органов;
- пациентам в отделении интенсивной терапии;
- пациентам, которые проходят химиотерапию;
- пациентам с нейтропенией .
Иногда профилактика противогрибковыми препаратами проводится новорождённым:
- при очень низкой массе тела (меньше 1000 г);
- при наличии факторов риска развития системного кандидоза, например кандидозной инфекции у матери во время беременности и родов.
Список литературы
- Eggimann P., Garbino J., Pittet D. Epidemiology of Candida species infections in critically ill non-immunosuppressed patients // Lancet Infect Dis. — 2003. — Vol. 3, № 11. — Р. 685–702.ссылка
- Marchetti O., Bille J., Fluckiger U. et al. Fungal Infection Network of Switzerland. Epidemiology of candidemia in Swiss tertiary care hospitals: secular trends, 1991–2000 // Clin Infect Dis. — 2004. — Vol. 38, № 3. — Р. 311–320.ссылка
- Vincent J. L., Rello J., Marshall J. et al. EPIC II Group of Investigators. International study of the prevalence and outcomes of infection in intensive care units // JAMA. — 2009. — Vol. 302, № 21. — Р. 2323–2329.ссылка
- Tortorano A. M., Kibbler C., Peman J. et al. Candidaemia in Europe: epidemiology and resistance // Int J Antimicrob Agents. — 2006. — Vol. 27, № 5. — Р. 359–366.ссылка
- Arendrup M. C., Bruun B., Christensen J. J. et al. National surveillance of fungemia in Denmark (2004 to 2009) // J Clin Microbiol. — 2011. — Vol. 49, № 1. — Р. 325–334.ссылка
- Pittet D., Monod M., Suter P. M. et al. Candida colonization and subsequent infections in critically ill surgical patients // Ann Surg. — 1994. — Vol. 220, № 6. — Р. 751–758.ссылка
- Wey S. B., Mori M., Pfaller M. A. Risk factors for hospital-acquired candidemia. A matched case-control study // Arch Intern Med. — 1989. — Vol. 149, № 10. — Р. 2349–2353.ссылка
- Blumberg H. M., Jarvis W. R., Soucie J. M. National Epidemiology of Mycoses Survey (NEMIS) Study Group. Risk factors for candidal bloodstream infections in surgical intensive care unit patients: the NEMIS prospective multicenter study. The National Epidemiology of Mycosis Survey // Clin Infect Dis. — 2001. — Vol. 33, № 2. — Р. 177–186.ссылка
- Saiman L., Ludington E., Dawson J. D. et al. National Epidemiology of Mycoses Study Group. Risk factors for Candida species colonization of neonatal intensive care unit patients // Pediatr Infect Dis J. — 2001. — Vol. 20, № 12. — Р. 1119–1124.ссылка
- Прилепская В. Н., Байрамова Г. Р. Вульвовагинальный кандидоз современные пути решения проблемы // Трудный пациент. — 2006. — № 9. — С. 33–36.
- Glocker E. O., Hennigs A., Nabavi M. et al. A homozygous CARD9 mutation in a family with susceptibility to fungal infections // N Engl J Med. — 2009. — Vol. 361, № 18. — Р. 1727–1735. ссылка
- Netea M. G., Brown G. D., Kullberg B. J., Gow N. A. An integrated model of the recognition of Candida albicans by the innate immune system // Nat Rev Microbiol. — 2008. — Vol. 6, № 1. — Р. 67–78.ссылка
- Van de Veerdonk F. L., Kullberg B. J., Netea M. G. Pathogenesis of invasive candidiasis // Curr Opin Crit Care. — 2010. — Vol. 16, № 5. — 453–459.ссылка
- Kаposzta R., Tree P., Maródi L., Gordon S. Characteristics of invasive candidiasis in gamma interferon- and interleukin-4-deficient mice: role of macrophages in host defense against Candida albicans // Infect Immun. — 1998. — Vol. 66, № 4. — Р. 1708–1717.ссылка
- Morace G., Borghi E. Fungal infections in ICU patients: epidemiology and the role of diagnostics // Minerva Anestesiol. — 2010. — Vol. 76, № 11. — Р. 950–956.ссылка
- Schelenz S., Barnes R. A., Barton R. C. et al. British Society for Medical Mycology. British Society for Medical Mycology best practice recommendations for the diagnosis of serious fungal diseases // Lancet Infect Dis. — 2015. — Vol. 15, № 4. — Р. 461–474.ссылка
- Clancy C. J., Nguyen M. H. Finding the «missing 50 %» of invasive candidiasis: how nonculture diagnostics will improve understanding of disease spectrum and transform patient care // Clin Infect Dis. — 2013. — Vol. 56, № 9. — Р. 1284–1292.ссылка
- Lamoth F., Cruciani M., Mengoli C. et al. Third European Conference on Infections in Leukemia (ECIL-3). β-Glucan antigenemia assay for the diagnosis of invasive fungal infections in patients with hematological malignancies: a systematic review and meta-analysis of cohort studies from the Third European Conference on Infections in Leukemia (ECIL-3) // Clin Infect Dis. — 2012. — Vol. 54, № 5. — Р. 633–643.ссылка
- Karageorgopoulos D. E., Vouloumanou E. K., Ntziora F. et al. β-D-glucan assay for the diagnosis of invasive fungal infections: a meta-analysis // Clin Infect Dis. — 2011. — Vol. 52, № 6. — Р. 750–770.ссылка
- He S., Hang J. P., Zhang L. et al. A systematic review and meta-analysis of diagnostic accuracy of serum 1,3-β-D-glucan for invasive fungal infection: Focus on cutoff levels // J Microbiol Immunol Infect. — 2015. — Vol. 48, № 4. — Р. 351–361.ссылка
- Mikulska M., Calandra T., Sanguinetti M. et al. Third European Conference on Infections in Leukemia Group. The use of mannan antigen and anti-mannan antibodies in the diagnosis of invasive candidiasis: recommendations from the Third European Conference on Infections in Leukemia // Crit Care. — 2010. — Vol. 14, № 6. ссылка
- Avni T., Leibovici L., Paul M. PCR diagnosis of invasive candidiasis: systematic review and meta-analysis // J Clin Microbiol. — 2011. — Vol. 49, № 2. — Р. 665–670.ссылка
- Neely L. A., Audeh M., Phung N. A. et al. T2 magnetic resonance enables nanoparticle-mediated rapid detection of candidemia in whole blood // Sci Transl Med. — 2013. — Vol. 5, № 182.ссылка
- Mylonakis E., Clancy C. J., Ostrosky-Zeichner L. et al. T2 magnetic resonance assay for the rapid diagnosis of candidemia in whole blood: a clinical trial // Clin Infect Dis. — 2015. — Vol. 60, № 6. — Р. 892–899. ссылка
- Bilir S. P., Ferrufino C. P., Pfaller M. A., Munakata J. The economic impact of rapid Candida species identification by T2Candida among high-risk patients // Future Microbiol. — 2015. — Vol. 10, № 7. — Р. 1133–1144.ссылка
- Cornely O. A., Bassetti M., Calandra T. et al. ESCMID Fungal Infection Study Group. ESCMID* guideline for the diagnosis and management of Candida diseases 2012: non-neutropenic adult patients // Clin Microbiol Infect. — 2012. — Suppl 7. — Р. 19–37. ссылка
- Bassetti M., Leon C., Timsit J. F. Are prophylactic antifungals in highly colonized patients safe and effective? // Intensive Care Med. — 2015. — Vol. 41, № 7. — Р. 1336–1339.ссылка
- Ferreira D., Grenouillet F., Blasco G. et al. Outcomes associated with routine systemic antifungal therapy in critically ill patients with Candida colonization // Intensive Care Med. — 2015. — Vol. 41, № 6. — Р. 1077–1088.ссылка
- Knitsch W., Vincent J. L., Utzolino S. A randomized, placebo-controlled trial of preemptive antifungal therapy for the prevention of invasive candidiasis following gastrointestinal surgery for intra-abdominal infections // Clin Infect Dis. — 2015. — Vol. 61, № 11. — Р. 1671–1678.ссылка
- Bassetti M., Marchetti M., Chakrabarti A. et al. A research agenda on the management of intra-abdominal candidiasis: results from a consensus of multinational experts // Intensive Care Med. — 2013. — Vol. 39, № 12. — Р. 2092–2106.ссылка
- Pappas P. G., Kauffman C. A., Andes D. R. et al. Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of America // Clin Infect Dis. — 2016. — Vol. 62, № 4. — Р. e1–е50.ссылка
- Strausbaugh L. J., Sewell D. L., Ward T. T. et al. High frequency of yeast carriage on hands of hospital personnel // J Clin Microbiol. — 1994. — Vol. 32, № 9. — Р. 2299–2300.ссылка
- Сахарук Н. А., Козловская А. А. Кандидоз: этиология, клиника, диагностика, лечение: монография. — Витебск: ВГМУ, 2010. — 192 с.
- Garey K. W., Rege M., Pai M. P. et al. Time to initiation of fluconazole therapy impacts mortality in patients with candidemia: a multi-institutional study // Clin Infect Dis. — 2006. — Vol. 43, № 1. — Р. 25–31.ссылка
- Pfeiffer C. D., Samsa G. P., Schell W. A. et al. Quantitation of Candida CFU in initial positive blood cultures // J Clin Microbiol. — 2011. — Vol. 49, № 8. — Р. 2879–2883.ссылка
- Sun Y. Q., Xu L. P., Liu D. H. et al. The incidence and risk factors of invasive fungal infection after haploidentical haematopoietic stem cell transplantation without in vitro T-cell depletion // Clin Microbiol Infect. — 2012. — Vol. 18, № 10. — Р. 997–1003.ссылка
- Ostrosky-Zeichner L. Clinical prediction rules for invasive candidiasis in the ICU: ready for prime time? // Crit Care. — 2011. — Vol. 15, № 5. — Р. 189. ссылка
- Vincent J. L., Rello J., Marshall J. et al. International study of the prevalence and outcomes of infection in intensive care units // JAMA. — 2009. — Vol. 302, № 21. — Р. 2323–2329.ссылка
- Darouiche R. O. Candida in the ICU // Clin Chest Med. — 2009. — Vol. 30, № 2. — Р. 287–293.ссылка
- Gagne J. J., Goldfarb N. I. Candidemia in the in-patient setting: treatment options and economics // Expert Opin Pharmacother. — 2007. — Vol. 8, № 11. — Р. 1643–1650.ссылка
- Pfaller M. A., Diekema D. J., Rinaldi M. G. et al. Results from the ARTEMIS DISK Global Antifungal Surveillance Study: a 6.5-year analysis of susceptibilities of Candida and other yeast species to fluconazole and voriconazole by standardized disk diffusion testing // J Clin Microbiol. — 2005. — Vol. 43, № 12. — Р. 5848–5859.ссылка
- Elhoufi A., Ahmadi А., Asnaashari A. M. H. et al. Invasive candidiasis in critical care setting, updated recommendations from «Invasive Fungal Infections-Clinical Forum», Iran // World J Crit Care Med. — 2014. — Vol. 3, № 4. — Р. 102–112.ссылка
- Cohen-Wolkowiez M., Smith P. B., Mangum B. et al. Neonatal Candida meningitis: significance of cerebrospinal fluid parameters and blood cultures // J Perinatol. — 2007. — Vol. 27, № 2. — Р. 97–100.ссылка
- Fernandez M., Moylett E. H., Noyola D. E., Baker C. J. Candidal meningitis in neonates: a 10-year review // Clin Infect Dis. — 2000. — Vol. 31, № 2. — Р. 458–463.ссылка
- Wey S. B., Mori M., Pfaller M. A. Hospital-acquired candidemia. The attributable mortality and excess length of stay // Arch Intern Med. — 1988. — Vol. 148, № 12. — Р. 2642–2645.ссылка
- Voss A., le Noble J. L., Verduyn Lunel F. M. et al. Candidemia in intensive care unit patients: risk factors for mortality // Infection. — 1997. — Vol. 25, № 1. — Р. 8–11.ссылка
- Blot S. I., Vandewoude K. H., Hoste E. A., Colardyn F. A. Effects of nosocomial candidemia on outcomes of critically ill patients // Am J Med. — 2002. — Vol. 113, № 6. — Р. 480–485. ссылка
- Wisplinghoff H., Bischoff T., Tallent S. M. et al. Nosocomial bloodstream infections in US hospitals: analysis of 24,179 cases from a prospective nationwide surveillance study // Clin Infect Dis. — 2004. — Vol. 39, № 3. — Р. 309–317.ссылка
- Gudlaugsson O., Gillespie S., Lee K. et al. Attributable mortality of nosocomial candidemia, revisited // Clin Infect Dis. — 2003. — Vol. 37, № 9. — Р. 1172–1177.ссылка
- Morrell M., Fraser V. J., Kollef M. H. Delaying the empiric treatment of candida bloodstream infection until positive blood culture results are obtained: a potential risk factor for hospital mortality // Antimicrob Agents Chemother. — 2005. — Vol. 49, № 9. — Р. 3640–3645. ссылка
- Pana Z. D., Dotis J., Iosifidis E., Roilides E. Fungal Endocarditis in Neonates: A Review of Seventy-one Cases (1971–2013) // Pediatr Infect Dis J. — 2015. — Vol. 34, № 8. — Р. 803–808.ссылка
- Invasive Candidiasis // Centers for Disease Control and Prevention. — 2020.ссылка
- Nicolatou-Galitis O., Velegraki A., Sotiropoulou-Lontou A. et al. Effect of fluconazole antifungal prophylaxis on oral mucositis in head and neck cancer patients receiving radiotherapy // Support Care Cancer. — 2006. — Vol. 14, № 1. — Р. 44–51.ссылка