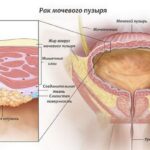
Рак яичников (ovarian cancer) — это злокачественная опухоль, которая возникает из-за бесконтрольного роста клеток в ткани яичников. Как правило, поначалу протекает бессимптомно и даёт о себе знать только на поздних стадиях. Может проявляться такими неспецифическими симптомами, как боль, вздутие живота, слабость, потеря веса и др.
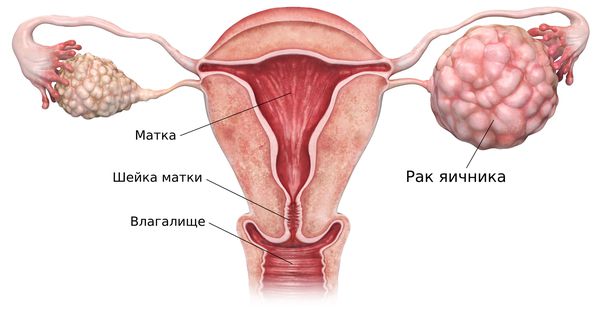
Рак левого яичника
Среди всех опухолей женской репродуктивной системы на долю рака яичников приходится 32 % . Ежегодно им заболевают 165 000 женщин в мире и более 100 000 умирают. В России диагностируется более 12 000 новых случаев рака яичников в год, а каждые 2 часа от этого недуга умирает одна пациентка .
Столь неутешительная статистика связана с особенностями этой болезни: она проявляет себя в основном на поздних стадиях (III и IV). При таком распространённом процессе 7 из 10 женщин умирают в течение 5 лет, несмотря на самое современное лечение. Доля пациентов с поздними стадиями составляет 70–80 % .
У рака яичников довольно много типов, но в статье пойдёт речь в основном об эпителиальном раке яичника, так как этот тип болезни встречается чаще всего (более 80 % случаев) .
Причины рака яичников (этиология)
Основные причины развития эпителиального рака яичника хорошо известны. К ним относятся:
- Возраст. Болезнь редко встречается до 40 лет. Половина всех случаев диагностируется после 63 лет.
- Роды после 35 лет или их отсутствие.
- Избыточная масса тела. Вероятно, эта причина связана с увеличением уровня эстрогенов, которые жировая ткань преобразует из других гормонов — андрогенов. Значительно повышенный уровень эстрогенов увеличивает риск развития рака яичников, поэтому чем больше жировой ткани, тем выше риск заболеть.
- Приём чистых эстрогенов в постменопаузе. Не все гормональные препараты приводят к раку яичников. Комбинированные оральные контрацептивы (КОК), напротив, значительно снижают риск формирования рака яичника, если принимать их не меньше пяти лет. КОК убирают овуляцию как один из основных механизмов развития болезни .
- Гормональная стимуляция яичников для наступления беременности. Она нарушает соотношение гормонов и приводит к функциональным изменениям ткани яичников.
- Генетическая предрасположенность: синдром Линча, синдром наследственного рака яичников или рака молочной железы. Эти заболевания могут стать проявлением так называемого наследственного синдрома, который возникает из-за мутаций в определённых генах (BRCA1, BRCA2, RAD51С, RAD51D, PALB2 и др.).
Наследственный рак яичников среди славянских женщин встречается примерно в 20 % случаев. Риск его развития при мутациях в генах BRCA1 составляет 35–70 %. Это значит, что рак яичников, по статистике, разовьётся у 35–70 женщин из 100. При мутации в гене BRCA2 риск несколько ниже (10–30 %) . Аналогичным образом повышается вероятность развития рака маточных труб и брюшины. Для сравнения, прижизненный риск развития рака яичников, не связанного с генетическими мутациями, составляет 2 %.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака яичников
Зачастую рак яичников начинает проявляться на поздних стадиях в виде неспецифических симптомов . К наиболее частым относятся:
- увеличение и вздутие живота;
- быстрая насыщаемость, тошнота, потеря аппетита;
- боли в животе (чаще внизу живота);
- учащённое мочеиспускание;
- затруднённая дефекация или диарея;
- слабость;
- потеря веса;
- одышка.
Эти симптомы вызывает не только рак яичников, но и другие болезни. Заподозрить злокачественную опухоль можно, если подобные проявления:
- новые — длятся меньше года;
- частые — беспокоят больше 12 дней каждого месяца.
Патогенез рака яичников
Яичники — это небольшой парный орган, расположенный по обе стороны от матки. В них созревают яйцеклетки и вырабатываются гормоны — эстрогены и прогестероны.
Яичники покрыты слоем ткани (эпителия), который состоит из эпителиальных клеток. В 90 % случаев рак развивается именно из этих клеток и называется эпителиальным. Аналогичная ткань покрывает маточные трубы и брюшину, поэтому опухоли, развивающиеся в этих органах, принято относить к одной группе и лечить схожим образом .
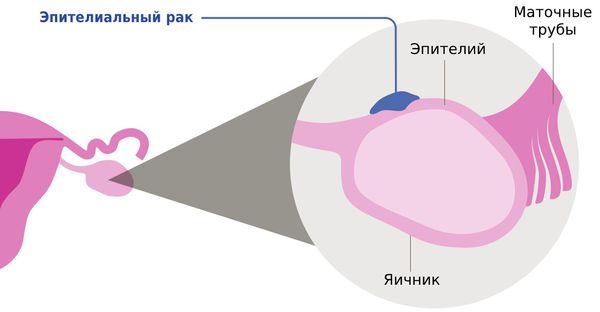
Эпителиальный рак яичника
Существует несколько теорий развития рака яичников.
Согласно первой, болезнь вызывают множественные овуляции, которые примерно раз месяц происходят у каждой женщины в репродуктивной период, т. е. примерно на 9-й день цикла. При овуляции яйцеклетка выходит из яичника и травмирует его поверхность. Тем самым она активирует сложный каскад реакций по его восстановлению. При сбое этого механизма может возникнуть атипическая (раковая) клетка, которая начинает активно делиться.
Согласно второй теории, опухолевые клетки изначально развиваются в маточной трубе (её фимбриальном отделе), затем мигрируют на поверхность яичника и там под действием различных факторов начинают делиться, со временем образуя опухоль.
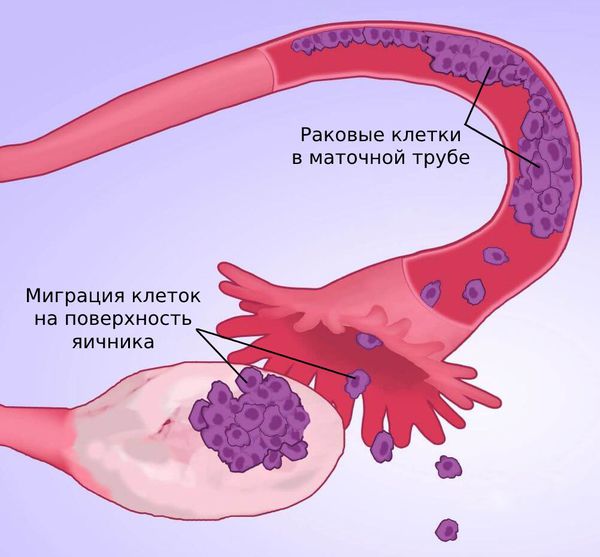
Миграция раковых клеток из маточной трубы на эпителий яичника
Согласно третьей теории, рак яичников развивается из-за мутаций при обратном токе менструальной крови через маточные трубы. Клетки эндометрия (слизистой оболочки матки) присоединяются к эпителию яичника, и в результате развиваются специфические типы рака — светлоклеточный и эндометриоидный.
Опухолевые клетки принципиально отличаются от здоровых по трём аспектам:
- Атипические клетки растут и делятся без контроля, они не умирают, когда приходит время. Объединяясь, они формируют опухоль.
- Раковые клетки способны прорасти в соседние ткани. Такой феномен называется инвазией. Со временем опухоль яичника может прорастать в матку, маточные трубы, кишку и мочевой пузырь.
- Опухолевые клетки могут метастазировать, то есть мигрировать в другие органы с током крови и лимфатической жидкости. При раке яичников часть клеток способна отделиться от первичной опухоли и сформировать опухоль на поверхности органов брюшной полости — это ещё один особенный механизм распространения рака яичников.
Имплантация опухолевых клеток по брюшине называется канцероматозом. Обычно брюшина выделяет немного жидкости, омывающей внутренние органы. Её избыток самостоятельно всасывается, но при канцероматозе этот процесс нарушается и жидкость скапливается, приводя к асциту. Зачастую это нарушение является одним из первых признаков болезни.
Аналогичным образом может поражаться плевра, выстилающая грудную полость. Это приводит к плевриту — скоплению жидкости вокруг лёгких. Но развитие асцита и плеврита является лишь косвенным признаком поздних стадий рака яичника.
Классификация и стадии развития рака яичников
Типы рака яичников
Рак яичников классифицируют по виду клеток, из которых он развивается . Тип опухоли устанавливает патолог — эксперт, который изучает удалённые ткани под микроскопом. Такое исследование — единственный способ определить разновидность рака и его дифференцировку, т. е. узнать, насколько клетки опухоли похожи на здоровую ткань, как быстро они могут расти и распространяться.
Выделяют три степени дифференцировки: G1, G2 и G3. Самая неблагоприятная — G3. Она указывает на быстрый рост опухоли.
Сейчас всё чаще выделяют только два класса: low grade (G1 и G2) и high grade (G3).
Классификация рака по виду клеток очень сложна из-за большого разнообразия: существует более ста видов опухолей. Чаще всего встречается эпителиальный рак. Он составляет более 80 % всех злокачественных опухолей яичников. Его подразделяют на четыре основных подтипа:
- серозный (80 %) — самый частый подтип, редко бывает G1 и G2 (в 10 % случаев);
- муцинозный (7–14 %) — относительно благоприятный тип, особенно на ранних стадиях;
- эндометриоидный (10%) — может сочетаться с раком эндометрия ;
- светлоклеточный (5%) — чаще выявляется на ранней стадии и хорошо поддаётся терапии, но в запущенных случаях устойчив к лечению .
Несмотря на разделение, все четыре подтипа часто лечатся схожим образом, но отличаются по прогнозу.
Стадии рака яичников
Стадия рака определяется по двум системам: классификации FIGO (Международной федерации гинекологии и акушерства) и классификации AJCC (Объединённого американского комитета по раку). Обе системы опираются на три ключевых аспекта — TNM:
- Tumor — размер опухоли.
- Node — наличие/отсутствие опухоли в лимфоузлах.
- Metastasis — наличие/отсутствие метастазов .
Исходя из этого, выделяют четыре стадии рака. Чем больше стадия, тем хуже прогноз.
| Категории TNM | Стадии FIGO | Характеристика стадии |
|---|---|---|
| T1 | I | Опухоль не выходит за пределы яичников |
| T1a | IA | Опухоль находится внутри одного яичника, её капсула не повреждена, злокачественных клеток в асцитической жидкости или смывах из брюшной полости нет |
| T1b | IB | Опухоль находится внутри двух яичников, капсулы опухоли не повреждены, злокачественных клеток в асцитической жидкости или смывах из брюшной полости нет |
| T1c | IC | Опухоль не выходит за пределы яичников, сопровождается одним из трёх факторов, перечисленных ниже |
| T1c1 | IC1 | Капсула опухоли повреждена при операции |
| T1c2 | IC2 | Капсула опухоли повреждена до операции, или опухоль разрослась на поверхности яичника/маточной трубы |
| T1c3 | IC3 | В асцитической жидкости или смывах с брюшины обнаружены злокачественные клетки |
| T2 | II | Опухоль распространилась на органы малого таза |
| T2a | IIA | Опухоль проросла и/или метастазировала в матку и/или маточную трубу |
| T2b | IIB | Опухоль распространилась на другие ткани таза |
| T2c | IIC | Опухоль затрагивает структуры малого таза (2a или 2b), в асцитической или перитонеальной жидкости обнаружены злокачественные клетки |
| T3 и/или N1 | III | Опухоль поражает один или оба яичника, гистологически подтверждены внутрибрюшинные метастазы за пределами таза и/или метастазы в регионарных лимфоузлах (внутренних, наружных и общих подвздошных, запирательных, крестцовых или поясничных) |
| N1 | IIIA1 | Метастазы находятся только в забрюшинных лимфоузлах |
| IIIA1(i) | Метастазы в лимфоузлах не больше 10 мм | |
| IIIA1(ii) | Метастазы в лимфоузлах больше 10 мм | |
| T3a | IIIA2 | Есть внутрибрюшинные метастазы за пределами таза, могут быть метастазы в забрюшинных лимфоузлах, результаты подтверждены микроскопически и гистологически |
| T3b | IIIB | Макроскопические внутрибрюшинные метастазы не больше 2 см, обнаружены за пределами таза, могут быть метастазы в забрюшинных лимфоузлах |
| T3c и/или N1 | IIIC | Размер внутрибрюшинных метастазов за пределами таза превышает 2 см, могут быть метастазы в забрюшинных лимфоузлах, на капсуле печени и селезёнки без поражения основной ткани органов |
| M1 | IV | Есть внутрибрюшинные и отдалённые метастазы |
| IVA | В плевральном выпоте обнаружены злокачественные клетки | |
| IVIB | Есть отдалённые метастазы внутри других органов, в том числе в паховых лимфоузлах и лимфоузлах за пределами брюшной полости |
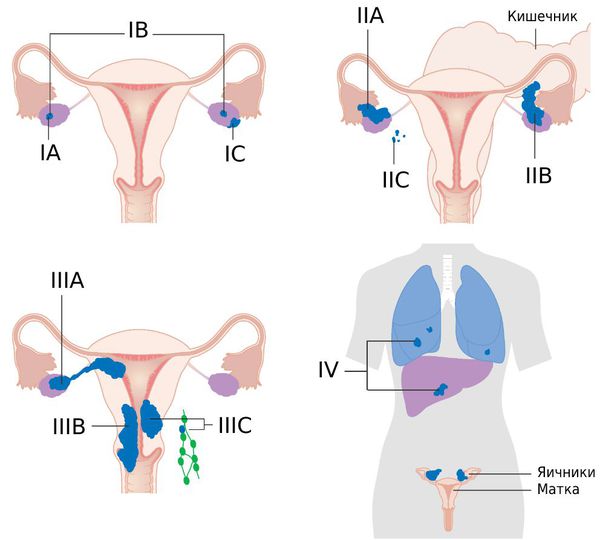
Стадии рака яичников [27]
Стадию рака обычно определяют дважды:
- первый раз — до лечения;
- второй раз — после операции.
Первое стадирование называется клиническим. Оно опирается на результаты инструментальной диагностики: КТ, МРТ, УЗИ и др.
Второе стадирование называется патологоанатомическим. Оно считается более точным и окончательным.
Со временем опухоль может прорасти в другие органы или появиться снова после полного излечения (чем меньше стадия рака, тем ниже вероятность рецидива). В этом случае установленная раньше стадия меняться не будет — к диагнозу добавится термин «прогрессирование» или «рецидив» с указанием места развития опухоли.
Осложнения рака яичников
При постепенном росте опухоли может нарушиться её питание. Кровеносные сосуды сдавливаются, что ведёт к омертвению опухоли, которое чаще всего сопровождается нестерпимой болью. Такое осложнение требует немедленного хирургического вмешательства.
Также постепенный рост опухоли может осложниться разрывом новообразования. Для него характерны схожие симптомы, но, помимо нестерпимой боли, возникает кровотечение.
Злокачественные опухоли яичника могут увеличиваться до 30–40 см, их ограничивает только размер брюшной полости. Со временем новообразования могут прорасти или сдавить соседние органы. При сдавлении мочевого пузыря у пациента учащается мочеиспускание, при сдавлении прямой кишки возникают запоры или учащается стул. При прорастании опухоли в органы малого таза в моче или стуле может появиться кровь.
Если опухоль поражает брюшину (ткань, выстилающую брюшную полость), в животе скапливается избыток жидкости, т. е. развивается асцит. Единственным адекватным лечением в этом случае является химиотерапия. Но асцит не проходит быстро, поэтому иногда проводят хирургическую эвакуацию — лапароцентез. Процедура несложная, занимает около 10 минут и проводится под местной анестезией.
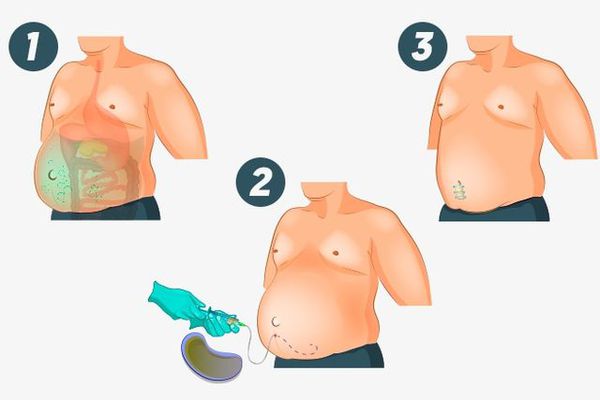
Асцит и лапароцентез
Единственным показанием к лапароцентезу является напряжённый асцит. Он сопровождается болью в пояснице, живот раздувается, как барабан, из-за затруднённого дыхания пациент вынужден находиться в полусидячем положении.
Поражение лёгких и плевры ведёт к развитию плеврита — избыточному скоплению жидкости в грудной клетке. Это осложнение проявляется одышкой и нехваткой воздуха. Как и в случае с асцитом, плеврит проходит на фоне лечения, но иногда может потребоваться хирургическая эвакуация жидкости .
Диагностика рака яичников
Заподозрить рак яичников можно по симптомам, но иногда болезнь диагностируется случайно при удалении кисты яичников. Чтобы подтвердить диагноз и спланировать лечение, нужно пройти комплекс обследований.
При общении с врачом следует упомянуть, когда появились первые признаки болезни, вспомнить, у кого из родственников были онкологические заболевания и какие именно. Эта информация называется наследственностью, для её интерпретации может потребоваться консультация генетика.
Перед лечением проводятся инструментальные тесты. К ним относятся:
- Компьютерная томография (КТ) груди и живота. По сути — это более детальная рентгенография. Пациентка ложится лицом вверх на стол, который движется через большой тоннель. Томограф делает несколько снимков под разными углами, затем компьютер обрабатывает их и объединяет в 3D-изображение. Чтобы лучше всё рассмотреть, перед исследованием используется контрастный препарат (контраст). Его вводят внутривенно и/или принимают внутрь в разведённом виде.
- Позитронно-эмиссионная компьютерная томография (ПЭТ-КТ). При исследовании используется глюкоза с радиоактивным элементом, который выделяет небольшое, но заметное количество энергии. Клетки опухоли активней поглощают глюкозу, чем здоровые, поэтому на изображении они будут заметнее остальных .
- Магнитно-резонансная томография (МРТ) малого таза. Позволяет оценить состояние мягких тканей. Снимок создаётся с помощью мощных магнитных полей и радиоволн. При этом облучение, как во время рентгенографии или КТ, не происходит.
- Эзофагогастроскопия. Проводится, чтобы исключить рак желудка, который иногда метастазирует в яичники. Также метод позволяет оценить состояние слизистой оболочки желудка, так как специализированное лечение рака (операция и химиотерапия) может обострить хронические процессы (язву или гастрит).
- Колоноскопия. Проводится для исследования толстой кишки на предмет метастазов или иных видов рака.
- Исследование онкомаркеров крови.
Компьютерная томография
УЗИ не обладает достаточной точностью, поэтому не используется как самостоятельный метод исследования при раке яичников. Оно помогает лишь заподозрить новообразование.
Онкомаркеры
При подозрении на эпителиальный рак яичников обычно исследуется маркер Са-125. Но его повышение не всегда указывает на онкозаболевание. Во-первых, в 20 % случаев болезни этот маркер не увеличивается. Во-вторых, Са-125 может повыситься при воспалительных заболеваниях или доброкачественных процессах, например простых кистах яичников и миоме матки. Практически всегда его концентрация увеличивается при беременности.
Чтобы увеличить точность диагностики, врачи стали применять специальные алгоритмы, которые учитывают несколько показателей крови. К самым распространённым относится алгоритм ROMA. Он учитывает значения двух маркеров: Са-125 и НЕ4 .
Помимо перечисленных, применяются онкомаркеры Са 19-9, ингибин, ХГЧ, ЛДГ и АФП. Их повышение может указать на конкретный тип рака.
Оценивать нужно все результаты обследования. Изолированная интерпретация того или иного теста может стать причиной ошибочного заключения. Если у пациентки нет симптомов рака яичника, то сдавать анализы на онкомаркеры нецелесообразно.
Гистологическое исследование
Перед лечением нужно подтвердить диагноз, т. е. обнаружить опухолевые клетки. Сделать это можно двумя способами:
- диагностическая операция — помогает забрать фрагмент опухоли для исследования и оценить распространённость рака;
- пункция брюшной полости под контролем УЗИ — позволяет взять жидкость для цитологического исследования.
Принципиально важен уровень специалиста, который тестирует полученный материал. Исследовать фрагмент опухоли или жидкость должен патолог, который специализируется в сфере онкологии.
Лечение рака яичников
Обычно план лечения включает операцию и химиотерапию. Чаще этим занимается онкогинеколог, но иногда к лечению подключается врач-химиотерапевт — он занимается только лекарственной терапией.
Хирургическое лечение рака яичников
Универсального способа борьбы с раком яичника не существует.
Принято считать, что лечение лучше начинать с операции, если её можно выполнить радикально, т. е. удалить всю опухоль без остатка . Операция позволит не только устранить новообразование, но и определить степень распространения и стадию рака. Крайне важно, чтобы хирургическое лечение проводил опытный онколог.
Стандартным минимальным объёмом операции считается удаление матки, яичников, маточных труб и большого сальника. И хотя полное удаление опухоли может снизить качество жизни пациентки, оно увеличивает продолжительность жизни.
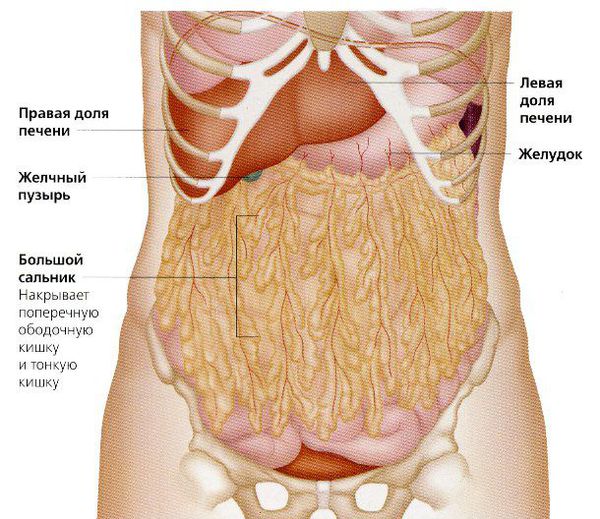
Большой сальник
Если опухоль распространилась на соседние органы, их частично или полностью удаляют. Такие операции называются циторедуктивными. Например, при врастании опухоли в кишку проводится её резекция (частичное удаление), зачастую с наложением колостомы — временным выведением кишки на переднюю брюшную стенку.
Врач не всегда наверняка знает, как именно распространился рак, поскольку точность инструментальных методов диагностики, на которые он полагается при планировании лечения, ограничена.
На объём операции влияет размер опухоли, её локализация и распространение. Важным фактором также является возраст пациентки и её желание забеременеть после лечения. Например, у молодых пациенток с первой стадией рака можно выполнить органосохранные хирургические вмешательства.
Большинство операций выполняется через продольный разрез передней брюшной стенки (лапаротомия). Лапароскопия, при которой через небольшие надрезы до 1 см вводятся камера и специальные длинные инструменты, применяется реже. В основном она нужна, чтобы оценить распространённость опухоли, или проводится на начальных стадиях рака, когда опухоль ещё не вышла за пределы яичников .
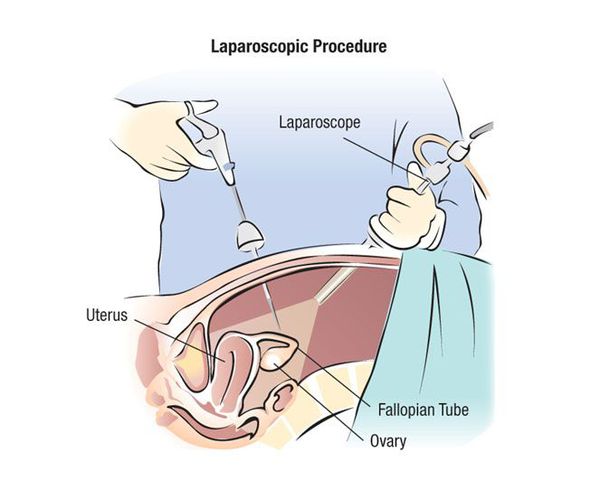
Лапароскопия
Химиотерапия при раке яичников
Химиотерапия воздействует на быстрорастущие раковые клетки. Иногда её назначают до операции, чтобы уменьшить размер и распространение опухоли, т. е. перевести опухолевый процесс из неоперабельного в операбельный. Такую химиотерапию называют неоадъювантной. Обычно пациентке назначают Паклитаксел и Карбоплатин, так как они считаются наиболее эффективными. В основном химиотерапия проводится однодневными циклами с перерывом в 21 день .
Также химиотерапию назначают после операции в рамках комплексного лечения. Чаще всего препараты вводят внутривенно, но иногда применяется гипертермическая внутрибрюшнная химиоперфузия, или «горячая химиотерапия»: во время операции в брюшную полость вводят подогретый химиопрепарат Цисплатин, который циркулирует в крови около 1,5 часов. Основным показанием к «горячей химиотерапии» является распространённый рак яичников с метастазами в брюшной полости.
Цисплатин также можно вводить неподогретым, но тогда он оказывает менее выраженное действие. Такая химиотерапия называется интраперитонеальной.
Одними из современных направлений в лекарственной терапии являются таргетная и иммунотерапия. Таргетные препараты менее токсичны для здоровых тканей. Они воздействуют на молекулы, которые помогают расти раковым клеткам. Иммунотерапия, напротив, увеличивает активность собственной иммунной системы, позволяя ей лучше справляться с онкологическим заболеванием.
Вот несколько современных препаратов:
- Ингибиторы ангиогенеза: Авастин (Бевацизумаб). Чтобы раковая опухоль могла расти, она формирует новые сосуды. Это процесс называется ангиогенезом. Бевацизумаб присоединяется к специальному белку VEGF, тем самым замедляя рост сосудов и опухоли в целом. Он эффективен против эпителиального рака яичников и может применяться как самостоятельно, так и вместе с химиопрепаратами .
- PARP-ингибиторы: Олапариб, Рукапариб, Нирапариб. PARP-энзимы — это молекулы, которые помогают восстанавливать повреждённые ДНК внутри клеток. Такие повреждения могут быть связаны с мутациями в генах BRCA, которые приводят к развитию рака. Блокируя PARP-путь, ингибиторы мешают опухолевым клеткам с этими мутациями восстанавливаться и делиться. PARP-ингибиторы менее токсичны, чем химиотерапия, но не лишены такого негативного воздействия.
Лучевая терапия не относится к основным методам лечения рака яичников, но иногда может с успехом применяться.
Прогноз. Профилактика
Прогноз зависит от стадии рака: чем она больше, тем хуже вероятный сценарий. Также на прогноз влияет тип опухоли, т. е. вид клеток, из которых она развивается. Высокодифференцированные опухоли (G1), близкие по строению к тканям яичника, растут медленнее остальных и лучше поддаются химиотерапии.
Предупредить развитие рака яичников можно несколькими способами. Если на такие факторы риска, как возраст или наследственность, повлиять нельзя, то другие можно проконтролировать, например избыточный вес, питание, курение, приём чистых эстрогенов.
Комбинированные оральные контрацептивы помогают снизить риск развития болезни на 50 %. Их рекомендуют принимать не меньше 5 лет. Чем дольше пациентка будет пользоваться такими препаратами, тем меньше вероятность заболеть раком яичников. Профилактический эффект сохраняется даже после их отмены.
Беременность и роды до 26 лет достоверно снижают риск развития рака яичников, причём риск уменьшается с каждой следующей беременностью . Грудное вскармливание также относится к благоприятным факторам.
Профилактические операции. Лигирование (перевязка) маточных труб и удаление матки снижают риск развития рака яичников, но эксперты сходятся во мнении, что такие операции должны выполняться по медицинским показаниям, а не ради профилактики. Единственная группа пациентов, чьи профилактические операции будут оправданы, — это женщины с мутациями в генах, кодирующих наследственный рак.
Яичники и маточные трубы целесообразно удалять после родов и/или после 45 лет. До тех пор женщины должны регулярно наблюдаться у врача: раз в шесть месяцев выполнять УЗИ малого таза с контролем онкомаркера Са-125, а также УЗИ и МРТ молочных желёз .
Вопрос о проведении профилактических операций в России ещё не урегулирован, поэтому пациентки пока не могут их сделать даже при желании и подтверждённых рисках развития рака.
Список литературы
- Каприн А. Д., Старинский В. В., Петрова Г. В. Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). — М.: МНИОН им. П. А. Герцина, 2018. — 250 с.
- Chan J. K., Cheung M. K., Husain A. et al. Patterns and progress in ovarian cancer over 14 years // Obstet Gynecol. — 2006. — Vol. 10, № 3. — P. 521–528.ссылка
- Siegel R. L., Miller K. D., Jemal A. Cancer statistics, 2018 // CA Cancer J Clin. — 2018. — Vol. 68, № 1. — P. 7–30.ссылка
- Ramirez P. T., Salvo G. Ovarian Cancer // MSD Manuals. — 2020.
- Rebbeck T. R., Mitra N., Wan F. et al. Association of type and location of BRCA1 and BRCA2 mutations with risk of breast and ovarian cancer // JAMA. — 2015. — Vol. 313, № 13. — P. 1347–1361.ссылка
- Walsh C. S., Blum A., Walts A. et al. Lynch syndrome among gynecologic oncology patients meeting Bethesda guidelines for screening // Gynecol Oncol. — 2010. — Vol. 116, № 3. — P. 516–521.ссылка
- Wentzensen N., Poole E. M., Trabert B. et al. Ovarian cancer risk factors by histologic subtype: an analysis from the Ovarian Cancer Cohort Consortium // J Clin Oncol. — 2016. — Vol. 34, № 24. — P. 2888–2898.ссылка
- Holschneider C. H., Berek J. S. Ovarian cancer: epidemiology, biology, and prognostic factors // Semin Surg Oncol. — 2000. — Vol. 19, № 1. — P. 3–10.ссылка
- Zeppernick F., Meinhold-Heerlein I. The new FIGO staging system for ovarian, fallopian tube, and primary peritoneal cancer // Arch Gynecol Obstet. — 2014. — Vol. 290, № 5. — P. 839–842.ссылка
- WHO Classification of Tumours. Female genital organ tumours, International agency for research on cancer IARC. — 5th edn. — Lyon, 2020. — 632 p.
- McCluggage W. G. Morphological subtypes of ovarian carcinoma: a review with emphasis on new developments and pathogenesis // Pathology. — 2011. — Vol. 43, № 5. — P. 420–432.ссылка
- Amin M., Greene F., Edge S. et al. AJCC Staging Manual. — 8th edn. — 2017. — P. 1–1024.
- Ferrell B. R., Temel J. S., Temin S. et al. Integration of palliative care into standard oncology care: American Society of Clinical Oncology Clinical Practice Guideline Update // J Clin Oncol. — 2017. — Vol. 35, № 1. — P. 96–112.ссылка
- Yamamoto Y., Oguri H., Yamada R. et al. Preoperative evaluation of pelvic masses with combined 18F-fluorodeoxyglucose positron emission tomography and computed tomography // Int J Gynaecol Obstet. — 2008. — Vol. 102, № 2. — P. 124–127.ссылка
- Romagnolo C., Leon A. E., Fabricio A. S. et al. HE4, CA125 and risk of ovarian malignancy algorithm (ROMA) as diagnostic tools for ovarian cancer in patients with a pelvic mass: An Italian multicenter study // Gynecol Oncol. — 2016. — Vol. 141, № 2. — P. 303–311.ссылка
- Brockbank E. C., Harry V., Kolomainen D. et al. Laparoscopic staging for apparent early stage ovarian or fallopian tube cancer. First case series from a UK cancer centre and systematic literature review // Eur J Surg Oncol. — 2013. — Vol. 39, № 8. — P. 912–917.ссылка
- Bristow R. E., Tomacruz R. S., Armstrong D. K. et al. Survival effect of maximal cytoreductive surgery for advanced ovarian carcinoma during the platinum era: a meta-analysis // J Clin Oncol. — 2002. — Vol. 20, № 5. — P. 1248–1259.ссылка
- Wright A. A., Bohlke K., Armstrong D. K. et al. Neoadjuvant chemotherapy for newly diagnosed, advanced ovarian cancer: Society of Gynecologic Oncology and American Society of Clinical Oncology Clinical Practice Guideline // Gynecol Oncol. — 2016. — Vol. 143, № 1. — P. 3–15.ссылка
- Garcia Y. G., Juan A. D., Mendiola C. et al. Phase II randomized trial of neoadjuvant (NA) chemotherapy (CT) with or without bevacizumab (Bev) in advanced epithelial ovarian cancer (EOC) (GEICO 1205/NOVA TRIAL) // J Clin Oncol. — 2017. — Vol. 35. — P. 5508.
- Webb P. M., Jordan S. J. Epidemiology of epithelial ovarian cancer // Best Pract Res Clin Obstet Gynaecol. — 2017. — Vol. 41. — P. 3–14.ссылка
- Falconer H., Yin L., Gronberg H., Altman D. Ovarian cancer risk after salpingectomy: a nationwide population-based study // J Natl Cancer Inst. — 2015. — Vol. 107, № 2.ссылка
- Hartmann L. C., Lindor N. M. The role of risk-reducing surgery in hereditary breast and ovarian cancer // N Engl J Med. — 2016. — Vol. 374, № 5. — P. 454–468.ссылка
- Chien J., Poole E. M. Ovarian Cancer Prevention, Screening, and Early Detection: Report From the 11th Biennial Ovarian Cancer Research Symposium // Int J Gynecol Cancer. — 2017. — Vol. 27. — P. S20–S22.ссылка
- Walker J. L., Powell C. B., Chen L. M. et al. Society of Gynecologic Oncology recommendations for the prevention of ovarian cancer // Cancer. — 2015. — Vol. 121, № 13. — P. 2108–2120.ссылка
- Cybulska P., Paula A. D. C., Tseng J., Leitao M. M. Jr. Et al. Molecular profiling and molecular classification of endometrioid ovarian carcinomas // Gynecol Oncol. — 2019. — Vol. 154, № 3. — P. 516–523.ссылка
- Fujiwara K., Shintani D., Nishikawa T. Clear-cell carcinoma of the ovary // Ann Oncol. — 2016. — Vol. 27. — P. i50–i52.ссылка
- Katopodis P., Chudasama D., Wander G., Sales L. et al. Kinase Inhibitors and Ovarian Cancer // Cancers. — 2019. — Vol. 11, № 9. — P. 1357.ссылка