Рак анального канала — редкое онкологическое заболевание, основным фактором развития которого является наличие в организме вируса папилломы человека (ВПЧ).
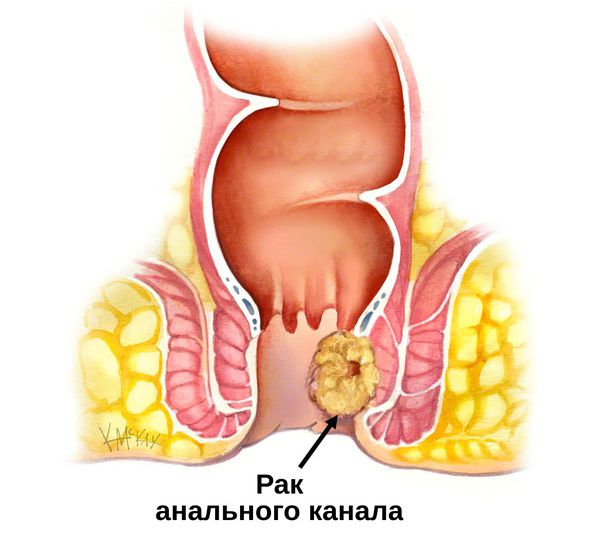
Опухоль анального канала
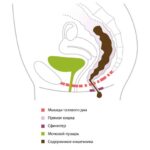
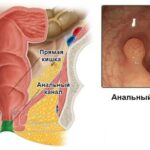
Анальный канал — это короткая трубка длиной в среднем около 2 сантиметром у женщин и 3 сантиметров у мужчин, в которую переходит прямая кишка. Это завершающий участок пищеварительного тракта. Анальный канал образован мышечным комплексом, который включает в себя два сфинктера (внутренний и наружный) и самые дальние пучки леваторов (мышц, поднимающих задний проход). Сфинктеры как два кольца расположены друг над другом и разделены особенной анатомической структурой — зубчатой линией, которая позволяет чувствовать позыв к испражнению.
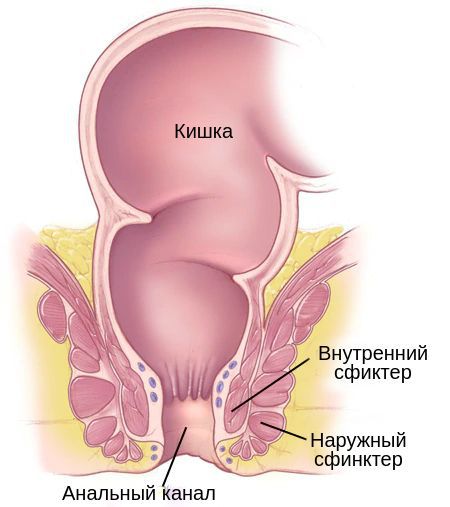
Внешний и наружный сфинктер анального канала
Частота встречаемости рака анального канала в настоящий момент составляет 2 на 100 000 в год, есть тенденция к повышению на 1-3 % ежегодно . Частота распространения заболевания растёт в связи с ростом распространенности наиболее сильных факторов риска — вируса иммунодефицита человека (ВИЧ) и вируса папилломы человека (ВПЧ), главным образом подтипа ВПЧ-16 .
Данное заболевание зачастую ассоциировано со снижением иммунитета, например, после пересадки органов или на фоне приёма медикаментов . Другими факторами риска являются:
- дисплазия шейки матки как ВПЧ-ассоциированное состояние;
- аутоиммунные заболевания (например, системная красная волчанка);
- ревматоидный артрит;
- язвенный колит;
- полипы анального канала;
- курение сигарет ;
- тяжелое течение свищевой формы болезни Крона .
Рак анального канала не является наследственным заболеванием, его развитие связано прежде всего с ВПЧ.
Рак анального канала в 100% случаев приводит к летальному исходу при отсутствии лечения. Но злокачественные опухоли данной локализации можно полностью вылечить, если вовремя начать терапию. По статистике наиболее часто данное заболевание развивается после 45 лет, однако люди между 35 и 44 годами составляют 10 % больных .
Распространение злокачественного процесса в лимфатические узлы диагностируют у 15-30 % пациентов в момент установки диагноза. Отдаленные метастазы в другие органы, например, лёгкие, печень и кости, встречаются в 10-17 % случаев. При длительном росте опухоль может повреждать элементы сфинктерного аппарата, который регулирует процесс дефекации.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака анального канала
Наиболее частой жалобой, с которой обращаются к врачу-колопроктологу пациенты при наличии рака анального канала, является боль в области заднего прохода .
Зачастую при появлении кровянистых следов на бумаге или капель крови в области заднего прохода люди путают эти настораживающие симптомы с проявлениями геморроя или анальной трещины. Часто это является причиной, по которой пациенты откладывают диагностику.
Наличие «шишки» или язвочки также может быть тревожным сигналом — даже самые, на первый взгляд, безобидные дефекты могут оказаться злокачественной опухолью.
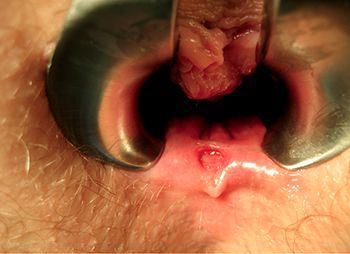
Небольшая язва анального канала
Зуд в области заднего прохода — это не всегда признак анальной трещины или аллергической реакции, иногда злокачественные опухоли анального канала также могут сопровождаться этим симптомом.
Иногда аноректальные свищи могут быть проявлением онкологического процесса в области анального канала, но это достаточно редкий симптом. Аноректальные свищи проявляются гнойными или кровянистыми выделениями из заднего прохода или патологического отверстия в перианальной области, а также периодическими повышениями температуры.
Недержание кала в результате распространения опухоли на мышцы-сфинктеры — тревожный симптом, который требуется срочного начала лечения.
Увеличение паховых лимфатических узлов также может свидетельствовать о распространении заболевания.
Другим симптомом может быть ощущение инородного тела в области заднего прохода. При пальцевом исследовании прямой кишки может пальпироваться объёмное образование .
Патогенез рака анального канала
Имеющиеся в научной литературе данные указывают на связь между инфицированием онкогенными типами вируса папилломы человека (ВПЧ) с развитием предраковых и злокачественных поражений ануса . В настоящее время до 88 % злокачественных опухолей анального канала, имеющих гистологическое строение плоскоклеточного рака, являются положительными на ВПЧ. Самый распространенный онкогенный тип вируса папилломы человека — 16 тип. В некотором проценте случаев обнаруживается инфицирование вирусом папилломы человека 9 типа .
ВПЧ может оставаться в ядрах клеток эпителия после первоначального инфицирования слизистой оболочки, которое обычно происходит в результате сексуального контакта . Генотипы ВПЧ высокого риска (16 и 18) кодируют не менее трёх специальных «онкологических» белков со стимулирующими свойствами: белки E5, E6 и E7. Внедрение ДНК вируса в геном клетки-хозяина влияет на развитие процессов, приводящих к возникновению рака анального канала. В процессе интеграции ВПЧ происходит разрушение области E2 вирусного генома в ДНК инфицированных клеток, что приводит к потере подавляющей функции белка Е2. Это приводит к увеличению количества белков Е6 и Е7, которые участвуют в росте новообразований, связанных ВПЧ .
Классификация и стадии развития рака анального канала
Существует несколько классификаций опухолей анального канала. Одна из них, Международная гистологическая классификация, отражает особенности строения опухоли. По данным на 2015 год, подавляющее большинство новообразований (70-80 %) являются плоскоклеточным раком. На втором месте — железистый рак (аденокарцинома). Отдельно стоит выделить доброкачественные опухоли, способные к перерождению, и предраковые состояния — плоскоклеточные папилломы, остроконечные кондиломы, воспалительные клоакогенные полипы, олеогранулемы и дисплазии анального канала различной степени дифференцировки, наиболее опасными из которых являются низкодифференцированные .
Стадирование рака анального канала в современном медицинском мире осуществляется по международной классификации TNM. Итак, буква T расшифровывается как Tumor (опухоль). Это значение отражает размер опухоли. Таким образом, существует семь возможных значений данного параметра:
- Tx — данных на момент оценки не достаточно;
- T0 — первичной опухоли по данным обследований нет;
- Tis — опухолевые клетки, расположенные поверхностно, без вовлечения более глубоких структур (преинвазивный рак);.
- T1 – наибольший диаметр опухоли составляет 2 см и менее;
- T2 – опухоль размером от 2 до 5 см;
- T3 – опухоль больше 5 см в своем наибольшей диаметре;
- Т4 – опухоль прорастает в окружающие органы и ткани (например, влагалище или мочевой пузырь), но если опухолевый процесс распространяется на кожу, подкожную жировую клетчатку или сфинктерный аппарат, то её не классифицируют как Т4.
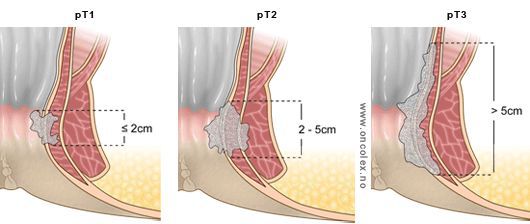
Стадии рака анального канал (размеры опухоли)
Буква N определяет распространение онкологического процесса в регионарные (местные) лимфатические узлы — наличие или отсутствие метастазов.
Регионарные лимфоузлы анального канала:
- мезоректальные лимфатические узлы (структуры, расположенные вокруг прямой кишки);
- латеральные (по ходу внутренних подвздошных сосудов);
- паховые;
- поверхностные лимфатические узлы.
По классификации TNM выделяют следующие состояния регионарных лимфоузлов:
- Nx — данных на момент оценки недостаточно;.
- N0 — нет поражения регионарных лимфатических узлов;
- N1 — есть данные о метастазах в лимфатические узлы мезоректальной клетчатки;
- N2 — есть данные о метастазах во внутренние подвздошные и/или паховые лимфоузлы с одной стороны;
- N3 — есть данные о метастазах во внутренние подвздошные и/или паховые лимфоузлы с двух сторон.
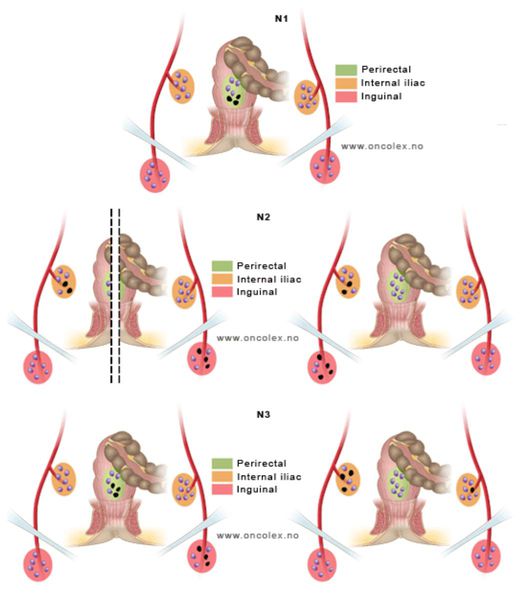
Стадии рака анального канал (состояние лимфоузлов)
Буква М в классификации TNM отражает распространение опухолевого процесса в отдаленные органы:
- М0 — нет отдаленных метастазов;
- М1 — есть отдаленные метастазы .
На основании сочетания параметров Т, N и М устанавливается стадия заболевания — I, II, III или IV.
- I стадия – небольшая опухоль без метастазов
- II стадия – более крупная опухоль без метастазов
- III стадия – любая опухоль с метастазами только в окружающие её лимфатические узлы
- IV стадия – любая опухоль с метастазами в другие органы, вне зависимости от наличия метастазов в ближайших лимфатических узлах.
Осложнения рака анального канала
Рак анального канала — заболевание, способное к быстрому распространению. Лечение при постановке диагноза следует начать незамедлительно.
Учитывая злокачественную природу новообразования, опухоль способна распространяться на соседние органы, провоцируя появление соответствующих симптомов — боль при сексуальном контакте, нарушения мочеиспускания, импотенция, гнойные осложнения, появление стриктуры (выраженного сужения) анального канала, возникновения проблем с удержанием кала при поражении мышц-сфинктеров .
На момент диагностирования 12 % больных имеют отдалённые метастазы. В дальнейшем метастазы развиваются ещё у 10–20 % пациентов . Наиболее часто поражается печень, реже — лёгкие, лимфатические узлы, брюшина и костная ткань.
Диагностика рака анального канала
При появлении симптомов рака анального канала следует обратиться к врачу-колопроктологу. Тщательное пальцевое обследование анального канала, прямой кишки и визуальный осмотр (ректороманоскопия) перианальной области может дать важную информацию о наличии, местоположении и распространенности опухоли анального канала.
У женщин осмотр и пальпация влагалища и области промежности помогают определить степень вовлечения в заболевание перегородки между прямой кишкой и влагалищем. Если пальцевое исследование сопровождается выраженной болезненностью, следует повторить осмотр в условиях операционной с общей или спинальной анестезией.
При подозрении на злокачественный процесс врач должен взять биопсию — кусочек измененных тканей, который потом отправляется на гистологическое исследование.
Приблизительно у трети пациентов с раком анального канала определяются увеличенные паховые узлы, но только 50 % из них оказываются метастатическими . Лимфатические узлы с метастазами около прямой кишки могут быть обнаружены также при пальцевом обследовании, но современные методы лучевой диагностики для визуализации опухоли более точны.
Позитронно-эмиссионная томография(ПЭТ) позволяет оценить состояние лимфатических узлов с выявлением патологического поглощения, даже если клинические свидетельств поражения отсутствуют. Кроме того при подозрении на поражение лимфатических узлов следует провести биопсию. В случае отрицательного результата по данным биопсии рекомендовано диагностическое хирургическое вмешательство — полноценное удаление пахового лимфатического узла для более точного и расширенного гистологического исследования.
Позитронно-эмиссионная томография
В диагностике рака анального канала широко используется магнитно-резонансная томография (МРТ). Этот безопасный с точки зрения облучения метод позволяет оценить степень инвазии (распространения) опухоли на окружающие структуры, а также заподозрить наличие метастатических лимфатических узлов.
С целью исключения метастазов в отдаленные органы, например, лёгкие и печень, часто применяют компьютерную томография (КТ) с внутривенным контрастированием. Этот метод необходим также и для составления плана лечения опухоли.
Анализ крови на маркер SCC (онкомаркер) может быть информативен только в процессе лечения для контроля за его эффективностью, в качестве первичной диагностики сдавать его не нужно.
Лечение рака анального канала
В лечении образований анального канала применяются различные методики, но в большинстве случаев полного излечения удается достичь без применения радикального хирургического вмешательства.
При кондиломах или низкодифференцированной дисплазии анального канала (предраковых состояниях) применяются местные препараты (например, 5-фторурацил) или выполняется локальное иссечение новообразования. Однако существует высокий процент рецидивов образований (около 59 %), что требует тщательного наблюдения после лечения.
При карциноме in situ (без метастазирования) выполняется локальное иссечение в пределах здоровых тканей. Выполнение лазерного удаления опухоли возможно в отдельных клинических ситуациях .
Небольшие опухоли анального канала (T1N0) могут быть удалены с помощью локального иссечения в пределах здоровых тканей (1 см от границы опухоли). При рецидивах опухоли после локального иссечения повторное малоинвазивное вмешательство возможно лишь у пациентов, которым можно сохранить функцию держания (нормальной работы сфинктера).
Карциномы T2N0 имеют повышенный риск метастазирования в паховые лимфатические узлы, в этом случае проводится облучение как первичной опухоли, так и паховых лимфатических узлов с обеих сторон. Применение химиолучевой терапии целесообразно в отдельных клинических ситуациях. Это позволяет увеличить эффективность лечения раннестадийных опухолей на 55 % .
Стандартом лечения образований на более поздних стадиях (T3-T4 или N1-N3) является применение химиолучевой терапии. Выявление единичных клеток опухоли по данным биопсии после прохождения терапии может говорить о ремиссии заболевания, однако в таких случаях следует выполнять повторную биопсию через 6 недель. Для пациентов, которые уже проходили курсы химиолучевой терапии, в случае рецидива эффективно оперативное вмешательство — брюшно-промежностная экстирпация прямой кишки с выведением постоянной стомы (трубки) на переднюю брюшную стенку. При данном вмешательстве прямая кишка удаляется навсегда .
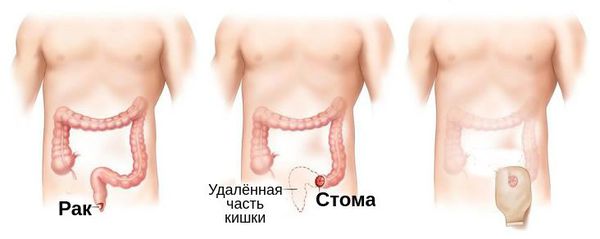
Брюшно-промежностная экстирпация
В случаях местнораспространенной карциномы методом выбора является химиолучевая терапия.
Лечение местнораспространненых опухолей анального канала подразумевает выполнение лучевой терапии в комбинации с применением 5-фторурацила и митомицина С. Эта стратегия позволяет уменьшить количество рецидивов на 23 % по сравнению с лучевой терапией. По результатам наблюдения в течение 13 лет было выявлено значительное снижение онкологической смертности на 33 % в группе комбинированной терапии .
Текущие рекомендации по лечению пациентов с раком анального канала старше 75 лет не подразумевают снижение дозы излучения у пациентов, физическое состояние которых удовлетворительно (не имеющих тяжелых сопутствующих заболеваний и ведущих активный образ жизни) .
При рецидивах опухоли в области тазовых лимфоузлов показано выполнение лучевой терапии (если не выполнялась ранее).
Лимфодиссекция — удаление лимфоузлов вместе с опухолью и подкожной клетчаткой в месте её образования (операция Дюкена) выполняется в случае неэффективности лучевой терапии.
Прогноз. Профилактика
После завершения курса химиотерапии обязательны регулярные осмотры пациента на протяжении следующих двух лет. Это необходимо для того, чтобы вовремя отследить возникновение рецидива. Окончательный эффект химиотерапии оценивается спустя 6 месяцев после завершения лечения.
Гистологическая форма опухоли анального канала не влияет на прогноз заболевания. Один из наиболее важных неблагоприятных для прогноза факторов — поражение лимфатических узлов, которое провоцирует развитие рецидива. Неблагоприятным фактором является также мужской пол .
У ВИЧ-инфицированных пациентов заболевание протекает тяжелее, однако антиретровирусная терапия позволяет применять стандартные для новообразований методы лечения.
В нескольких исследованиях изучалось влияние курения на прогноз при раке анального канала. Их результаты достоверно указывают, что у курильщиков течение заболевания проходит хуже, а прогноз при лечении более неблагоприятен .
Определенный выбор образа жизни может помочь предотвратить рак анального канала. Одной из наиболее важных задач является предотвращение инфицирования ВПЧ. Некоторые способы снижения вероятности заражения ВПЧ:
- использовать презервативы во время полового акта;
- исключить табакокурение;
- вакцинирование против ВПЧ — помогают защитить от определенных типов вируса. Применение вакцины против ВПЧ по исследованиям сопровождалось значительным снижением риска развития рака анального канала . Но если вирус папилломы человека уже присутствует в организме, вакцина не будет эффективной.
В рамках скрининга рака анального канала следует раз в три года начиная с возраста 40 лет выполнять колоноскопию, а также обращаться к врачу-колопроктологу при появлении любых новообразований в перианальной области.
Список литературы
- Grulich AE, Poynten IM, Machalek DA, Jin F, Templeton DJ, Hillman RJ. The epidemiology of anal cancer. Sex Health. 2012 Dec;9(6):504-8.ссылка
- Johnson LG, Madeleine MM, Newcomer LM, Schwartz SM, Daling JR. Anal cancer incidence and survival: the surveillance, epidemiology, and end results experience, 1973-2000. Cancer. 2004;101:281–288ссылка
- Uronis HE, Bendell JC. Anal cancer: an overview. Oncologist. 2007;12:524–534ссылка
- Hoots BE, Palefsky JM, Pimenta JM, Smith JS. Human papillomavirus type distribution in anal cancer and anal intraepithelial lesions. Int J Cancer. 2009;124:2375–2383ссылка
- Barral M, Dohan A, Allez M, Boudiaf M, Camus M, Laurent V, et al. Gastrointestinal cancers in inflammatory bowel disease: an update with emphasis on imaging findings. Crit Rev Oncol Hematol. 2016;97:30–46ссылка
- Epidermoid anal cancer: results from the UKCCCR randomised trial of radiotherapy alone versus radiotherapy, 5-fluorouracil, and mitomycin. UKCCCR Anal Cancer Trial Working Party. UK Co-ordinating Committee on Cancer Research. Lancet. 1996;348:1049–1054ссылка
- Welton, M. L. and Raju, N. Chapter 20, “Anal Cancer” Chapter in Beck, D. E., Roberts, P. L., Saclarides, T. J., Senagore, A. J., Stamos, M. J., Wexner, S. D., Eds. ASCRS Textbook of Colon and Rectal Surgery, 2nd Edition. Springer, New York, NY; 2011
- Ostrbenk A, Kocjan BJ, Hosnjak L, et al. Identification of a novel human papillomavirus, type HPV199, isolated from a nasopharynx and anal canal, and complete genomic characterization of papillomavirus species gamma-12. PLoS One 2015;10(9)ссылка
- Hoff PM, Coudry R, Moniz CM. Pathology of Anal Cancer. Surg Oncol Clin N Am. 2017 Jan;26(1):57-71ссылка
- Hellner K, Munger K. Human papillomaviruses as therapeutic targets in human cancer. J Clin Oncol 2011;29(13)ссылка
- Mai S, Welzel G, Ottstadt M, et al. Prognostic relevance of HPV infection and p16overexpression in squamous cell anal cancer. Int J Radiat Oncol Biol Phys 2015;93(4):819–27ссылка
- Klingelhutz AJ, Roman A. Cellular transformation by human papillomaviruses:lessons learned by comparing high- and low-risk viruses. Virology 2012;424(2):77–98ссылка
- Барсуков Ю.А., Шелыгин Ю.А. Клинические рекомендации по диагностике и лечению больных раком анального канала, анального края и перианальной кожи. Москва, 2014: 6-7.
- Glynne-Jones R, Kadalayil L, Meadows HM, Cunningham D, Samuel L4, Geh JI et al. Tumour-and treatment-related colostomy rates following mitomycin C or cisplatin chemoradiation with or without maintenance chemotherapy in squamous cell carcinoma of the anus in the ACT II trial. Ann Oncol 2014; 25(8)ссылка
- Schwarz JK, Siegel BA, Dehdashti F, Myerson RJ, Fleshman JW, Grigsby PW. Tumor response and survival predicted by post-therapy FDG-PET/CT in anal cancer. Int J Radiat Oncol Biol Phys 2008; 71(1): 180-6.ссылка
- Klas JV, Rothenberger DA, Wong WD, Madoff RD. Malignant tumors of the anal canal: the spectrum of disease, treatment, and outcomes. Cancer 1999; 85(8ссылка
- Bandieramonte G, Bono A, Zurrida S, Bartoli C, de Palo G. Laser surgery for small perianal neoplasms. Eur J Cancer 1993; 29A(11)ссылка
- Mendenhall WM, Zlotecki RA, Vauthey JN, Copeland EM 3rd. Squamous cell carcinoma of the anal margin treated with radiotherapy. Surg Oncol 1996; 5(1)ссылка
- Northover J, Glynne-Jones R, Sebag-Montefiore D, James R, Meadows H, Wan S et al. Chemoradiation for the treatment of epidermoid anal cancer: 13-year follow-up of the first randomised UKCCCR Anal Cancer Trial (ACT I). BrJ Cancer 2010; 102(7)ссылка
- Lestrade L, De Bari B, Montbarbon X, Pommier P, Carrie C. Radiochemotherapy and brachytherapy could be the standard treatment foranal canal cancer in elderly patients? A retrospective single-centre analysis. Med Oncol 2013; 30(1)ссылка
- Palefsky JM, Garner EI. HPV vaccine against anal HPV infection and anal intraepithelial neoplasia. N Engl J Med 2011; 365: 1576-1585ссылка
- Horner M., Ries L., Krapcho M., et al. SEER Cancer Statistics Review, 1975–2006
- Arnott S., Cunningham J., Gallagher J., UK Co-ordinating Committee on Cancer Research Anal Cancer Trial Working Party. Epidermoid anal cancer: results from the UKCCCR randomised trial of radiotherapy alone versus radiotherapy, 5-fluorouracil, and mitomycin. Lancet. 1996ссылка