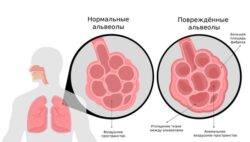
Синдром Пьера Мари — Бамбергера (Pierre Marie — Bamberger syndrome) — это поражение костей и суставов, которое развивается на фоне хронических воспалительных или онкологических заболеваний, чаще с вовлечением лёгких (например, при раке лёгкого или хронических лёгочных инфекциях) .
Синонимы: вторичная гипертрофическая остеоартропатия (ГОАП), лёгочная остеодистрофия, гипертрофическая лёгочная остеопатия, акропахия.
Синдром проявляется болями в костях и суставах, изменением концевых фаланг и ногтей (так называемыми, часовыми стёклами и барабанными палочками).
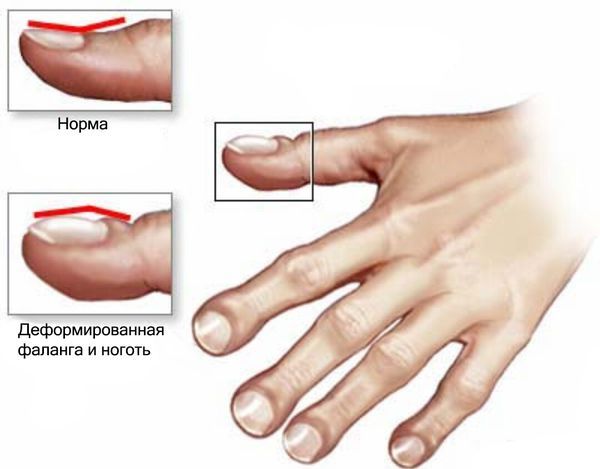
Часовые стёкла и барабанные палочки
Впервые синдром был описан французским неврологом Пьером-Мари и австрийским врачом Бамбергером, отсюда и название патологии.
Чаще всего гипертрофическая остеоартропатия (ГОАП) — это первое проявление рака лёгких и плевры. Так, синдром может сочетаться с операбельной стадией немелкоклеточного рака лёгкого.
Часто пациенты с этим синдромом безуспешно наблюдаются и лечатся у ревматологов с подозрением на заболевания суставов, что приводит к поздней диагностике рака. Нередко таким пациентам ошибочно выставляется диагноз «деформирующий остеоартроз».
Распространённость
Точная распространённость синдрома ГОАП не определена, но известно, что он развивается в 80 % случаев злокачественных опухолей лёгких . Чаще всего он возникает в 40–50 лет.
Есть противоречивые данные о том, кто болеет этим синдромом чаще. По одним данным, среди мужчин он встречается в пять раз чаще, чем среди женщин . Однако по информации из журнала Chest, он чаще возникает у женщин, чем у мужчин (40 против 19 %) .
Причины синдрома Мари — Бамбергера
Синдром может развиться:
- при раке лёгкого;
- хронических инфекционных или неинфекционных заболеваниях лёгких (например, при ХОБЛ, эмфиземе, бронхоэктатической болезни, туберкулёзе);
- аневризме аорты;
- воспалительных заболеваниях кишечника (неспецифическом язвенном колите и болезни Крона);
- поражении печени (первичном билиарном циррозе, опухоли жёлчных протоков, хроническом активном гепатите);
- гипертиреозе.
В очень редких случаях ГОАП бывает самостоятельным наследственным заболеванием. Такую первичную форму гипертрофической остеоартропатии называют пахидермопериостозом, или синдромом Турена — Соланта — Голе .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы синдрома Мари — Бамбергера
ГОАП проявляется периоститом длинных трубчатых костей — воспалением надкостницы. В ней находится много нервных окончаний, поэтому воспаление вызывает сильную боль в трубчатых костях, соседних суставах и сковывает движения. Могут возникать контрактуры — ограничение пассивных движений в суставе, при котором не получается полностью согнуть или разогнуть руку или ногу. Также может развиться синовит — поражение тканей, покрывающих сустав .
Иногда отмечается пахидермия (утолщение кожи лица и кистей), акне, себорея, бледность кожи, повышенная потливость ладоней и стоп (ладонно-подошвенный гипергидроз).
При раке лёгкого отличительной особенностью синдрома Мари — Бамбергера является симметричность, т. е. одновременное поражение костей с двух сторон. Пациентов беспокоят жгучие боли в костях рук и ног, отёк и скованность суставов пальцев. На фоне злокачественных опухолей синдром начинается остро, с сильной боли и скованности в руках и ногах по утрам. Пациенты жалуются на мышечную слабость, утолщение концевых фаланг пальцев рук и ног по типу барабанных палочек, изменение ногтей по типу часовых стёкол .
Клинические проявления синдрома варьируют: от лёгких болей в запястьях, лучезапястных, локтевых, голеностопных и коленных суставах до постоянных мучительных болей.
Патогенез синдрома Мари — Бамбергера
Синдром Мари — Бамбергера (в отличие от первичной формы ГОАП) — это всегда проявление какого-то другого заболевания: хронического воспалительного или онкологического, чаще всего рака лёгкого. Исходя из определения заболевания, гипертрофическая остеоартропатия — это разрастание, увеличение концевых отделов трубчатых костей.
Трубчатые кости бывают длинными и короткими. К длинным костям относятся бедренная, большеберцовая, малоберцовая, плечевая, локтевая и лучевая; к коротким — пястные, плюсневые кости и фаланги пальцев.
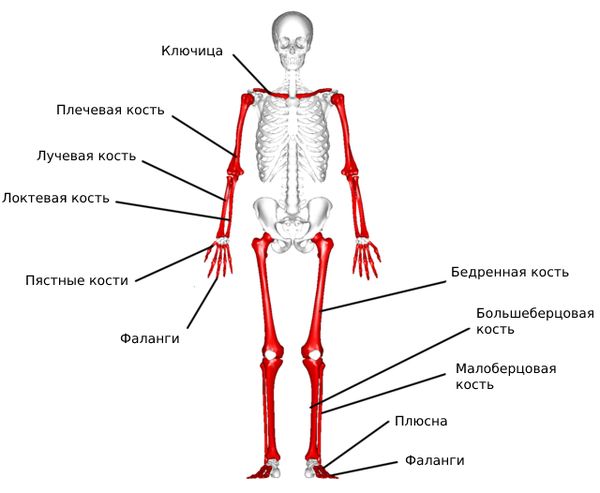
Трубчатые кости
Гипертрофические нарушения вызваны асептическим воспалением, т. е. не связанным с инфекцией. При этом развивается отёк капиллярного ложа, разрастаются капилляры и соединительная ткань с избытком коллагеновых волокон .
Синдром часто опережает развитие опухоли, нередко предшествует заболеванию на 6–20 лет, хотя является для него вторичным признаком .
На фоне рака лёгкого ГОАП начинается остро с сильной боли и быстрой деформации пальцев и ногтей. На фоне хронических заболеваний синдром развивается постепенно с развёрнутой клинической картиной основного заболевания. Например, при развитии ГОАП на фоне бронхоэктазов вначале возникает кашель с гнойной мокротой и повышается температура тела, а уже после этого появляются клинические симптомы остеоартропатии.
Считается, что к развитию синдрома приводит несколько факторов:
- Ухудшение работы лёгких при лёгочной гипертензии (повышении давления в лёгочной артерии).
- Увеличение уровня фактора роста фибробластов (ФРФ) за счёт повышенной выработки или нарушения элиминации. Элиминация — это самопроизвольное устранение, рассасывание ФРБ. Например, любое воспаление или повреждение кожи повышает уровень ФРФ, но заживление раны — это сигнал к прекращению выработки и «самоуничтожению» ФРФ. С остеоартропатией на фоне рака или воспалительных заболеваний этот механизм нарушается.
- Высокий уровень антигена фактора Виллебранда в крови, который помогает тромбоцитам прикрепляться к участку повреждённого сосуда.
- Избыток сосудистого эндотелиального фактора роста (СЭФР) из-за гипоксии — пониженного содержания кислорода в организме или отдельных тканях . При длительной гипоксии, воспалении или мутации, в том числе на фоне онкологического заболевания, повышается уровень СЭФР. Он, в свою очередь, стимулирует костную перестройку и образование соединительной ткани (изменяется экспрессия структурных генов коллагенов типа I и II), что проявляется симптомами синдрома Мари — Бамбергера .
Предложены две гипотезы патогенеза гипетрофической остеоартропатии: нейрогенная и гуморальная.
Согласно нейрогенной гипотезе, изменения в костях скелета и коже возникают из-за повышенной активности парасимпатического отдела вегетативной нервной системы. В норме она отвечает за то, чтобы организм накапливал и восстанавливал запасы энергии во время сна, покоя и отдыха. Например, под её влиянием замедляется ритм сердца и активизируется пищеварение.
Главным нервом парасимпатической системы является блуждающий нерв. Он отвечает за связь между желудочно-кишечным трактом, сердцем и другими органами, регулирует пищеварение, иммунную систему и воспаление.
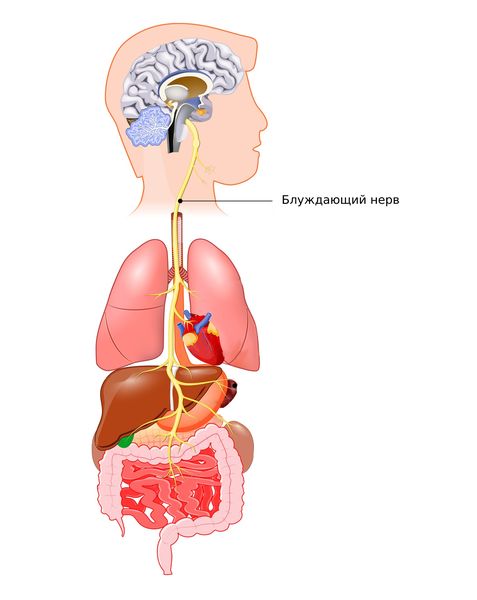
Блуждающий нерв
При избыточной активности этого нерва расширяются сосуды, увеличивается кровоток в руках и ногах, что приводит к симптомам ГОАП . Эта теория подтверждается тем, что проявления синдрома уменьшаются после внутригрудной или шейной ваготомии — рассечения основного ствола или ветви блуждающего нерва .
Симпатическая нервная система стимулирует расход энергии в стрессовых ситуациях. Под её влиянием учащается пульс, ускоряется дыхание и повышается давление при сильном напряжении и опасности. В нормальных условиях симпатическая и парасимпатическая системы уравновешивают друг друга.
Согласно второй, гуморальной теории, симптомы ГОАП формируются под влиянием цитокинов и факторов роста, в том числе тромбоцитарного фактора роста и СЭФР .
Классификация и стадии развития синдрома Мари — Бамбергера
Единой классификации вторичной ГОАП не существует. Проявления синдрома различаются по уровню поражения суставов: могут страдать руки или ноги.
Также различают острое и постепенное начало синдрома. При остром начале выражена боль и утренняя скованность, что характерно для онкологических процессов. При постепенном начале изменяется конфигурация суставов, форма ногтевых фаланг пальцев и преобладают симптомы основного заболевания.
Течение ГОАП волнообразное: периоды обострения с усилением болей сменяются уменьшением симптомов.
Осложнения синдрома Мари — Бамбергера
Осложнения ГОАП связаны с усиленным образованием новых сосудов — неоангиогенезом, а также избыточным отложением соединительной ткани. Всё это приводит к образованию новой костной ткани, что сопровождается жжением, нарушением чувствительности в фалангах пальцев, скованностью кистей или стоп, потливостью ладоней и ступней . Эти симптомы можно считать как проявлением синдрома, так и осложнением, когда лечение не начато вовремя и изменения прогрессируют.
Диагностика синдрома Мари — Бамбергера
Неспецифичные жалобы, в особенности поражение суставов и костей, нередко заводят врача в тупик — он начинает подозревать другие заболевания, например ревматологические, в частности деформирующий остеоартроз. Это приводит к потере драгоценного времени, неправильному лечению, финансовым тратам и тяжёлым последствиям. Поэтому нужно быть внимательным к неспецифическим симптомам онкологических заболеваний (паранеопластическим синдромам).
Сбор анамнеза и осмотр
При сборе анамнеза врач обращает особое внимание на боль или другие неприятные ощущения в костях и суставах, а также на изменение кожи и ногтей. Отличительным признаком синдрома Мари — Бамбергера являются пальцы Гиппократа — утолщение концевых фаланг пальцев кистей и стоп по типу барабанных палочек.
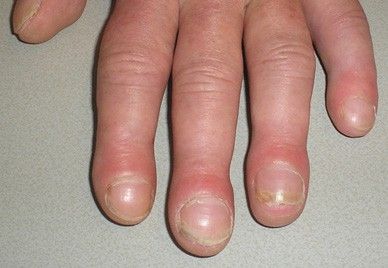
Пальцы Гиппократа [25]
Также при этом синдроме ограничен объём движений в поражённых суставах и может появиться отёк из-за выпота в крупных суставах: коленных, голеностопных, лучезапястных.
Кроме того, может возникать утолщение кожи и фолликулит — расширение волосяных фолликулов из-за повышенного скопления роговых масс. Ещё при ГОАП становится больше потовых и сальных желёз, а также объём и количество железистых клеток . Доктор может увидеть эти изменения под микроскопом.
Инструментальная диагностика
Рентгенологическое исследование — это один из наиболее информативных методов диагностики синдрома.
При таком обследовании можно выявить разрушение костной ткани, к которой нередко приводит её перестройка .
К специфическим рентгенологическим признакам синдрома относится симметричное поражение диафизов длинных трубчатых костей — разрастание и утолщение надкостницы. Эпифизы при этом не изменяются.
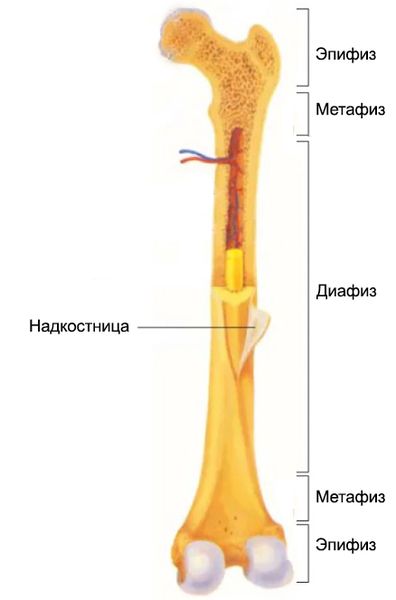
Строение трубчатой кости
Со временем при ГОАП повреждённых костей становится больше и увеличивается протяжённость поражения, что видно при рентгенографии.
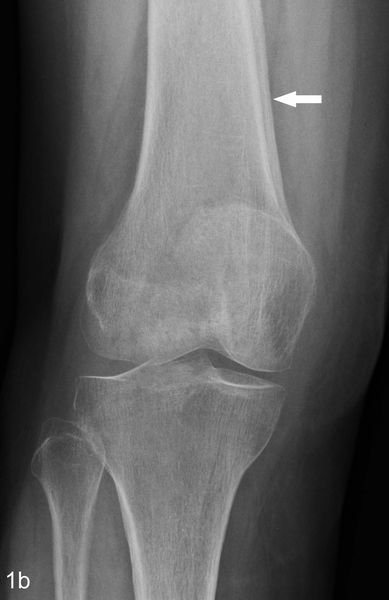
Поражение костей при ГОАП [26]
В лёгких случаях патологические изменения наблюдаются только в голенях малоберцовых костей, в тяжёлых — во всех трубчатых костях, при этом вовлекаются диафизы и метафизы. Периостоз (увеличение надкостницы) на снимках выглядит как тень неправильной конфигурации .
Инструментальные исследования (рентгенография органов грудной клетки, ультразвуковое исследование органов брюшной полости и сердца, эндоскопические методы исследования и т. п.) также помогают выявить заболевания, сопровождающиеся признаками ГОАП .
При синдроме важно продиагностировать возможные онкологические процессы, прежде всего в лёгких. Наиболее информативным обследованием для лёгких и органов грудной клетки считается мультиспиральная компьютерная томография органов грудной клетки (МСКТ ОКГ). Она позволяет выявить даже мелкие опухоли или кальцинаты без дополнительных уточняющих обследований.
Лабораторная диагностика
Пока не предложено ни одного специфического лабораторного признака ГОАП. Неспецифическим и необязательным признаком может быть повышенный уровень маркеров костной ткани — щелочной фосфатазы, остеокальцина или аминоконцевого пропептида проколлагена I типа.
При пункции сустава жидкость невоспалительного характера, в ней содержится меньше 500 клеток в 1 мкл .
Частым лабораторным признаком является повышение СОЭ. Также врач может рекомендовать сдать анализ на онкомаркеры — СА 125, АФП.
Дифференциальная диагностика
ГОАП следует отличать от деформирующего остеоартроза, ревматоидного артрита и вторичных артропатий другого происхождения: системной красной волчанки, ювенильного артрита, анкилозирующего спондилита, остеоартрита и стероидной миопатии .
По мере исследования иммунологических, лабораторных маркеров и получения рентгенологических данных исключают ревматологическое заболевание.
Также ГОАП следует отличать от акромегалии — заболевания, которое развивается при нарушении работы передней доли гипофиза. Проявляется увеличением размеров и утолщением костей лица, черепа, рук и ног. Пациентов могут беспокоить головные боли, утомляемость, снижение интеллектуальных способностей, боли в крупных суставах, повышение артериального давления, потливость, гиперпигментация кожи в складках, изменение голоса. Заболевание диагностируют по внешним признакам. Также по анализам определяют повышенный уровень соматотропного гормона, положительный оральный тест на толерантность к глюкозе и гиперкальциурию — высокое содержание кальция в моче. Нередко рентгенологически диагностируют опухоль гипофиза .
Лечение синдрома Мари — Бамбергера
Специфической терапии ГОАП не существует — нужно лечить основное заболевание. Но если выявить его не удаётся, проводится симптоматическое лечение и пациент наблюдается у терапевта и ревматолога.
При выраженном болевом синдроме назначают нестероидные противовоспалительные препараты (НПВП). Результаты их использования при данном синдроме противоречивы, но известно, что они уменьшают признаки воспаления . Чтобы ослабить боль и снизить количество жидкости в суставах, используют Эторикоксиб .
Для уменьшения боли при рефрактерном артрите (одном из проявлений синдрома) применяют:
- Инфликсимаб — моноклональные антитела к фактору некроза опухоли (ФНО-α);
- Гефитиниб — ингибитор СЭФР, тирозинкиназы EGFR;
- Тамоксифен — противоопухолевый препарат, который обладает комбинированным действием как антагониста, так и агониста эстрогена в различных тканях .
При утолщении кожи применяют ретиноиды — препараты, которые содержат витамин А или химические соединения, схожие с ним. Они снижают выработку кожного сала, уменьшают воспаление и снижают способность фибробластов синтезировать коллаген . При выраженных косметических недостатках лечение проводят косметологи с помощью хирургических методов и введения ботулотоксина типа А.
При выраженных трофических нарушениях кожи проводится ваготомия или чрескожная блокада блуждающего нерва. Ваготомия — это хирургическое удаление части блуждающего нерва. Операция позволяет избавиться от жгучих болей в костях рук, ног и повышенной потливости.
Артропатия проходит после хирургического удаления опухолей средостения, лёгких и плевры либо после лечения обострения хронического воспаления.
Прогноз. Профилактика
Развитие ГОАП не влияет на продолжительность жизни. Но игнорирование симптомов этого синдрома может привести к поздней диагностике и несвоевременному лечению злокачественной опухоли, что может стать причиной гибели пациента.
Специфической профилактики не существует. При изменении кожи на руках и ногах, болях в суставах, повышенной потливости кожи нужно пройти комплексное обследование и лечить выявленное заболевание .
Список литературы
- Крылов А. С., Щипахина Я. А., Фёдорова А. В. и др. Вторичная гипертрофическая остеоартропатия (синдром Пьера Мари — Бамбергера) // Вестник рентгенологии и радиологии. — 2017. — № 5. — С. 251–255.
- Tsai M. Y., Jo-Ching W., Wu F. Z. Hypertrophic pulmonary osteoarthropathy in a patient with lung cancer // Intern Med. — 2014. — № 23. — Р. 2757–2578. ссылка
- Потапова М. В., Гриценгер В. Р., Липатова Т. Е. и др. Гипертрофическая остеоартропатия как паранеопластический синдром у больного с раком лёгкого: клинический случай // Кубанский научный медицинский вестник. — 2015. — № 2. — С. 128–131.
- Ito T., Goto K., Niho S. Hypertrophic pulmonary osteoarthropathy as a paraneoplastic manifestation of lung cancer // Thorac oncol. — 2010. — № 5. — P. 976–980. ссылка
- Zhang Z., Zhang C., Zhang Z. Primary hypertrophic osteoarthropathy: an update // Front Med. — 2013. — № 1. — Р. 60–64. ссылка
- Трисветова Е. Л. Первичная гипертрофическая остеоартропатия // Научно-практическая ревматология. — 2020. — № 5. — С. 544–549.
- Uppal S., Diggle C. P., Carr I. M. et al. Mutations in 15-hydroxyprostaglandin dehydrogenase cause primary hypertrophic osteoarthropathy // Nat Genet. — 2008. — № 6. — Р. 789–793. ссылка
- Treasure T. Hypertrophic pulmonary osteoarthropathy and the vagus nerve: an historical note // J R Soc Med. — 2006. — № 8. — Р. 388–390. ссылка
- Yao Q., Altman R. D., Brahn E. Periostitis and hypertrophic pulmonary osteoarthropathy: report of 2 cases and review of the literature // Semin Arthritis Rheum. — 2009. — № 6. — Р. 458–466.ссылка
- Giancane G., Diggle C. P., Legger E. G. et al. Primary hypertrophic osteoarthropathy: an update on patient features and treatment // J Rheumatol. — 2015. — № 11. — Р. 2211–2214.ссылка
- Martinez-Lavi M., Pineda C., Valdez T. et al. Primary hypertrophic osteoarthropathy // Semin Arthritis Rheum. — 1988. — № 3. — Р. 156–162. ссылка
- Korsten P., Bohnenberger H., Vasko R. Hypertrophic osteoarhropathy presenting as inflammatory arthritis // Arthritis Rheumatol. — 2015. — № 11. — Р. 3036. ссылка
- Sridhar K. S., Lobo C. F., Altman R. D. Digital clubbing and lung cancer // Chest. — 1998. — № 4. — Р. 1535–1537. ссылка
- Li S.-S., He G.-W., Fu W.-Z. et al. Clinical, biochemical, and genetic features of 41 han chinese families with primary hypertrophic osteoarthropathy, and their therapeutic response to etoricoxib: results from a six-month prospective clinical intervention // J Bone Miner Res. — 2017. — № 8. — Р. 1659–1666. ссылка
- Padula S. J., Broketa G., Sampieri A. et al. Increased collagen synthesis in skin fibroblasts from patients with primary hypertrophic osteoarthropathy. Evidence for trans activational regulation of collagen transcription // Arthritis Rheum. — 1994. — № 9. — Р. 1386–1394. ссылка
- Bozzao F., Bernardi S., Dore F. et al. Hypertrophic osteoarthropathy mimicking a reactive arthritis: a case report and review of the literature // BMC Musculoscelet Disord. — 2018. — № 1. ссылка
- Yap F. Y., Skalski M. R., Patel D. B. et al. Hypertrophic osteoarthropathy: сlinical and imaging features // RadioGraphics. — 2017. — № 1. — Р. 157–195. ссылка
- Shakya P., Pokhrel K., Mlunde L. B. et al. Effectiveness of nonsteroidal anti-inflammatory drugs among patients with primary hypertrophic osteoarthropathy: а systematic review // J Dermatol Sci. — 2018. — № 1. — Р. 21–26. ссылка
- DaCosta F. V., de Magalhães Souza Fialho S. C., Zimmermann A. F. et al. Infliximab treatment in pachydermoperiostosis: a rare disease without an effective therapeutic option // J Clin Rheumatol. — 2010. — № 4. — Р. 183–184. ссылка
- Kikuchi R., Itoh M., Tamamushi M. et al. Hypertrophic оsteoarthropathy secondary to lung cancer: beneficial effect of anti-vascular endothelial growth factor antibody // J Clin Rheumatol. — 2017. — № 1. — Р. 47–50. ссылка
- Armstrong D. J., McCausland E. M., Wright G. D. Hypertrophic pulmonary osteoarthropathy (HPOA) (Pierre Marie-Bamberger syndrome): two cases presenting as acute inflammatory arthritis. Description and review of the literature // Rheumatol Int. — 2007. — № 4. — Р. 399–402. ссылка
- Nguyen S., Hojjati M. Review of current therapies for secondary hypertrophic pulmonary osteoarthropathy // Clin. Rheumatol. — 2011. — № 1. — Р. 7–13. ссылка
- Фурсенко В. А., Гребенникова Т. А., Никитин А. Г., Белая Ж. Е. Пахидермопериостоз: особенности диагностики на примере клинического случая // Остеопороз и остеопатии. — 2017. — № 2. — Р. 52–57.
- Diner W. C. Hypertrophic osteoarthropathy. Relief of symptoms by vagotomy in a patienh qihh pulmonary metastases from a lympho-epithelioma of the nasopharynx // JAMA. — 1962. — № 6. — Р. 555–557. ссылка
- Roumen Р., Ooms R. Trommelstokvingers door longtumor // Medisch Contact. — 2016.
- Jobke B., Wormanns D. LuBo diseases: Disorders affecting the Lung and Bone — a Review // EPOS. — 2013.